Пухлини нирок
Етіологія
Пухлини нирок становлять велику групу новоутворень різної морфологічної структури, які розподіляють на доброякісні та злоякісні.
Серед усіх злоякісних новоутворень рак нирки становить близько 3%. Двобічні злоякісні пухлини нирок трапляються досить рідко (приблизно 1% загальної кількості пухлин нирок). Злоякісні пухлини нирок спостерігають значно частіше, ніж доброякісні (співвідношення приблизно 20:1).
Пухлини нирок поділяють на пухлини ниркової паренхіми і пухлини ниркової миски.
1. Пухлини ниркової паренхіми
Доброякісні пухлини: аденома, ліпома, фіброма, міома, ангіома, гемангіома, лімфангіома, міксома, остеома, хондрома, дермоїд.
Злоякісні пухлини: нирковоклітинний рак, фібро-, міо-, ліпо-, ангіосаркома, нефробластома (пухлина Вільмса).
Вторинна (метастатична) злоякісна пухлина нирки.
2. Пухлини ниркової миски
Доброякісні пухлини: папілома, ангіома, лейоміома.
Злоякісні пухлини: перехідно-клітинний рак, плоско клітинний рак, слизово-залозистий рак, саркома.
Серед усіх пухлин нирок у дорослих найчастіше трапляється нирковоклітинний рак, у дітей — нефробластома (пухлина Вільмса).
Нефробластома (пік захворюваності — на 3-му році життя) становить близько 6% усіх злоякісних новоутворень у дитячому віці і 85% усіх пухлин нирок у дітей. На частку мезобластомної нефроми приходиться 5% новоутворень нирок у дітей, світлоклітинної саркоми — 4%, рабдоїдної пухлини — 2%, нейрогенні і нирковоклітинні пухлини, а також ангіоміоліпома та інші рідкісні пухлини разом становлять до 4% спостережень. Нирковоклітинний рак спостерігають у 2—3% випадків усіх злоякісних новоутворень у дорослих і становить 90—95% усіх пухлин нирок серед пацієнтів даної категорії (з піком захворюваності на шостій-сьомій декаді життя), онкоцитома трапляється в 5—10%, ангіоміоліпома — в 1—2% випадків.
Доброякісні пухлини паренхіми нирок спостерігають дуже рідко — не більше ніж в 1—2% хворих з пухлинами нирок. Чоловіки хворіють майже в 2 рази частіше від жінок. Переважний вік хворих — понад 50 років. За останні роки пухлини нирок трапляються частіше, ніж це відзначалося раніше. Це можна пояснити як збільшенням у складі населення осіб літнього і старечого віку, так і значним поліпшенням діагностики захворювання, у тому числі широким використанням таких методів дослідження, як ультразвукове сканування і ниркова ангіографія.
Невеликі доброякісні пухлини нирок клінічно не проявляються і їх знаходять переважно випадково під час секції. Однак пухлини, доброякісні за гістологічною будовою, але такі, що досягли значних розмірів, проявляються клінічно як злоякісні: швидко ростуть, дають метастази. Відомі випадки, коли через деякий час після видалення нирки з приводу аденоми виявляли метастази у віддалених органах, тому всі пухлини нирок незалежно від їхньої гістологічної будови слід уважати злоякісними.
Для нирковоклітинного раку типовими є зростання показників захворюваності з півдня на північ (найвищі рівні традиційно характерні для Скандинавських країн і Північної Америки, а найнижчі — для Індії, Китаю, країн Центральної і Південної Америки), позитивна залежність від рівня економічного розвитку країни, а також у 2—3 рази вища захворюваність серед чоловіків.
В Україні захворюваність на рак нирки в середньому становить 8—10 випадків на 100 тис. населення; при цьому міські жителі хворіють частіше, ніж сільські.
На сьогодні причини розвитку пухлин нирки вивчені недостатньо. Уважають, що це захворювання поліетіологічне, однак якогось конкретного специфічного канцерогену, відповідального за розвиток раку нирок, не виявлено. У виникненні новоутворень нирки відіграють роль такі чинники: йонізувальне випромінювання, гормональні порушення, хімічні речовини, професійні і генетичні чинники. Появі атипових клітин сприяє також куріння, пероральні контрацептиви, цитостатики, нітрозаміни, ароматичні аміни, вірусоносійство, надмірна маса тіла, нераціональне харчування.
Велике значення можуть мати професійні чинники ризику в металургійній, коксохімічній, нафтопереробній промисловості, а також виробництві азбесту і органічних розчинників.
Патогенез
Патогенез нирковоклітинного раку тісно пов’язаний із загальними закономірностями канцерогенезу. Основні положення двостадійної моделі канцерогенезу можна визначити таким чином. Протягом першої стадії (ініціації) відбуваються незворотні порушення генотипу нормальної клітини, унаслідок чого вона переходить у схильний до трансформації стан. Друга стадія — стадія промоції канцерогенезу. Ініційована клітина набуває фенотипових властивостей трансформованої клітини внаслідок зміненої генної експресії.
Локально пухлина може поширюватися на капсулу нирки, проростати навколониркову клітковину, прилеглі органи, інфільтрувати ниркову миску. Однією з особливостей цієї пухлини є здатність поширюватися на ниркові вени, нижню порожнисту вену аж до лівого передсердя.
Злоякісні пухлини нирки метастазують лімфогенним і гематогенним шляхами. Лімфогенне метастазування відбувається в регіональні лімфовузли і, рідко, — у середостінні, шийні. Гематогенні метастази у хворих діагностують у легенях (55%), кістках (32%), печінці (32%), надниркових залозах (19%), головному мозку (14%).
Найнебезпечніший прояв прогресування неопластичного утворення — процес метастазування — утворення вторинних вогнищ пухлинного росту. Цей процес є основною причиною смерті онкологічних хворих. Щоб набути здатності до метастазування, клітина також повинна мати здатність проникати вглибину прилеглих тканин, у тому числі в кров і лімфатичні судини, а також виживати після надходження до судин, а потім пенетрувати і розмножуватися, утворюючи нове вогнище.
Здатність до метастазування складається з комплексу ознак, найістотніші з яких — набуття локомоторного фенотипу і підвищення протеолітичної активності, здатність стимулювати ангіогенез і створювати тим самим шляхи евакуації пухлинних клітин з первинного вогнища, пригнічувати апоптоз і набувати незалежності від субстрату. Запуск неопластичного процесу здійснюється за участі онкогенів (гени, інактивація яких веде до виникнення і / або прогресування новоутворення).
На підставі наявних даних про процес онкогенезу можна виділити такі групи маркерів прогресування раку нирки:
• маркери зміни ядра клітини;
• маркери стромальних змін у пухлинній тканині;
• маркери регуляції апоптозу;
• фактори ангіогенезу;
• молекули клітинних мембран;
• фактори росту;
• маркери проліферативної активності.
Для оцінювання прогресування пухлинного процесу використовують також хромосомні інверсії і гістохімічне визначення рівнів різних ферментів у тканинах пухлини. Ці фактори можуть мати діагностичну і прогностичну цінність (як правило, вони мають прямий або непрямий зв’язок із класичними прогностичними ознаками).
Клінічні фактори несприятливого прогнозу, які грунтуються на результатах широкомасштабних досліджень із використанням багатофакторного аналізу, включають:
• зниження маси тіла (>10%), збільшена ШОЕ (> 30 мм/год), анемію (рівень гемоглобіну < 10—13 г/дл), гіперкальціємію (> 10 мг/дл), зростання рівня гострофазових білків;
• соматичний статус за шкалою Карновського < 80%;
• підвищення більше ніж в 1,5 разу рівня лактатдегідрогенази;
• відсутність в анамнезі нефректомії, тривалий безрецидивний період після виконання радикальної нефректомії (> 24 міс.);
• короткий інтервал між часом діагностування захворювання і початком системного лікування хворого на дисемінований нирковоклітинний рак.
Серед патоморфологічних критеріїв несприятливого прогнозу виділяють:
• високі pTNM і ступінь ядерної градації (табл. 24);
• світлоклітинний варіант нирковоклітинного раку;
• наявність ділянок саркомоподібного росту;
• рак збірних проток;
• мікросудинна інвазія.
Серед молекулярних (імуногістохімічних) маркерів несприятливого прогнозу називають: високу експресію маркерів проліферації, молекул міжклітинної адгезії, білків пухлино-супресорних генів і онкогенів. Певне прогностичне значення мають і демографічні характеристики.

Патологічна анатомія
Макроскопічно нирковоклітинний рак являє собою пухлину сферичної форми, що розташовується в кірковій речовині нирки і поширюється на периферійні тканини. Справжня капсула відсутня, але по периферії пухлини може бути ущільнення з фіброзної тканини і запальних клітин — фасція Героти — часто вона є бар’єром для інвазії в навколо-ниркову клітковину.
На розрізі пухлина, як правило, неоднорідна через численні крововиливи, некрози, ділянки фіброзу, кісти і кальцифікати. Переважають пухлини жовтого кольору, що зумовлено накопиченням внутрішньоклітинних ліпідів. Коричневе забарвлення мають пухлини з великою кількістю гранульованих клітин (містять цитохромні ферменти). Пухлини, що складаються з веретеноподібних клітин, менше пігментовані — сірі або білуваті.
Пухлина добре васкуляризована. Через неповноцінність пухлинних судин для раку нирки типові численні крововиливи. Інші мікроскопічні ознаки — некрози, фібрози, депо гемосидерину, псамозні тільця, поодинокі мононуклеарні інфільтрати. Виражену запальну реакцію спостерігають рідко.
При гістологічному дослідженні визначають такі форми нирковоклітинного раку:
1) конвекційний (типовий, світлоклітинний) — його діагностують у 60—65% хворих на нирковоклітинний рак;
2) капілярний (тубулопапілярний) — у 10—15%;
3) хромофобний — у 5—10%;
4) рак збірних проток (рак проток Белліні) — у 1—2%;
5) некласифікований — у 4—7%.
В останні роки до морфологічної характеристики пухлинного процесу внесено градацію злоякісності:
Gx — ступінь диференціації не може бути визначений;
G2 — помірнодиференційована пухлина;
G3 — низькодиференційована пухлина;
G4 — недиференційована пухлина.
Відповідно до морфологічної характеристики рак нирки представлений 5 основними гістологічними типами: світлоклітинний (конвекційний), папілярний (хромофільний), хромофобний нирковоклітинний рак, рак збірних проток і некласифікований нирковоклітинний рак. Ця Міжнародна гістологічна класифікація нирковоклітинних пухлин грунтується як на традиційних характеристиках — дані про гістогенез і цитоморфологічні особливості пухлини, так і нових критеріях оцінювання пухлин (цитогенетичний і молекулярно-генетичний параметри).
Міжнародна класифікація хвороб 10-го перегляду:
С 64 — злоякісне новоутворення нирки, крім ниркової миски.
С 65 — злоякісне новоутворення ниркової миски.
Міжнародну класифікацію за системою TNM застосовують тільки для нирковоклітинної карциноми. Діагноз має бути підтверджений гістологічно.
TNM — клінічна класифікація.
Т — первинна пухлина:
Тх — недостатньо даних для оцінювання первинної пухлини;
ТО — первинна пухлина не визначається;
ТІ — пухлина до 7 см у найбільшому діаметрі, у межах нирки;
Т2 — пухлина понад 7 см у найбільшому діаметрі, у межах нирки;
ТЗ — пухлина поширюється на великі вени або надниркову залозу чи навколониркові тканини, але в межах ниркової фасції (фасції Героти):
ТЗс — пухлина поширюється на надниркову залозу або навколониркові тканини, але в межах ниркової фасції;
ТЗЬ — масивне поширення пухлини на ниркову і/або порожнисту вени, нижче від діафрагми;
ТЗс — масивне поширення пухлини на порожнисту вену, вище від діафрагми;
Т4 — пухлина поширюється за межі ниркової фасції.
N — регіонарні лімфатичні вузли. Регіонарними лімфатичними вузлами для нирки є лімфатичні вузли воріт нирки, живота, приаортальні і лімфатичні вузли навколопорожнистої вени (паракавальні).
При визначенні категорії N сторону ураження не враховують.
Nx — недостатньо даних для оцінювання стану регіонарних лімфатичних вузлів;
NO — немає ознак метастатичного ураження регіонарних лімфатичних вузлів;
N1 — метастаз в одному лімфатичному вузлі;
N2 — метастази в кількох лімфатичних вузлах.
М — віддалені метастази:
Мх — недостатньо даних для визначення віддалених метастазів;
МО — немає ознак віддалених метастазів;
МІ — є віддалені метастази.
Залежно від величини і поширення пухлини, наявності метастазів у регіональні лімфатичні вузли та віддалених метастазів виділяють 4 клінічні стадії нирковоклітинного раку (табл. 25).
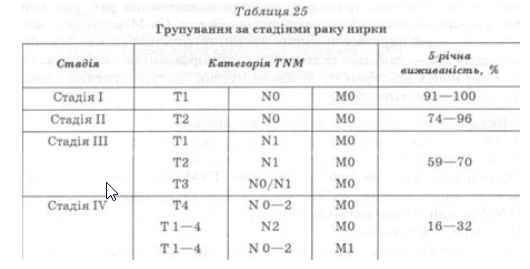
Віддалені метастази спостерігають майже в половини хворих з пухлиною нирки, насамперед в органах зі значним кровопостачанням, венозна система яких тісно пов’язана з венозною системою нирки.
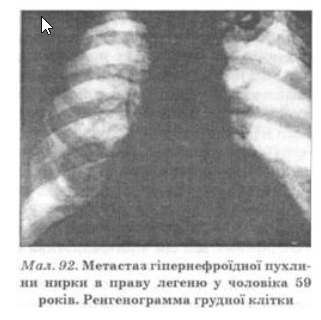
Найчастіше віддалені метастази раку нирки бувають у легенях (мал. 92), дещо рідше — кістках, печінці, мозку. Нерідко віддалені метастази з’являються через багато років після видалення первинного вогнища при нефректомії. Описані випадки самостійного зникнення метастазів у легенях після видалення ураженої пухлиною нирки.
Регіонарні лімфатичні вузли — паракавальні та парааортальні, а також ті, що розташовані в ділянці воріт нирки, — метастазуються найраніше. Тому, виконуючи радикальну нефректомію, обов’язково треба проводити ревізію регіонарних лімфатичних вузлів.
У клінічній картині пухлини нирок виділяють класичну тріаду симптомів — наявність гематурії, локальна болючість і промацування пухлини. Поряд із цим у хворих із пухлиною нирки часто виявляють і так звані нетипові, або паранеопластичні, симптоми захворювання: підвищення температури тіла, схуднення, анемію, артеріальну гіпертензію, варикозне розширення вен сім’яного канатика тощо.
В останні роки частіше спостерігають нетипову клінічну картину пухлини нирок, що зумовлено як неспецифічністю її основних ознак, так і наявністю великої кількості паранеопластичних реакцій, які можуть виявлятись одночасно з пухлиною і бути єдиними клінічними симптомами захворювання.
Гематурію виявляють у 50—65% хворих із пухлиною нирки і майже одинаково часто на всіх стадіях розвитку хвороби. Варто зауважити, що в третини хворих тотальна безболісна гематурія є першою ознакою захворювання, але в багатьох пацієнтів із пухлиною нирки І і II стадії вона може бути одноразовою, що досить часто є причиною несвоєчасного звернення хворого до лікаря. Найчастіше гематурія виникає раптово, на тлі задовільного загального стану, і швидко минає. Згустки крові можуть бути відсутні, але в деяких хворих гематурія супроводжується наявністю червоподібних згустків крові, що є зліпками просвіту сечоводу. Однак згустки крові при нирковій кровотечі можуть утворюватися і в порожнині сечового міхура, тоді вони бувають безформними. Іноді виражена гематурія у хворих із пухлиною нирки може спричинити тампонаду сечового міхура згустками крові і гостре затримання сечовипускання.
Причинами гематурії при пухлині нирки є деструкція судин у пухлинній тканині, проростання пухлини в стінку чашечки або миски, венна гіпертензія в нирці через стиснення ниркової тканини пухлиною. Але майже в половини хворих із пухлиною нирки гематурія відсутня не тільки на початкових, а й на пізніх стадіях розвитку захворювання.
При обтурації сечоводу згустками крові може порушуватися відтік сечі з нирки, при цьому виникає біль різної інтенсивності аж до ниркової кольки. Тому гематурію при пухлині нирки називають "передбольовою", на відміну від "післябольової", наприклад при сечокам’яній хворобі.
Біль у попереку може бути пов’язаний з розтягненням фіброзної капсули нирки внаслідок набряку ниркової тканини, проростання її пухлиною і натягнення ниркових судин. Інтенсивність болю варіює від незначного, відчуття деякого дискомфорту, до сильного. Найчастіше біль при пухлині нирки виражений незначно. Біль у поперековій ділянці належить до пізніх проявів захворювання і з’являється переважно в III і IV стадіях захворювання. Дуже рідко біль у ділянці нирки може бути першою ознакою хвороби. Зазвичай біль буває тупим або ниючим.
Виявлення новоутворення при пальпації — третій місцевий симптом, який визначають на пізніх стадіях захворювання. Зазвичай вдається промацати пухлину, що виходить із нижнього полюса нирки. При цьому пальпована ділянка нирки є горбистою, щільною, з чіткими контурами, частіше безболісною. У пацієнтів з надмірною масою тіла не завжди можлива пальпація навіть значно збільшеної нирки. Пальпацію слід проводити в положені хворого на спині, на боці і стоячи.
Пальпаторно пухлину визначають рідко, переважно в III і IV стадіях розвитку. Чіткіше промацуються пухлини паренхіми нирки, що виходять із нижнього її сегмента. Нирка, уражена пухлиною, тривалий час зберігає свою рухливість.
Важливим місцевим симптомом пухлини нирки в чоловіків є варикоцеле. Розширення вен сім’яного канатика при пухлині нирки може бути спричинене проростанням пухлиною лівої ниркової вени, стисненням пухлиною або метастазами регіонарних лімфатичних вузлів нижньої порожнистої вени, тромбозом нижньої порожнистої вени і перегином лівої ниркової вени через зміщення нирки ураженою пухлиною.
Поява варикоцеле в пацієнтів середнього і старшого віку є підставою для ретельного обстеження нирок. Виявлення варикоцеле у хворих з новоутвореннями нирки — несприятлива прогностична ознака, оскільки вказує на значне поширення пухлинного процесу.
Загальні симптоми раку нирки досить різноманітні. Оскільки такі симптоми не специфічні для пухлини нирки, то часто виявлення безпосередньої причини їхньої появи затягується надовго.
Найчастіший загальний симптом раку нирки — підвищення температури тіла. Гарячка, переважно субфебрильна, постійна і тривала. Підвищення температури тіла пов’язане з виділенням пухлиною токсичних речовин, які мають пірогенні властивості. Інколи гарячка супроводжується ознобом і досягає 38-39 °С.
Інші симптоми інтоксикації продуктами пухлинного метаболізму — схуднення, слабкість, зниження апетиту, погіршення сну. У хворих із пухлиною нирки досить часто виявляють анемію, розвиток якої пов’язаний не лише з гематурією, а й із гальмівним впливом на еритропоез секретованих пухлиною токсичних речовин. Артеріальна гіпертензія буває в 15—20% хворих із пухлиною нирки. Механізм розвитку артеріальної гіпертензії при пухлині нирки пояснюють ішемізацією ниркової тканини через стиснення її пухлиною, деформацією магістрального венозного стовбура при зміщенні нирки через великі розміри пухлини і знекровлюванням клубочків нирки внаслідок артеріо-венозного шунтування в тканині пухлини. Можливою причиною появи артеріальної гіпертензії може бути вплив пухлини на ренін-ангіотензин-альдостеронову систему.
Гіперкальціємію виявляють у 5—10% хворих із пухлиною нирки, але тільки в III і IV стадіях розвитку. Пухлина нирки, яка супроводжується гіпер-кальціємією, швидко прогресує.
До важливих екстраренальних ознак пухлини відносять порушення функції печінки. Печінкова дисфункція набагато випереджає за часом появу симптомів з боку самої пухлини нирки і трапляється як рання та єдина ознака хвороби в 15%, а в сукупності з іншими проявами захворювання — в 40— 50% хворих. Функціональні порушення печінки зумовлені впливом на неї пухлинної токсичної субстанції, що виходить із ураженої бластоматозним процесом нирки.
Клінічний перебіг епітеліальних пухлин ниркової миски істотно відрізняється від перебігу пухлин паренхіми нирки. Гематурія — найчастіший симптом при цій локалізації пухлини, вона буває досить інтенсивною, зі згустками і дуже рідко — безболісною. Причиною тупого болю в ділянці нирки є порушення відтоку сечі через пухлину, що міститься в мисці, а також вторинний пієлонефрит. Збільшення нирки при пухлинах ниркової миски спостерігають рідко. Зазвичай воно зумовлено розвитком гідронефрозу. У частини хворих діагностують одночасне ураження пухлиною ниркової миски і сечоводу.
Діагностика
За наявності пухлини нирки великих розмірів її можна пропальпувати через передню черевну стінку. Пухлина щільна, горбиста, найчастіше безболісна при пальпації, зазвичай вдається промацати пухлинний вузол у нижньому полюсі нирки. При перкусії над пухлиною буває тимпаніт, оскільки перед новоутворенням у заочеревинному просторі розташований кишківник. Однак якщо пухлина великих розмірів, перкуторно відзначають тупий звук.
Лабораторні дослідження мають обмежене значення в діагностиці пухлини нирки. У загальному аналізі сечі можна виявити еритроцити. Клінічний аналіз крові дає змогу виявити анемію, збільшення ШОЕ, рідше — поліцитемію. При раку нирки характерним є підвищення вмісту фібриногену і глобулінів. У хворих, які страждають на рак нирки, часто підвищується активність лужної фосфатази, а також змінюються деякі імунологічні показники: підвищується концентрація феритину, гаптоглобіну тощо. Реакція бласттрансформацїї з фітогемаглютиніном виявила, що бласттрансформаційна активність цієї популяції імунокомпетентних клітин у хворих на рак нирки різко знижена. Однак зміни лабораторних параметрів не є специфічними, їх можна спостерігати при багатьох інших захворюваннях.
Ультразвукове дослідження (УЗД) має виняткове значення в діагностиці пухлин нирки. Це пов’язано з доступністю та неінвазивністю методу. У більшості хворих з пухлиною нирки новоутворення було вперше виявлено саме за допомогою УЗД, яке проводили в рамках диспансерного спостерігання або з приводу інших захворювань. Ультразвуковою ознакою пухлини нирки є зміна контуру нирки за рахунок утворення тканинної акустичної щільності. Наявність гіпоехогенних ділянок у цьому новоутворенні свідчить про процеси пухлинного розпаду.
Рентгенологічні дослідження відіграють досить важливу роль у діагностиці пухлини нирки. При оглядовій рентгенографії нирок можна виявити зміну контуру нирки за рахунок випинання пухлинного утворення.
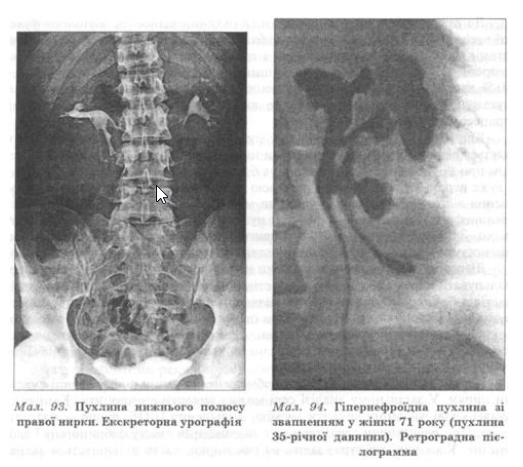
До зміни форми нирки можуть призвести лише досить великі пухлини. У 10% хворих злоякісні пухлини нирок містять вогнища кальцифікації, які також можна виявити на оглядовій рентгенограмі. Вираженість кальцифікації різна і варіює від крапкових кальцифікатів до звапнення всієї пухлинної тканини.
Екскреторна урографія пае змогу виявити характерні для пухлинного ураження нирки ознаки, а також оцінити функцію протилежної нирки. Останнє досить важливо, оскільки основним методом лікування пухлини нирки є нефректомія. У переважної більшості хворих в ураженій пухлиною нирці відзначають цілком нормальну екскрецію контрастної речовини, що забезпечує гарну видимість миски, чашечок і сечоводу (мал. 93).
Рентгенологічними симптомами пухлини нирки, які визначають на екскреторних урограмах, є дефект наповнення миски або чашечок аж до повного їх зникнення (ампутації), сегментарне розширення миски і чашечок, деформація або вкорочення чашечок з відтискуванням їх убік. Якщо пухлина розташовується медіально в нижньому полюсі нирки, вона може стискувати сечовід і зміщувати його в бік хребта.
Якщо на екскреторних урограмах не вдається чітко візуалізувати чашечково-мискову систему нирки, виконують ретроградну пієлографію. Це дослідження не варто проводити на тлі гематурії, щоб згусток крові, який є в мисці або чашечці, не став причиною дефекту наповнення і не був помилково інтерпретований як пухлина. Зазвичай ретроградну пієлографію проводять через 5—7 діб після припинення гематурії. При її виконанні особливо важливо вводити рентгеноконтрастні речовини повільно і в обсязі не більше ніж 5—6 мл. Це пов’язано з профілактикою мисково-ниркових рефлюксів і, отже, зі зменшенням імовірності метастазування.
Селективна ниркова ангіографія має велике значення в діагностиці пухлин нирки, особливо коли вони незначні. Характерні ангіографічні ознаки пухлини нирки — розширення ниркової артерії з ураженого боку, наявність ділянок підвищеної васкуляризацїї, а також зміна судинного малюнка. У пухлинному вузлі видно стоншені, вплетені, з безліччю аневризмоподібних розширень кровоносні судини (мал. 95).
Надзвичайно характерна ознака новоутворення нирки — наявність безладних, різних за величиною і формою скупчень рентгеноконтрастної речовини в пухлинній тканині — одержала незвичайну назву "симптом калюж і озер".
При недостатній інформативності стандартного ангіографічного дослідження нирок виконують фармакоангіографію. Відомо, що судини, розташовані в пухлинному вузлі і нормальній тканині, по-різному реагують на введення вазоактивних речовин.
Венокаваграфія має важливе значення в оцінюванні поширеності пухлинного процесу і виборі обсягу оперативного втручання. Виявлення дефекту наповнення в нирковій вені і нижній порожнистій вені при венокаваграфії вказує на проростання пухлини в ці судини. Дистальніше від місця тромбозу нижня порожниста вена розширена. Метастази в навколопорожнисті лімфатичні вузли можуть проявлятися дефектами наповнення внаслідок тиску нижньої порожнистої вени ззовні.
Комп’ютерна томографія є найінформативнішим і найважливішим методом діагностики пухлини нирки.
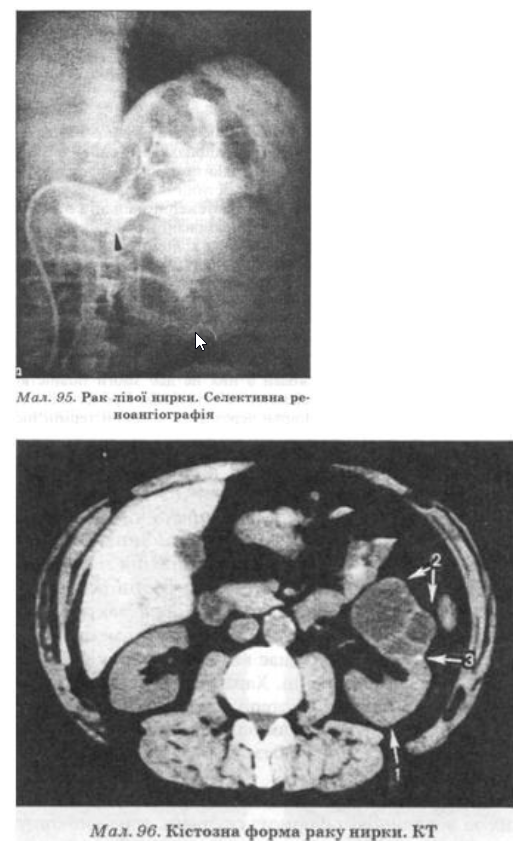
Це дослідження дає змогу не тільки виявити факт наявності новоутворення, а й оцінити його розміри, локалізацію, відношення до чашечково-мискової системи, прилеглих органів і тканин, а також наявність метастазів (мал. 96).
За допомогою комп’ютерної томографії встановлюють стадію пухлинного процесу і визначають тактику лікування хворих. Хворим, в яких виникла підозра на пухлину нирки, показане виконання комп’ютерної томографії. Більш інформативною є мультиспіральна комп’ютерна томографія і магнітно-резонансна томографія (МРТ), яка дає змогу оцінити ступінь поширення пухлини за ходом вен і визначити межі поширення пухлинного тромбу.
Радіоізотопні методи дослідження після появи комп’ютерної томографії втратили своє діагностичне значення (однак їх використовують для оцінювання функціонального стану ураженої і, що важливіше, протилежної нирки). На радіоізотопних нефросцинтиграмах можна помітити відсутність зображення частини ниркової паренхіми.
При обстеженні пацієнта з пухлиною нирки потрібно провести дослідження, спрямовані на виявлення віддалених метастазів. Метастази в легені виявляють за допомогою рентгенографії і комп’ютерної томографії легень. Кісткові метастази діагностують за допомогою рентгенографії, а також сцинтиграфїї кісток. Метастази в печінку виявляють завдяки комп’ютерній томографії та ультразвуковому дослідженню. Метастатичні ураження мозку найкраще виявляти за результатами МРТ.
Віддалені метастази найчастіше локалізуються в легенях, кістках, печінці, головному мозку. Для їх виявлення запропоновані різні методи, однак жоден з них не дає змоги повністю виключити наявність безсимптомних віддалених метастазів. Про це свідчать численні факти появи метастазів раку нирки через дуже великий термін після нефректомії. У багатьох дослідженнях на момент установлення діагнозу раку нирки у 23—40% хворих уже були віддалені метастази. З урахуванням того, що найчастіше спостерігають метастази раку нирки в легені і кістки, перед операцією слід проводити рентгенографію легень, черепа, хребта, таза, метафізів трубчастих кісток. Для виключення кісткових метастазів широко застосовують ізотопну сцинтиграфію, а для виключення метастазів у лімфатичні вузли середостіння, печінки, головний мозок, легені — комп’ютерну томографію.
Диференціальна діагностика
При пухлині нирки потрібно проводити диференціацію з простою кістою, полікістозом, гідронефрозом, нефроптозом, карбункулом нирки, піонефрозом, пухлиною заочеревинного простору та іншими захворюваннями, при яких нирка збільшується і змінює свою конфігурацію.
Диференціальний діагноз пухлини і кісти нирки найчастіше здійснюють за допомогою УЗД. При ультразвуковому дослідженні розрізняють 3 види об’ємних утворень нирки: щільні, рідинні і змішані. Для щільної пухлини характерна негомогенна структура, що зумовлює появу внутрішнього ехосигналу. Для кісти нирки характерні рівні контури, відсутність внутрішніх ехоструктур, посилення відбитих ультразвукових хвиль на дистальній межі утворення. Однак аналогічну картину можна спостерігати при абсцесі, гематомі, аденомі, ліпомі і навіть саркомі, тому не можна судити про морфологічну структуру пухлини на підставі неморфологічних методів. У разі сумнівів щодо щільного чи рідинного характеру утворення проводять пункцію його під ультразвуковим контролем із цитологічним дослідженням отриманої рідини і кістографією.
Кісту нирки можна промацати через передню черевну стінку, однак консистенція її буде еластичною.
Характерний вигляд матиме кіста нирки при комп’ютерній томографії. Однак з огляду на той факт, що пухлина може розвиватися в кісті, при виконанні різних втручань з приводу кісти нирки (пункція, вирізування) слід проводити цитологічне дослідження вмісту кісти на наявність атипових клітин.
Нирку можна пальпувати також при гідронефрозі. Однак правильний діагноз дають змогу встановити результати УЗД і екскреторної урографії.
При полікістозі нирок можна промацувати горбисті щільні нирки з обох боків. Для диференціальної діагностики полікістозу і двобічних пухлин нирки виконують УЗД, комп’ютерну томографію, а за відсутності вираженої хронічної ниркової недостатності — екскреторну урографію.
Диференціальна діагностика пухлини нирки і нефроптозу на підставі лише пальпаторних даних важка. Тому в разі виявлення під час пальпації об’ємного утворення живота або поперекової ділянки потрібно застосувати комплекс методів обстеження — ультразвукових і рентгенологічних.
Діагноз гідронефрозу встановлюють за допомогою УЗД, при якому видно стоншення ниркової паренхіми, розширення миски і чашечок, якщо немає термінальної стадії гідронефрозу. Це можна підтвердити екскреторною урографією. Труднощі диференціальної діагностики пухлини нирки і піоне- фрозу пов’язані з тим, що товщина стінки піонефротичного мішка і включення всередині нього нагадують при УЗД картину пухлини із крововиливом усередині. При цьому доводиться вдаватися до комп’ютерної томографії і комплексної ангіографії.
В 1—2% хворих виникають труднощі у визначенні органної належності утворень заочеревинного простору і черевної порожнини (при пухлинах надниркової залози, хвоста підшлункової залози, новоутвореннях І сегмента печінки, а також при збільшеній селезінці). У таких випадках найбільш інформативна селективна ниркова артеріографія.
Абсцес (карбункул) нирки при УЗД і екскреторній урографії можна розцінити як пухлину нирки. Для уточнення діагнозу нерідко виконують ниркову ангіографію і комп’ютерну томографію.
Пухлини, що виходять із заочеревинного простору або сусідніх органів, можуть проростати нирку і давати характерні для пухлини нирки рентгенологічні та ультразвукові ознаки. Правильно встановити діагноз допомагають ниркова ангіографія і комп’ютерна томографія.
Доброякісні новоутворення становлять близько 6—8% усіх пухлин нирки. Запідозрити доброякісну пухлину можна в 11 % хворих з виявленими при УЗД об’ємними утвореннями нирки. Доопераційна диференціальна діагностика раку нирки і доброякісних новоутворень можлива для жировмісних пухлин типу ангіоміоліпоми і ліпоми на підставі наявності гіперехогенного утворення і жирових включень, які добре візуалізуються при комп’ютерній томографії. На ангіограмах ці утворення гіперваскулярні.
Доброякісність новоутворення має бути підтверджена за допомогою аспіраційної біопсії.
Цей метод простий, безпечний, досить інформативний і дає змогу встановити правильний цитологічний діагноз приблизно у 80—87% випадків. Однак одержати досить матеріалу для цитологічної оцінки вдається не завжди; крім того, є імовірність неправильної інтерпретації даних через можливу деформацію клітин при виконанні аспіраційної біопсії, а також співіснування в одній пухлині клітин доброякісного і злоякісного новоутворення.
У 7—10% хворих виявити пухлину і встановити її природу важко навіть із використанням усіх сучасних методів. Це особливо стосується новоутворень діаметром менше ніж 3 см, які нерідко доводиться диференціювати із додатковою часточкою ниркової паренхіми, особливо при так званій горбатій нирці. У таких випадках використовують комп’ютерну томографію, інформативність якої збільшується за рахунок внутрішньовенного посилення, що дає змогу чіткіше диференціювати патологічну тканину.
Труднощі виникають при диференціюванні раку нирки і вузлової форми ксантогранульоматозного пієлонефриту. Подібність клінічної картини, наявність щільного утворення в нирці у більшості хворих змушує припускати рак нирки і виконувати нефректомію. Запідозрити і підтвердити експрес-біопсією ксантогранульоматозний пієлонефрит можна лише в пацієнтів, у яких щільне новоутворення в нирці при вазографії не має судин, а під час операції виявляють перифокальний інфільтративний процес, характерний для ксантогранульоми.
У лікуванні хворих на рак нирки застосовують оперативні, променеві, медикаментозні, комбіновані і симптоматичні методи лікування.
Радикальним методом лікування пухлини нирки є оперативне видалення пухлини миски. В останні роки показання до нефректомії при пухлині нирки значно розширилися. Навіть за наявності метастазів видалення основного пухлинного вогнища може продовжити життя хворого.
Показання до нефректомії у хворих із пухлиною нирки залежать від загального стану хворого, наявності і ступеня ракової інтоксикації, стадії первинної пухлини, наявності метастазів, стану і функції протилежної нирки і віку хворого. При цьому вирішальну роль відіграє стадія пухлини, що переважно визначає також вибір оперативного доступу і необхідні міри профілактики оперативних ускладнень. Рак нирки вважають радіорезистентним. Дотепер ще немає ефективних гормонів і хіміопрепаратів для лікування пухлини нирки.
При пухлині миски оперативне втручання полягає у видаленні нирки, сечоводу на всьому його протязі та резекції сечового міхура в окружності вічка сечоводу ураженої нирки. Таке розширене оперативне втручання є необхідним через можливе поширення пухлини на відділи сечових шляхів, які розташовані нижче.
Крім радикальної нефректомії в деяких хворих показане виконання органозберігальної операції — резекції нирки. Вона є загальноприйнятим методом лікування хворих з пухлиною єдиної нирки, двобічними ураженнями, а також у разі порушення функції протилежної нирки. В останні роки резекцію нирки виконують за наявності невеликих (до 4 см) пухлин.
Під час органозберігальної операції слід виконувати морфологічне дослідження тканини нирки, щоб визначити межу поширення пухлини.
Поряд із хірургічним лікуванням при пухлинах нирки можна застосувати консервативні методи, зокрема неспецифічну імунотерапію. Остання показана здебільшого при метастатичному і рецидивному раку нирки. Найбільше поширення одержало використання інтерлейкіну-2, а-інтерферону або комбінації їх. Ефективними препарати є для 15—20% хворих, у яких вони дають змогу досягти короткочасної або тривалої ремісії. Для ефективної протипухлинної терапії метастатичного нирковоклітинного раку нині розробляють і використовують також методи адаптивної клітинної імунотерапії із застосуванням автолімфоцитів, лімфокінактивованих кілерів, туморинфільтрівних лімфоцитів та специфічної імунотерапії (вакцинотерапія, моноклональні антитіла).
Для одержання протипухлинних вакцин важливо мати на увазі, що пухлино-асоційовані антигени можуть бути як зв’язані з цілими або лізованими пухлинними клітинами, так і виділені в частково або повністю очищеному вигляді. Імуногенність таких пухлино-асоційованих антигенів може бути посилена за рахунок модифікації (гаптенами, вірусами, опроміненням тощо) або шляхом трансфекції в пухлинні клітини певних генів (наприклад, генів цитокінів). Особливо перспективними є ад’юванти мікробного походження, які нині широко використовують для виготовлення протипухлинних вакцин.
Усе більше поширення одержує використання з лікувальною метою моноклональних антитіл. Механізм їхньої протипухлинної дії є досить складним і включає комплементзалежну цитотоксичність (з активізацією системи комплементу внаслідок зв’язування антитіла антигену на поверхні пухлинної клітини), антитілозалежну клітинну цитотоксичність (за рахунок зв’язування моноклонального антитіла своїм гіперваріабельним доменом з відповідним пухлино-асоційованим антигеном на поверхні пухлинної клітин, а постійним доменом — із Fc-рецептором цитотоксичного лімфоцита), а також блокаду рецепторів, ініціацію апоптозу та ін.
Певні перспективи пов’язані з досягненнями молекулярної генетики нирковоклітинного раку, які дають підстави сподіватися на швидку появу принципово нових імунопрепаратів для лікування хворих на рак нирки, зокрема інгібіторів ангіогенезу пухлини.
Основні методи генної терапії пухлин передбачають:
• посилення імуногенності пухлини;
• генетичну модифікацію клітин імунної системи для посилення їхньої протипухлинної активності;
• уведення в пухлину генів чутливості до хіміотерапевтичних препаратів;
• блокування експресії онкогенів (наприклад, за допомогою антисенсо- вих конструкцій);
• уведення в пухлинні клітини пухлино-супресорного гена, наприклад гена р53 (р53-вектори);
• захист нормальних тканин від системної токсичної дії хіміотерапії (наприклад, уведення в стовбурові клітини кісткового мозку гена множинної медикаментозної стійкості);
• підвищення стійкості до опромінення клітин нормальних тканин, прилеглих до пухлини, за рахунок гіперекспресії в них антиоксидантів (наприклад, глутатіон-синтетази або трансферази);
• створення і використання рекомбінантних генних протипухлинних вакцин.
Роль хіміотерапії в лікуванні хворих з пухлинами нирки незначна. Однак при метастатичних і рецидивних пухлинах протипухлинні хіміопрепарати можуть давати певний ефект. Ці препарати зазвичай застосовують у комбінації з імунотерапією.
Із цитотоксичних препаратів найчастіше призначають вінбластин і 5-фторурацил. Низька ефективність хіміотерапії при нирковоклітинному раку зумовлена феноменом мультимедикаментозної резистентності, пов’язаної з наявністю відповідного гена.
Гормональну терапію, зокрема препаратами прогестерону, які ще недавно широко застосовували для лікування поширених форм раку нирки, нині через низьку ефективність практично не використовують.
Променева терапія внаслідок радіорезистентності раку нирки також не одержала значного поширення. Її роль у лікуванні пухлин нирки продовжує залишатися предметом дискусій.
Медико-соціальна експертиза
Хворим із доброякісними пухлинами нирок (аденоми, фіброми, лейоміоми) протипоказана робота в несприятливих метеоумовах, у гарячих і холодних цехах, робота з отрутохімікатами, праця водія транспорту і робота в зоні йонізувального опромінення. Полегшені умови і види праці визначає J1KK.
Хворим зі злоякісними пухлинами нирок (змішані пухлини, саркоми, гіпернефроїдний рак I, II і III стадії) рекомендують полегшення умов і видів праці на підставі висновку JIK.K. У період оперативного лікування пацієнти тимчасово непрацездатні. У подальшому встановлюють II групу інвалідності з переоглядом через 12 міс. Хворі з рецидивами і метастазами — непрацездатні, потребують постійного стороннього догляду ( І група інвалідності по життєво).
При раку нирки IV стадії хворі непрацездатні, потребують постійного стороннього догляду (І група інвалідності по життєво).
Хворим із доброякісними пухлинами сечового міхура (папіломатоз, фіброми, лейоміоми), якщо їхній загальний стан порушений (інколи гематурія, дизурійних явищ або немає, або вони незначні), рекомендують полегшення умов праці на підставі висновку J1KK. При значному зниженні кваліфікації і заробітку встановлюють III групу інвалідності до раціонального працевлаштування.
У разі незадовільного загального стану (слабкість, гематурія, анемія, виражені дизурійні явища) хворі непрацездатні — встановлюють II групу інвалідності на 1—2 роки.
Прогноз при пухлинах нирок загалом сприятливий і залежить від стадії пухлини. Так, серед хворих із І стадією 5-річна виживаність становить 60—90%, із II стадією — 50—60%, із III стадією — 20—40%, а при IV стадії вона не перевищує 10%. Середня виживаність хворих з віддаленими метастазами — близько 1 року.
Нефробластома (пухлина Вільмса) становить приблизно 20—25% усіх злоякісних новоутворень у дітей. Її виявляють у дітей різного віку, однак найчастіше від 2 до 5 років. Частота виявлення (1:10 000 дітей) пухлини не залежить від статі дитини: у хлопчиків і дівчаток її діагностують з однаковою частотою. У 4—5% хворих пухлина Вільмса буває двобічною. У дорослих пухлину Вільмса теж виявляють, але дуже рідко.
Приблизно 2% нефробластом є сімейними, ще 2% — складниками спадкових синдромів. П’ятирічна виживаність становить близько 90%.
Етіологія
В останні роки досягнуті значні успіхи у вивченні причин розвитку пухлини Вільмса. Установлено, що розвиток пухлини пов’язаний з порушенням ембріогенезу нирки. Ключова роль при цьому належить генетичним порушенням. Доведено, що за виникнення пухлини Вільмса відповідальні порушення в кількох генах — WT1, WT2 і WT3.
Роль генетичних чинників у розвитку пухлини Вільмса підтверджує той факт, що вона часто поєднується з вадами розвитку інших органів і систем. Виявлено, що мутації в гені WT1 призводять до розвитку не тільки даного новоутворення, а й різних аномалій сечових і статевих органів, аніридії (уродженої відсутності райдужки), уродженої гемігіпертрофії, синдрому Беквітта—Відемана.
Типова нефробластома — трифазна пухлина, в якій поєднуються примітивна нефробластична (бластемна) тканина, епітеліальні клітини, що формують тубулярні, гломерулоподібні структури, і мезенхімальна тканина, іноді з наявністю елементів посмугованих м’язів, хряща і кістки. За різноманіттям гістологічної будови нефробластома може конкурувати з тератомами. Джерелом розвитку нефробластоми є нефрогенна тканина.
Макроскопічно нефробластома зазвичай представлена солітарним, досить однорідним вузлом м’якої консистенції. На розрізі поверхня пухлини трохи вибухає, білувато- або рожево-сірого кольору. Нефробластома, як правило, чітко відмежована псевдокапсулою від прилеглих тканин. Нерідко на розрізі видно септи і пухлина є мультилобулярною. Трапляються кістозні утворення. Крововиливи і вогнища некрозів відзначають досить часто, але вони рідко бувають вираженими. Іноді пухлина досить щільна на дотик, що можна пояснити переважанням мезенхімального компонента. Інколи спостерігають кальцифікацію пухлини, але в цілому вона не характерна для нефробластоми. Пухлинний вузол у середньому має діаметр близько 12 см. Мультицентричні і білатеральні пухлини діагностують у 7,0 і 5,4% випадків відповідно. Типовими є метастази в регіонарні лімфовузли, легені і печінку; метастази в цілому не характерні (менше ніж 1% випадків).
Мікроскопічно нефробластоми в більшості випадків є трифазними, однак нерідко трапляються біфазні або монофазні пухлини.
Бластомний варіант складається переважно з дрібних вогнищ незабарв- лених поверхневих недиференційованих клітин без утворення тубулярних структур (див. вклейку, мал. 100).
Епітеліальний варіант представлений переважно тубулярними структурами, вистеленими поверхневим епітелієм. Слід зауважити, що епітеліальні елементи місцями нагадують картину нефрогенезу і схожі то на нефрони ембріональної нирки, то на різні стадії гломерулогенезу.
Мезенхімальний, або стромальний, варіант складається переважно зі стромальних елементів у поєднанні з поверхневою нефробластичною тканиною.
У змішаних формах можна виявити ділянки лейоміосаркоми і рабдоміосаркоми, папілярні структури зі слизотвірного і плоского епітелію. У рідкісних випадках у нефробластомі спостерігають ділянки, які нагадують нейробластому (з формуванням розеток) і гангліозні клітини. Імуногістохімічне дослідження має обмежене значення для діагностики нефробластоми. Його результати віддзеркалюють диференціювання представлених компонентів та їх клітинних типів.
Розміри або маса пухлини не мають істотного значення для прогнозу хвороби. Більш значущими є вік, в якому виявлена пухлина, вираженість анаплазії і стадія. Перші дві ознаки досить тісно взаємопов’язані. Так, зони вираженої анаплазії відзначають не більше ніж у 4,5% хворих із нефроблас- томами. Вони вкрай рідко трапляються у дітей перших двох років життя, але у віці 6 років їх кількість становить 10%. Нижче представлено групування пухлини Вільмса за стадіями.
Стадія І. Пухлина обмежена ниркою. Власна капсула нирки інтактна. Ниркова пазуха може бути інфільтрована, але в межах органа.
Стадія II. Пухлина поширюється за межі нирки, але повністю операбельна. Включає випадки із проростанням ниркової капсули або ниркових судин за межі ниркової пазухи.
Стадія III. Резидуальна негематогенна пухлина в межах черевної порожнини. Включає один із перелічених нижче варіантів:
• метастази в абдомінальних лімфовузлах;
• дифузне перитонеальне обсіменіння;
• проростання пухлини макро- або мікроскопічно за межі вилученого препарату;
• залишкова пухлина в межах черевної порожнини.
Стадія IV. Гематогенні метастази.
Клінічна картина пухлини Вільмса залежить від стадії захворювання, наявності метастазів і віку пацієнта.
На ранніх стадіях захворювання клінічні прояви незначні і найчастіше проявляються слабкістю, нездужанням, схудненням, зниженням апетиту, періодичним субфебрилітетом, помірною анемією, збільшенням ШОЕ.
На пізніх стадіях пухлини Вільмса найспецифічнішою ознакою є об’ємне утворення в животі, що пальпується. Іноді його виявляє мати або лікар під час профілактичного огляду дитини, що не пред’являє ніяких скарг і добре почувається. При пальпації пухлина частіше щільна і гладенька, рідше — горбиста. Вона може фіксуватися до прилеглих структур і не зміщуватися при пальпації.
Біль не характерний, але іноді буває у дітей з великою пухлиною Вільмса, що тисне на прилеглі органи або проростає діафрагму, печінку або заочеревинну клітковину.
Гематурію при пухлині Вільмса спостерігають приблизно в 10—12% хворих, артеріальну гіпертензію виявляють досить часто.
Здавлення і проростання нижньої порожнистої вени призводить до асциту і набряку нижніх кінцівок. Компресія ниркової вени супроводжується виникненням колатерального кровотоку і появою симптоматичного варикоцеле.
Уже на ранніх стадіях розвитку пухлина Вільмса схильна до метастазування, що залежить не стільки від величини пухлини, скільки від характеру її росту. Метастазування відбувається гематогенним і лімфогенним шляхами. Спочатку зазвичай ушкоджуються заочеревинні лімфатичні вузли. Метастази спричинюють біль у попереку, що іррадіює в пах, статеві органи. Метастази можуть також виникати в легенях, печінці, протилежній нирці, яєчку, кістках, головному мозку та інших органах.
Діагностика. Якщо лікар запідозрив пухлину Вільмса, потрібно провести комплексне обстеження дитини, що включає рентгенологічне, радіоізотопне, ультразвукове та інші дослідження.
Під час огляду дитини звертають увагу на посилення малюнка підшкірних вен, асиметрію живота і сколіоз. Підставу запідозрити пухлину нирки дає наявність варикоцеле в ранньому віці. Пальпацію живота проводять у вертикальному положенні дитини і в горизонтальному — на спині і боці. Інколи для визначення пухлини доводиться робити пальпацію живота під наркозом.
При дослідженні сечі нерідко виявляють протеїнурію і лейкоцитурію. Остання наростає в разі приєднання вторинної інфекції. У 20% дітей з пухлиною Вільмса відзначають високу ШОЕ.
У діагностиці пухлини найважливішими є рентгенологічні методи дослідження. На оглядовому знімку помітне щільне утворення, що зміщує петлі кишок, іноді з ділянками звапнення. Тінь поперекового м’яза на боці ураження нечітка або не визначається. На знімку в бічній проекції пухлина розташовується позаду від наповненої газом товстої кишки (при пухлинах органів черевної порожнини ця кишка зазвичай відтискується дозаду).
Екскреторна урографія — досить специфічний метод виявлення пухлини Вільмса, однак він недостатньо інформативний при диференціальній діагностиці об’ємних утворень, які виходять із нирки, і позаниркових, наприклад нейробластоми надниркових залоз, а також при невеликій пухлині Вільмса.
Пухлину нирки найкраще можна виявити в разі поєднання екскреторної урографії з пневморетроперитонеумом і томографією. При збереженій функції нирки спостерігають деформацію чашечково-мискової системи пухлиною, що має на томограмах неоднорідну контрастність.
Ультразвукове дослідження нирки дає змогу виявити об’ємне утворення в нирці, провести диференціальну діагностику з кістозними утвореннями. Його використовують для скринінгового обстеження дітей з групи ризику розвитку пухлини Вільмса.
Комп’ютерна томографія черевної порожнини і заочеревинного простору є одним із найточніших методів виявлення пухлини, оцінювання стану регіонарних лімфатичних вузлів і прилеглих органів і тканин.
Ниркову артеріографію використовують, якщо не можна підтвердити наявність пухлини іншими методами, для диференціальної діагностики ниркових і позаниркових утворень, точного визначення розмірів пухлини та проростання її у прилеглі тканини.
Рентгенограми грудної клітки і черепа виконують для виявлення метастазів відповідно в легенях і в кістках черепа. Венокаваграфію використовують для виявлення проростання пухлини в нижню порожнисту вену і визначення положення цієї вени щодо пухлини.
Радіоізотопне сканування скелета застосовують для виявлення метастазів пухлини в кістках.
Диференціальну діагностику потрібно проводити з простою кістою нирки, гідронефрозом, полікістозом, тромбозом ниркової вени. Найбільші труднощі в доопераційний період виникають під час проведення диференціальної діагностики пухлини Вільмса та інших новоутворень нирки, таких як доброякісні фетальна мезодермальна гамартрома, ангіоміолінома і злоякісна аденокарцинома.
Гідронефроз при екскреторній урографії проявляється відсутністю або запізнюванням контрастування різко розширеної чашечково-мискової системи нирки на відміну від пухлини, при якій миска здавлена, чашечки деформовані і розсунуті.
Диференціально-діагностичні труднощі виникають і при полікістозі нирок. Двобічне ураження, характерна павукоподібна картина чашечково-мискової системи на екскреторних урограмах, наявність множинних ділянок зі збідненою васкуляризацією при нирковій ангіографії підтверджують діагноз полікістозу нирок.
Для карбункулу нирки, рентгенологічні ознаки якого може стимулювати пухлина, характерними симптомами є гострий розвиток захворювання, гіперемія, різка болючість і напруження м’язів на боці ураження, відсутність функції нирки.
Лікування. Вибір тактики лікування пухлини Вільмса ґрунтується на оцінюванні стадії захворювання, особливостей гістологічної будови пухлини, молекулярних маркерів і віку дитини. Основним принципом лікування таких хворих є застосування комплексного лікування: хірургічного, хіміо- і радіотерапії.
Хірургічне лікування залишається основним методом лікування хворих із пухлиною Вільмса. При однобічній пухлині операцією вибору є транс перитонеальна нефректомія, при двобічній — двобічна резекція нирки в межах здорових тканин під контролем гістологічного дослідження. Наявність віддалених метастазів не є протипоказанням до видалення первинного вогнища.
У деяких хворих, якщо виконання нефректомії пов’язане із серйозними технічними труднощами через проростання пухлини, проводять передопераційну терапію — хіміо-, радіо- або їх комбінації.
Радіотерапію використовують як доповнення до хірургічного методу лікування. Пухлина Вільмса є відносно радіочутливою. Радіотерапію можна використовувати як у перед-, так і в післяопераційний період.
Променеве лікування при пухлині Вільмса застосовують у різних модифікаціях: 1) у післяопераційний період; 2) у перед- і післяопераційний період; 3) як самостійний метод лікування в разі неможливості радикального оперативного втручання. В останні роки променеву терапію успішно поєднують із уведенням протипухлинних антибіотиків (актиноміцин, хризомалін, бруне- оміцин), які крім специфічної дії мають потенціювальний вплив на ефект опромінення. Для променевої терапії застосовують рентгенівські випромінювання (200—250 КеВ), гаммавипромінювання 137С (0,6 МеВ), гаммавипромі- нювання 60Со (1,2 МеВ), гальмове випромінювання (2—45 МеВ) і швидкі електрони (до 30—40 МеВ). Якщо потрібно опромінювати більші обсяги тканин (первинне вогнище в ділянці регіонарного метастазування), варто віддати перевагу застосуванню джерел високих енергій. Зазвичай сумарна середня доза, необхідна для одержання стійкого терапевтичного ефекту при пухлині Вільмса, становить 2000—4000 рад. Щоденна вогнищева доза становить 150— 200 рад. Кількість шкірних полів визначають залежно від використовуваної енергії випромінювання — що вища енергія, то менше полів: при гальмовому випромінюванні — 1—2 поля, при гаммавипромінюванні — 3—4 поля, при рентгенівському випромінюванні — 5—6 полів. Поля випромінювання переважно розташовують на боці ураження (попереду, позаду, збоку від пухлини); іноді додатково проводять опромінення протилежного поля. У цих випадках потрібно враховувати небезпеку променевого ураження здорової нирки.
Хіміотерапія є важливим компонентом комбінованого лікування хворих з пухлиною Вільмса, її використовують на всіх стадіях хвороби.
Перевагу віддають поліхіміотерапії — одночасно декількома цитостатиками. Найбільше поширення одержала поліхіміотерапія вінкристином і циклофосфаном або цими препаратами в поєднанні з олівоміцином. При цьому використовують ті ж дози, що й при роздільному застосуванні препарату (табл. 26).

Кращі результати дає комбінована терапія. Якщо пухлина не проростає капсулу нирки і метастази не виявлені, показана нефректомія з курсом профілактичної хіміотерапії. При малорухомій пухлині без віддалених метастазів проводять передопераційне опромінення, а потім — нефректомію, у післяопераційний період — опромінення і курс профілактичної хіміотерапії. При легеневих метастазах негайно після нефректомії призначають хіміотерапію з опроміненням легень. Операція на легені (пульмонектомія) з наступною хіміотерапією доцільна при метастазах, виявлених у віддалений термін після нефректомії.
Основні труднощі під час проведення хіміотерапії пов’язані з дотриманням балансу між досягненням високої ефективності лікування і його переносимістю дитиною, переважно раннього віку, або немовлям. Дози хіміопрепаратів дітям віком до 12 міс. зменшують на 50% порівняно зі звичайними дозами через ризик розвитку тяжких побічних ефектів. Ще одним зі способів запобігти небажаним побічним ефектам хіміотерапії є використання пульс-терапії, тобто короткочасне введення великих доз хіміопрепаратів. Для зменшення токсичного ефекту не рекомендують проводити хіміотерапію одночасно з радіотерапією.
Прогноз залежить від ступеня злоякісності пухлини і термінів її розпізнання, відзначають також залежність прогнозу від віку хворого. Серед дітей старшого віку частота 5-річної виживаності після операції коливається в межах 30—50%, а у дітей віком від 1 року вона досягає 80—90%. Прогноз може бути добрим у дитини, яка після операції прожила 2 роки.
Подальша інформація
Завжди консультуйтеся зі своїм лікарем, щоб переконатися, що інформація, яка відображається на цій сторінці, може бути застосована до ваших особистих обставин. Інформація призначена тільки для медичних фахівців.