Хвороби оперованого шлунка
Класифікація хвороб
Операції резекції шлунка та різні варіанти ваготомії дуже поширені. У більшості випадків після цих операцій не виникає помітних порушень функцій органів травлення, але у частини хворих з’являються функціональні та органічні розлади як у системі травлення, так і в інших системах організму. Частота цих розладів неоднакова не лише в різних країнах, айв окремих лікувальних закладах. Практично майже повна відмова від операцій гастро- ентеростомії, вдосконалення методики та широке впровадження у практику більш фізіологічних операцій селективної ваготомії дали змогу в останні роки зменшити кількість ускладнень, пов’язаних з цими втручаннями.
Під терміном "хвороби оперованого шлунка" мають на увазі захворювання, що розвиваються унаслідок проведених на шлунку операцій, тобто з’являються нові хвороби і причиною їх розвитку служать хірургічні втручання, спрямовані на ліквідацію хвороби, що була до операції (виразкової хвороби, доброякісної або злоякісної пухлини). Слід диференціювати хвороби оперованого шлунка і післяопераційні ускладнення.
Запропоновано багато класифікацій зазначених розладів, але для застосування в клінічній практиці найбільш прийнятною є класифікація хвороб оперованого шлунка, що наведена нижче.
Класифікація хвороб оперованого шлунка
Пострезекційні розлади
Функціональні розлади:
• демпінг-синдром;
• гіперглікемічний синдром;
• гіпоглікемічний синдром;
• пострезекційна (агастральна) астенія;
• функціональний синдром привідної петлі;
• гастроезофагальний рефлюкс;
• лужний рефлюкс-гастрит;
• харчова алергія;
• невротичні стани. Органічні ураження:
• пептична виразка анастомозу;
• хронічний анастомозит;
• шлунково-ободовокишкова нориця;
• механічний синдром привідної петлі;
• рубцева деформація і звуження анастомозу;
• пострезекційні супутні захворювання (панкреатит, гепатит, ентерит, холецистит, рефлюкс-езофагіт та ін.);
• постастрорезекційна анемія;
• технічні помилки первинної операції. Змішані ураження:
• поєднання органічних і функціональних розладів. Постваготомічні розлади
Функціональні розлади:
• демпінг-синдром;
• гіпоглікемічний синдром;
• функціональна діарея;
• порушення функції кардіальної частини шлунка;
• гастроезофагальний рефлюкс;
• рефлюкс-гастрит;
• гастростаз.
• дуоденостаз;
• синдроми недостатності травлення і всмоктування;
• імпотенція;
• поєднання кількох розладів. Органічні ураження:
• рецидив пептичної виразки;
• органічний демпінг-синдром;
• органічні порушення функції кардіального сфінктера;
• рубцева деформація і звуження в зоні анастомозу або пластики;
• технічні помилки первинної операції;
• жовчнокам’яна хвороба;
• постфундаплікаційний синдром;
• хронічний панкреатит;
• рак шлунка.
За термінами виникнення
• ранні (до 1 міс після операції);
• найближчі (1—6 міс після операції);
• пізні (понад 6 міс після операції).
Клінічні прояви
Клінічні прояви і терапевтична тактика при окремих пострезекційних та постваготомічних розладах
Із функціональних ускладнень резекції шлунка найчастіше спостерігають демпінг-синдром. У це поняття інколи включають також гіпо- та гіпер-глікемічний синдроми, постгастрорезекційну астенію. Однак, на думку більшості клініцистів, таке широке трактування терміна "демпінг-синдром" невиправдане.
Демпінг-синдром (синонім — єюнальний гіперосмолярний синдром) виникає після споживання легкозасвоюваної їжі (вуглеводів) і проявляється комплексом нейровегетативних, вазомоторних і кишкових розладів. Для хворих із цим синдромом характерні блідість або гіперемія обличчя, загальна слабкість організму, пітливість, запаморочення, іноді блювання та проноси, які виникають через 10—15 хв після іди, диспепсичні явища, серцебиття, артеріальна гіпотензія, зміни на електрокардіограмі (зниження зубця Т, розширення комплексу QRS).
Механізм виникнення проносів, найімовірніше, є таким: спожита їжа дуже швидко переходить з кукси шлунка в тонку кишку. Унаслідок цього в останній утворюється високий осмотичний тиск, а відтак у просвіт порожньої кишки переходить значна частина рідини з кров’яного русла. Ця рідина та спожита їжа розтягують кишку, внаслідок чого рефлекторно посилюється кишкова моторика і виникають вазомоторні порушення аж до зменшення кровопостачання головного мозку.
У патогенезі демпінг-синдрому мають значення:
• дегрануляція ентерохромафінних клітин (ЕС1), що є важливим складником APUD-системи кишок, із звільненням мотиліну, що стимулює перистальтику, а також підвищенням секреції серотоніну і гістаміну; ентерохромафінних клітин особливо багато в початковому відділі (40 см) порожньої кишки, де наявний градієнт їхньої активності;
• при введенні глюкози (та інших легкозасвоюваних речовин) кишкові ворсинки розширюються, деформуються, на них утворюються тріщини й укорочення;
• ці зміни і гіперосмія ентероцитів — джерело патологічної імпульсації в ЦНС зі збудженням вегетативних центрів четвертого шлуночка і подальшою еферентною імпульсацією на "периферію";
• зміна функції надниркових залоз веде до викиду адреналіну, норадреналіну; підвищення рівня серотоніну, кінінів, субстанції Р (вазоактивного пептиду); порушення травної функції печінки, підшлункової залози, кишок;
• гіперглікемія призводить до подальшого зниження рівня глюкози і глюкозурії за рахунок підвищеного викиду інсуліну;
• виникають функціональна мезентеріальна гіперемія (унаслідок підвищення виділення холецистокініну, секретину, панкреозиміну) і перерозподіл крові з розвитком гіповолемії.
Частота розвитку демпінг-синдрому значною мірою залежить від розмірів шлунково-кишкового анастомозу і становить від 10 до 20% від загального числа прооперованих.
Клінічна картина:
• слабкість, що виникає під час і після їди;
• відчуття жару, гіпергідратація, сонливість, шум у вухах, тремтіння кінцівок (при цьому хворі вимушені лягти);
• напади супроводжуються тахікардією, задишкою, головним болем, поліурією, парестезіями;
• іноді виникають нудота, печія і відрижка (блювання не властиве);
• напад супроводжується бурчанням у животі і проносом наприкінці нападу;
• розвиток нападу провокує молочна, вуглеводна їжа;
• після нападу — розбитість, слабкість, зниження працездатності, дратівливість, апатія, зниження лібідо.
За перебігом демпінг-синдром ділиться на три ступені тяжкості (табл. 37).
Таблиця 37
Ступені тяжкості демпінг-синдрому
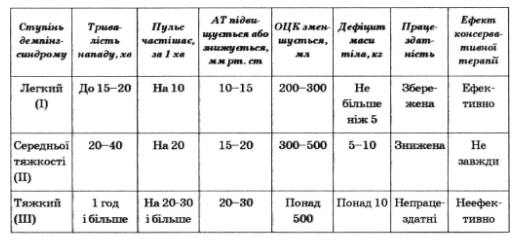
Лікування
Консервативне лікування застосовують при легкому і середньому ступені тяжкості, при тяжкому — хворого готують до операції.
Рекомендується дотримання дієтичного режиму із загальною енергетичною цінністю близько 3000 ккал, який передбачає споживання їжі, багатої на білки, вітаміни, мінеральні солі, з нормальним вмістом жирів: виключають легкозасвоювані вуглеводи (з вуглеводів призначають сорбіт по 3—5 г на день), їжу слід споживати невеликими порціями, часто (5—6 разів на добу), лежачи на лівому боці. Перед їдою деяким хворим уводять атропін, апрофен, пла- тифілін або застосовують дію електростимуляторів.
Медикаментозне лікування включає:
— седативну терапію (валеріана, транквілізатори, іноді — нейролептики);
— замісну терапію (хлоридна кислота з пепсином, шлунковий сік, у разі проносу — кальцію карбонат або біла глина);
— антагоністи серотоніну — дезерил (зменшує інтенсивність падіння об’єму циркулюючої плазми), резерпін і немелін;
— інсулін (5—8 ОД за 15 хв до їди внутрішньом’язово) або букарбан (по 0,5 г всередину); інгібітор моноаміноксидази — преніламін;
— гормони анаболізму (ретаболіл, неробол, метіан-дростенолон);
— гемотрансфузії, плазмотрансфузії вітамінів В, С і А, рутину, у разі порушення електролітного балансу — поліелектролітні суміші, калій і залізо.
Багато клініцистів вважають гіперглікемічний синдром варіантом єюнального гіперосмотичного синдрому. Він розвивається у хворих, які перенесли резекцію шлунка, після споживання їжі зі значним вмістом легкозасвоюваних вуглеводів.
Унаслідок швидкого переходу цих вуглеводів у тонку кишку, всмоктування їх, зокрема глюкози, значно прискорюється. Це призводить до виникнення гіперглікемії,. Характерні ознаки з’являються через 10—20 хв після споживання їжі: виділення гарячого поту, великої кількості густої слини, серцебиття, нудота, відчуття жару, різка слабкість, запаморочення, почервоніння обличчя, підвищення артеріального тиску, відрижка, бурчання у животі, пронос.
Хворим із гіперглікемічним синдромом слід рекомендувати вживати їжу часто, малими порціями, значно обмеживши кількість вуглеводів у харчовому раціоні (передусім легкозасвоюваних). Зокрема, цукор можна замінити на сорбіт або ксиліт. У зв’язку з підвищеною збудливістю цієї категорії хворих їм призначають седативні засоби (бром, валеріана, собача кропива, рідкий екстракт пасифлори тощо) і транквілізатори.
Гіперглікемічний синдром, який дуже швидко виникає після споживання їжі, багатої на вуглеводи, через 2—4 год може змінитися на гіпоглікемічний, але ступінь прояву кожного з них може бути різним.
Гіпоглікемічний синдром розвивається за типом ваготонічного кризу. При цьому гіперглікемія, спричинена швидким всмоктуванням вуглеводів, призводить до компенсаторного надходження у кров інсуліну, який знижує рівень глюкози у крові. Що швидше падає цей рівень, то значнішими будуть прояви гіпоглікемічного синдрому, тоді як абсолютні величини рівня гіпоглікемії мають менше значення.
Ступені тяжкості гіпоглікемічного синдрому.
І ступінь — симптоми з’являються через 2—2,5 години 2—3 рази на тиждень, хворі можуть їх не помічати;
II ступінь — симптоми з’являються 2—3 рази на тиждень, хворі знають їх і прагнуть харчуватися частіше. Нерідко гіпоглікемічний синдром поєднується з іншими тяжкими синдромами;
III ступінь — ознаки хвороби виявляються щодня. Через напад, що змушує припинити роботу і лягти, хворі змушені харчуватися дуже часто, постійно носити із собою цукор і хліб.
Гіпоглікемічному синдрому притаманні такі ознаки: тремтіння, холодний піт, слабкість, запаморочення, "вовчий" голод, біль у надчеревній ділянці, блідість, артеріальна гіпотензія, брадикардія, біль за грудниною, шум у вухах. При тяжких формах цього синдрому можуть спостерігатися збудження, потьмарення свідомості, дезорієнтація або, навпаки, сонливість і навіть непритомність, судоми. Хворі з легкими формами цього синдрому можуть бути збудженими, у них з’являються відчуття голоду, слабкість, артеріальна гіпотензія, тахікардія. Іноді гіпоглікемічний синдром може розвинутися не після споживання "їжі, а в разі великої перерви між їдою або внаслідок значного фізичного навантаження. При цьому варіанті полегшення виникає після іди. Для гіпоглікемічного синдрому, на відміну від гіперглікемічного, характерне переважання парасимпатичної іннервації.
Щоб обірвати гіпоглікемічний криз, слід рекомендувати їжу, яка містить багато вуглеводів, що легко всмоктуються, але при цьому варто стежити, щоб гіпоглікемічний синдром не змінився гіперглікемічним. З метою запобігання розвитку гіпоглікемії хворим зі схильністю до її виникнення рекомендують їсти часто (до 6 разів на добу), малими порціями, уникаючи споживання легкозасвоюваних вуглеводів. Кількість вуглеводів у харчовому раціоні треба збільшувати поступово і дуже обережно —до 250—300 г на добу. Кількість цукру, яку можна вживати такому хворому, встановлюють індивідуально. Виключають солодкі страви, вироби із здобного тіста. Рекомендують м’ясо, овочі, фрукти, які не містять глюкози, молочні продукти. Показані також фізіотерапевтичні процедури, які діють седативно (теплі ванни, електрофорез брому та кальцію за Вермелем або Щербаком, електросон), а також голковколювання. Із лікарських засобів показані вегетативні гармонізатори, седативні препарати, транквілізатори.
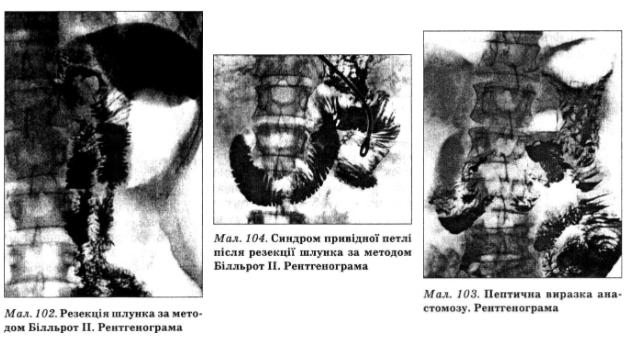
У походженні пострезекці йного рефлюкс-гастриту відіграє роль закидання кишкового вмісту з жовчю в шлунок. Жовч впливає на слизову оболонку шлунка, цьому сприяє також припинення продукування гастрину після видалення дистальної частини шлунка. Пострезекційний рефлюкс-гастрит найчастіше розвивається після операції резекції шлунка за Білльрот II (мал. 102).
Клінічно рефлюкс-гастрит виявляється тупим болем у надчеревній ділянці, відчуттям гіркоти і сухості в роті, відрижкою, зниженням апетиту. При фібро- гастродуоденоскопії виявляють картину атрофії слизової оболонки кукси шлунка з ознаками запалення.
Рефлюкс-езофагіт виникає внаслідок недостатньої замикальної функції кардії. Як правило, його супроводжує рефлюкс-гастрит. Кишковий вміст із домішкою жовчі закидається в стравохід, виникає лужний рефлюкс-езофагіт.
Він виявляється відчуттям болю або печії за грудниною. Зазначені ознаки з’являються зазвичай після іди, але можуть бути і не зв’язані зі споживанням їжі. Часто турбують сухість і гіркота в роті, відчуття "застрявання" їжі в горлі, відчуття "грудки". Діагноз рефлюкс-езофагіту підтверджується при езофагоскопії. У деяких випадках ре- флюкс-езофагіт може ускладнюватися сте- нозуванням стравоходу.
Агастральна астенія виникає внаслідок порушення травної функції шлунка, підшлункової залози, печінки і тонкої кишки.
Патогенез. Після резекції шлунка його кукса втрачає свою функцію, прогресує атрофія слизової оболонки, випадає трофічна роль гастрину та інших гормонів травного тракту. Відсутність у соку хлоридної кислоти призводить до дисбактеріозу, розвитку проксимальної мікробної контамінації травного тракту (мікрофлора, у тому числі і патогенна, дистальних відділів заселяє проксимальні), холециститу, дуоденіту, призводить до зниження дезінтоксикаційної функції печінки, розвитку гепатиту. їжа надходить у кишки ферментативно необробленою. У дванадцятипалій кишці в недостатній кількості виробляються секретин і хо- лецистокінін, внаслідок чого порушується функціональна активність печінки і підшлункової залози. У тонкій кишці прогресує хронічний ентерит (з розвитком набряку строми ворсинок, інфільтрацією лімфо’ідної тканини, десквамацією епітелію слизовою оболонкою), порушуючи функції ентеро- цитів, секреції і всмоктування різних речовин (мальабсорбції). Усе це призводить до порушення обміну білків, жирів, вуглеводів, мікроелементів і вітамінів. Через прогресування білкових порушень хворий втрачає масу тіла. Виникає дефіцит вітамінів групи В і D, рибофлавіну, нікотинової кислоти. Порушення обміну вітаміну D, кальцію і фтору призводить до розвитку ос- теопорозу й артропатій. Виникає гіпохромна анемія (залізо- і білководефі- цитна). У скелетних і непосмугованих м’язах прогресують процеси атрофії, дистрофії і порушення іннервації.
Клінічна картина. Хворі пред’являють скарги на слабкість, набряки, прогресивну кахексію, проноси, наявність шкірних змін і ендокринних порушень. Можуть виникати: асцит, анасарка, олігурія і анурія. Мають місце анорексія, яка змінюється булемією, глосит, фарингіт, езофагіт, хейлоз. На шкірі з’являється висипка (симетрична пурпура), пігментація, телеангіоектазії. Може розвинутися ендокринопатія з жіночим типом оволосіння, ламкістю волосся, імпотенція. Часом відзначають зміни психіки. Формується вторинна імунопатія з розвитком різноманітних інфекційних процесів, зокрема туберкульозу.
Ступені тяжкості агастральної астенії: 1) легка (незначні прояви); 2) помірної тяжкості (проноси, набряки, втрата білка, жирів, анемія); 3) тяжка (кахексія, авітаміноз, остеопороз).
Консервативне лікування включає дієтотерапію, переливання крові, плазми, білків, жирів, вуглеводів, вітамінів, електролітів. Призначають анаболічні стероїди — анабол, неробол, ретаболіл, феноболіл, метиландростенолон. їду поєднують з уживанням розчину хлоридної кислоти, пепсину і ферментів.
При тяжкій астенії проводять оперативне втручання, в основі якого лежить включення в пасаж дванадцятипалої кишки, збільшення ємності шлунка, уповільнення його спорожнення.
Після резекції шлунка у 12% хворих досить часто розвивається синдром харчової алергії, який в 20—30% випадків носить аліментарно-алергійний характер. Алергенами виступають яйця, молоко, риба, полуниці, томати, какао, шоколад та інші продукти.
Патогенез. Порушення ферментації їжі, що розвиваються після резекції шлунка, призводять до утворення великої кількості нерозщеплених білків, які діють як алергени (антигени), стимулюючи синтез антитіл. Цьому процесу сприяє зниження активності протеолітичних ферментів, прискорення евакуації вмісту шлунка, ушкодження епітелію тонкої кишки, запалення слизової оболонки травного тракту, утворення вазоактивних речовин (гістаміну, серотоніну тощо).
Через швидке надходження їжі (особливо білкової) з кукси шлунка, де вона не встигла достатньо перетравитися, у тонку кишку, у ній високомоле- кулярні білкові комплекси, які мають антигенні властивості, всмоктуються і сенсибілізують організм. Усмоктуванню цих комплексів сприяють речовини, що підвищують проникність стінки кишок (передусім алкоголь та прянощі). При харчовій алергії на перший план виступає клінічна картина гострого алергійного гастриту або гастроентериту.
Клінічна картина. Після іди виникають пронос, біль у животі, нудота. Можливі шкірні дерматози.
Діагностика базується на проведенні проб з харчовим навантаженням підозрюваним алергеном (молочним тестом) з оцінюванням:
• лейкопенічного індексу Вогена — зменшення числа лейкоцитів крові на 1000 і більше;
• проби Кока — зростання частоти серцевих скорочень на 12—15 за 1 хв і більше;
• індексу Стокса — збільшення числа тромбоцитів на 15% і більше;
• гемодинамічної проби — збільшення артеріального тиску на 15 мм рт. ст.;
• гістамінопектичного індексу крові.
Лікування полягає у виключенні з харчового раціону продуктів, які спричинюють або можуть спричинити алергійні реакції, а також у призначенні відповідних антиалергійних препаратів (кальцію хлориду або глюконату, димедролу, супрастину, кортикостероїдів). У деяких хворих проводять специфічну десенсибілізацію зростаючими дозами непереносимого продукту.
У хворих, які перенесли резекцію шлунка, ще частіше, ніж при виразковій хворобі, спостерігають невротичний стан, переважно астенічний, іпохондричний, тривожно-депресивний синдроми. Найяскравіше невротичний стан проявляється після іди, хоча загалом астенічний синдром і вегетативні розлади досить постійні.
Серед хвороб оперованого шлунка значне місце посідають органічні пост- резекційні розлади. Так, досить часто (до 5—10%) спостерігають пептичну виразку анастомозу. Виникненню її сприяють також наявність гіперсекреції та гіперхлоргідрії, підвищення тонусу блукаючого нерва, порушення евакуа- торної функції шлунка, дистопія слизової оболонки антрального відділу. Як рецидивна виразка кукси, так і пептична виразка анастомозу можуть виникнути і через декілька місяців після операції, і через багато років. Якщо клінічна картина виразкової хвороби зберігається відразу після операції абсолютно незмінною, то ймовірною є наявність нерозпізнаної під час операції виразки.
Пептичну виразку анастомозу (мал. 103) частіше діагностують у чоловіків. Біль при ній дуже інтенсивний, локалізується в пупковій ділянці. Він виникає не тільки після їди, а й вночі, іррадіює у ліве підребер’я, ліву лопатку. Крім болю спостерігаються блювання (іноді криваве), мелена, печія за грудниною, яка є проявом рефлюкс-езофагіту. Під час пальпації відзначають болючість у пупковій ділянці. Можуть бути пронос або закреп, схуднення. При виникненні ускладнень пептичної виразки анастомозу з’являються ознаки гастродуоденальної кровотечі (близько 2/3 хворих), перитоніту (перфорація, 6—9% хворих), шлунково-ободової нориці.
Діагностика передбачає виконання рН-метрії (з проведенням тестів Кея, Холландера, атропінової проби); визначення в крові пепсиногену-І. Уточненню діагнозу допомагають проведення фіброгастродуоденоскопії і рентгенологічного дослідження шлунка. Для уточнення діагнозу синдрому Цоллінгера—Еллісона показано сканування кукси шлунка і дванадцятипалої кишки радіоізотопом "Тс, проведення дослідження за допомогою ядерно- магнітного резонансу, комп’ютерної томографії і визначення рівня гастрину в крові.
Вирішальне значення для розпізнавання пептичної виразки анастомозу має езофагогастроскопія, що виявляє виразковий дефект у ділянці анастомозу і часто катаральний або ерозивний рефлюкс-езофагіт.
Клінічний перебіг цієї виразки тяжкий. Вона швидко стає кальозною, може пенетрувати в прилеглі органи (брижу, підшлункову залозу, поперечну ободову кишку) з утворенням нориці між шлунком, порожньою та поперечною ободовою кишками. Для останньої характерні блювання каловими масами, профузний пронос, зменшення маси тіла, анемізація, дегідратація. Діагноз підтверджується рентгенологічним дослідженням.
Консервативне лікування пептичних виразок анастомозу малоефективне. Основним методом лікування є операція, обсяг якої залежить від характеру попереднього втручання і виразкового дефекту, виявленого під час перед- та інтраопераційного обстеження.
При синдромі Цоллінгера-Еллісона показана резекція підшлункової залози з гормонопродукувальною пухлиною, при іншій локалізації — її видалення. Якщо гормонально-активну пухлину не знайдено, то в деяких випадках показана гастректомія.
Рецидиви виразки в куксі шлунка спостерігають рідко (частіше після операції за методом Білльрот II в модифікації Фінстерера та Поліа— Рейхеля, рідше — після операції за методом Білльрот І). Як правило, вони виникають у хворих на виразкову хворобу дуоденальної локалізації, в яких унаслідок недостатньої за обягом резекції шлунка зберігається висока кислотність шлункового вмісту.
Синдром привідної петлі анастомозу (мал. 104). До складу привідної петлі входять дванадцятипала кишка і початковий відділ порожньої кишки — від підвішувальної зв’язки дванадцятипалої кишки (зв’язки Трейтця) до гастро- ентеростомозу. Частота цього синдрому, за даними різних авторів, коливається в дуже широких межах (від 3 до 40%). Синдром привідної петлі часто може розвиватися в ранній післяопераційний період, протягом першого місяця, і тоді він найчастіше зумовлений механічними причинами (перегин, зрощення, інтермітивна інвагінація привідної петлі в куксу шлунка чи у відвідну петлю, атонія дванадцятипалої кишки).
Клінічна картина гострої непрохідності привідної петлі: біль у надчеревній ділянці, правому підребер’ї, нудота, блювання. Наростає інтоксикація, запальний синдром. При пальпації живота в надчерев’ї та правому підребер’ї визначають болючість, виявляється напруження м’язів черевної стінки. При некрозі дванадцятипалої кишки та її перфорації виникає клініка поширеного перитоніту. При залученні до процесу жовчного міхура і підшлункової залози виникає оперізувальний біль, з’являються ознаки жовтяниці і холангіту. На оглядовій рентгенограмі черевної порожнини виявляють затемнення, пневматоз кишкової петлі; відзначають тривале затримання контрасту при виконанні холеграфії. Лікування — термінова операція (летальність досягає 25%).
Крім гострого може спостерігатися хронічний синдром привідної петлі, який зазвичай розвивається в більш пізній термін після операції (через один рік і пізніше). Виділяють механічний і функціональний різновиди цього синдрому. Виникнення першого спричинюють механічні перешкоди, які заважають випорожненню привідної петлі (зрощення, спайки, перегин), другий є наслідком функціональних порушень: гіпотонії дванадцятипалої кишки, привідної петлі, сфінктера Одді та жовчного міхура, які можуть поєднуватися зі спазмом стоми та вивідної кишки.
У разі легкого перебігу хронічного синдрому привідної петлі відзначають лише нудоту, зригування жовчю і зрідка блювання невеликою кількістю жовчі, яке виникає через 0,5—2,5 години після іди. При синдромі середньої тяжкості після їди виникає біль у ділянці правого підребер’я, часто інтенсивний, блювання жовчю, слабкість, зниження працездатності, втрата маси тіла.
Для тяжкої форми захворювання характерні біль у правому підребер’ї, блювання жовчю майже після кожного споживання їжі, значне зменшення маси тіла, слабкість. Прояви синдрому привідної петлі посилюються при емоційному збудженні, споживанні молока та кисломолочних продуктів, жирних і солодких страв. Після блювання і в положенні хворого на лівому боці біль зменшується, а іноді навіть минає. У кишках посилюються процеси бродіння, що призводить до розвитку метеоризму, буркотіння.
Зазначені симптоми дають змогу лише запідозрити синдром привідної петлі. Остаточний діагноз встановлюють за допомогою рентгенологічного дослідження: барій, що проник у привідну петлю, затримується там надовго. При хронічному синдромі привідної петлі спостерігається порушення функції печінки та підшлункової залози.
Основні принципи лікування: часте харчування дрібними порціями, обмеження жирів. Після споживання їжі хворому слід деякий час полежати на правому боці. Пацієнтам із тяжкою формою синдрому привідної петлі показане оперативне лікування (дуоденоєюностомія, реконструктивні операції).
Хронічний гастрит кукси шлунка може бути і до операції, але в деяких випадках він розвивається або перебіг його погіршується після операції внаслідок закидання жовчі у шлунок (рефлюкс-гастрит), розвитку ахлоргідрії, розмноження в шлунку бактеріальної флори (зокрема Helicobacter pylori). На клінічну картину хронічного гастриту кукси може нашаровуватися симптоматика, притаманна синдрому малого шлунка: відчуття повноти, тиску і розпирання в надчеревній ділянці та ситості після споживання навіть невеликої кількості їжі, а також відрижка, нудота. Слизова оболонка кукси шлунка поступово атрофується, розвиваються вогнища кишкової метаплазії. Наслідком цього є виникнення в більшості хворих стійкої ахлоргідрії, зниження утворення пепсину. Евакуація вмісту кукси прискорюється. Водночас з атрофією слизової оболонки можуть виявлятися ерозії, особливо в ділянці анастомозу. Ерозії можуть бути як поверхневі, так і глибокі, з фібринозними нашаруваннями.
Атрофічний хронічний гастрит у куксі шлунка може через багато років трансформуватись у поліпоз чи рак (через 15 років — у 3% хворих). Нерідко вони не дають яскравих суб’єктивних симптомів, але якщо пухлина розташована близько до анастомозу, то вона може порушувати евакуацію шлункового вмісту. При рентгенологічному та ендоскопічному дослідженні часто важко відрізнити рак від псевдопухлини; у цьому випадку допомагає біопсія. Нерідко рак кукси розпізнають пізно, коли проведення радикальної операції неможливе.
Хронічний анастомозит, єюніт, ентерит, коліт. За наявності анастомозу хворі скаржаться на печію, спазматичний біль у верхній частині живота, іноді — блювання (особливо після вживання вина, цукру, кислої їжі). Вирішальне значення для розпізнавання анастомозиту має гастроскопія. Відмежувати органічні та функціональні зміни кишок після резекції шлунка дуже важко, найчастіше вони поєднуються.
Дискінезію кишок без органічних змін спостерігають досить рідко. Характерні такі морфологічні та функціональні зміни кишок: 1) прискорення проходження їжі по тонкій кишці, що поєднується зі спастичними скороченнями її; 2) атрофія слизової оболонки, утворення псевдокіст у відвідній петлі; 3) підгострий та хронічний єюніт з атрофічними змінами слизової оболонки або без них (в останньому випадку при електронній мікроскопії іноді виявляють ультраструктурні зміни в мікроворсинках та мітохондріях); 4) надмірне заселення верхнього відділу тонкої кишки патогенними або умовно-патогенними бактеріями (стафілококи, протей, кишкова паличка, зокрема її патогенні штами, дріжджові гриби, дипло-, стрептококи та інші бактерії, зокрема анаеробні). Частота та інтенсивність цього заселення корелює зі ступенем зниження кислотності шлункового соку, досягаючи максимуму при ахлоргідрії.
Запальні зміни відбуваються не лише в тонкій, а й у товстій кишці. Після резекції шлунка нерідко розвиваються органічні та функціональні ураження печінки, жовчних шляхів і підшлункової залози, які іноді виходять на перше місце в клінічній картині. Часто спостерігається загострення захворювань, які були до операції, або посилення властивих виразковій хворобі органічних та функціональних змін органів травлення. Порушуються основні функції печінки та підшлункової залози, розвивається жирова дистрофія печінки і, найчастіше, ультраструктурні зміни гепатоцитів, розвивається холецистит, дискінезія жовчних шляхів. Ці зміни зумовлені дисбактеріозом, порушення секреції холецистокініну та секретину слизовою оболонкою дванадцятипалої кишки, порушенням нормального складу жовчі та її стазом унаслідок розладу нервово-гуморальної регуляції.
Клінічна картина ентериту характеризується здуттям живота, болем у ділянці пупка, бурчанням у животі, болючістю при пальпації, спастичними скороченнями ділянок тонкої і товстої кишки. При коліті спостерігають проноси, що чергуються із закрепами, зміну характеру випорожнень.
Лікування — консервативне (дієта, антибактеріальні препарати, ферментні засоби, речовини еубіотичної дії на мікробну екосистему кишок).
Розвиток хронічного гепатиту пов’язаний з подовженням латентного періоду виділення жовчі після резекції шлунка, застоєм у привідній петлі, запальними і застійними змінами в ній і в зоні великого сосочка дванадцятипалої кишки. Нерідко діагностують пострезекційний гепатит, що в 4—20% випадків призводить до цирозу печінки.
Лікування пострезекційного гепатиту — консервативне (дієта, гепатотропні засоби, інфузійна терапія, вітаміни, спазмолітики, жовчогінні, фізіотерапія).
Корекція функціональних розладів жовчних шляхів полягає в дотриманні дієтичного режиму (дієти № 5а та 5), беззондовому дренажі жовчних шляхів; призначенні жовчогінних засобів, теплових процедур.
Поряд з ураженням гепатобіліарної системи виявляють патологічні зміни підшлункової залози. Операційна травма може призвести до розвитку як гострого панкреатиту та панкреонекрозу, так і хронічного панкреатиту. Виникненню останнього сприяють підвищення тиску у дванадцятипалій кишці, атонія сфінктера Одді, порушення харчування, розлади функції печінки та жовчних шляхів. Основними проявами панкреатиту є порушення зовнішньосекреторної функції підшлункової залози, які найбільшою мірою виявляються в ранній післяопераційний період, а пізніше зменшуються і навіть зникають. Водночас зі зменшенням секреції, зниженням активності панкреатичних ферментів, диспанкреатизмом можуть з’являтися порушення внут- рішньосекреторної функції підшлункової залози.
Розрізняють хронічний рецидивний, латентний і больовий панкреатит. Рецидивний панкреатит виявляється періодичними загостреннями, болем у надчеревній ділянці з іррадіацією в спину, ліве плече, підвищенням рівня амілази в крові і сечі, запальним і диспепсичним синдромами. Больовий панкреатит проявляється безперервним болем у животі, схудненням, астенічним синдромом. Латентна форма хронічного панкреатиту проявляється ознаками екскреторної (ферментної) та інкреторної (цукровий діабет) недостатності.
Лікування хронічного пострезекційного панкреатиту аналогічне такому при інших формах хронічного панкреатиту — дієта, замісна, ферментна терапія, фізіотерапевтичні процедури тощо. Лікування інших постгастрорезек- ційних синдромів поліпшує перебіг панкреатиту. У поодиноких випадках показане оперативне лікування (при розвитку кіст, повній оклюзії проток підшлункової залози, малігнізації).
Рефлюкс-езофагіт особливо часто спостерігають після тотальної резекції шлунка. Найхарактернішими його симптомами є печія, біль за грудниною, регургітація гіркого і кислого шлункового вмісту, особливо в положенні лежачи.
Частим ускладненням резекції шлунка буває пострезекційна дистрофія.
Постгастрорезекційна анемія розвивається у 10-15% хворих, оперованих за методом Білльрот II, і зустрічається у двох варіантах: гіпохромна залізодефіцитна анемія і гіперхромна В12-дефіцитна анемія.
Патогенез залізодефіцитної анемії пов’язаний з порушенням йонізації і резорбції заліза внаслідок ахлоргідрії, прискореного пасажу по тонкій кишці й атрофічного ентериту, а також із кровотечами, нерідко прихованими, із септичних виразок анастомозу.
До розвитку В12-дефіцитної анемії призводять різке зменшення продукування внутрішнього фактора Кастла після видалення антрального відділу шлунка, розвиток атрофії слизової оболонки тонкої кишки і дисбактеріозу.
Диференціальна діагностика анемій грунтується на вивченні периферійної крові і кісткового мозку. У периферійній крові при залізодефіцитній анемії спостерігається гіпохромія еритроцитів і мікроцитоз, а при В12-дефіцитній анемії — гіперхромія і макроцитоз. У мазку кісткового мозку при В12-дефіцитній анемії виявляють мегалобласто’ідний тип кровотворення.
Лікування гіпохромної залізодефіцитної анемії проводять препаратами заліза. Зазвичай призначають всередину залізовмісні препарати (фероплекс, ферамід, тардиферон) з одночасним уживанням аскорбінової кислоти в добовій дозі 0,2—0,3 г. Парентеральна терапія препаратами заліза показана тільки в разі непереносимості препаратів заліза, застосовуваних всередину, та їхньої неефективності.
Лікування хворих на В12-дефіцитну анемію починають зі щоденного введення вітаміну В12 (по 100—200 мкг) і продовжують до ретикулоцитного кризу (підвищення кількості ретикулоцитів у периферійній крові більше ніж у 10 разів), що зазвичай настає на 5-й день лікування. У подальшому, до настання гематологічної ремісії (зазвичай 4—5 тиж) препарат уводять у таких самих дозах через день, а надалі — 2 рази на місяць. Лікування вітаміном В12 слід поєднувати з призначенням фолієвої кислоти всередину по 0,001—0,002 г З рази на день.
Метаболічні порушення розвиваються найчастіше після резекції шлунка, що значно порушує функціональний синергізм органів травної системи. У патогенезі цих порушень, очевидно, істотну роль відіграє не тільки видалення значної частини органа, а й вимикання пасажу через дванадцятипалу кишку, якщо резекція виконана за методом Білльрот II. Метаболічні порушення можуть супроводжувати перераховані вище розлади, ніби вплітаючись у їхню клінічну картину, або, іноді, мати самостійне значення. Найяскравішим проявом метаболічних порушень у клініці є дефіцит маси тіла. Зменшення маси тіла нижче від нормальної або неможливість набрати доопераційну масу відзначають приблизно в 1/4 оперованих.
Серед багатьох причин цих порушень можна відзначити зменшення об’єму їжі, непереносимість окремих продуктів, порушення абсорбції жиру і білка, засвоєння вітамінів і мінеральних речовин. Усе це досить демонстративно, коли оперовані хворі страждають на виражену діарею, гіповітамінози, кісткову патологію (остеопороз або остеомаляція).
Лікування метаболічних порушень є складною проблемою і в його основі повинна лежати дієтотерапія. У тяжких випадках показане стаціонарне лікування (спеціальні висококалорійні дієти, замісна терапія, андрогени).
Підвищена сприйнятливість до інфекційних захворювань. Висока резекція шлунка досить часто призводить до реактивації туберкульозу легень, який був у хворого раніше, або підвищує схильність до цього захворювання. Цю обставину варто завжди мати на увазі, вирішуючи питання діагностики і лікування постгастрорезекційних порушень, особливо якщо у хворих наявні виражені розлади харчування і дефіцит маси. Вказівки на туберкульоз в анамнезі є вагомою підставою для вибору найраціональнішого способу операції при виразковій хворобі, що забезпечить належною мірою запобігання тяжких розладів харчування в післяопераційний період (наприклад, пілороплас- тика з ваготомією).
Після резекції шлунка досить часто (до 10% усіх випадків) розвиваються перигастрит і перивісцерит, що зумовлено: 1) загостренням після операції перигастриту, який ускладнює перебіг виразкової хвороби; 2) травматизацією та інфікуванням під час операції; 3) рецидивами виразкової хвороби; 4) запальними змінами в ділянці анастомозу.
Для перивісцериту характерний сталий тривалий біль у животі, який посилюється під час різких рухів, трясьби. При об’єктивному дослідженні відзначають гіперестезію у зонах Захар’Їна—Геда. У хворих з перигастритом зона тимпанічного звуку над куксою шлунка може досягати правої пригруднинної, а інколи — навіть правої середньоключичної лінії, одночасно поширюючись догори. При повторному обстеженні через декілька днів конфігурація і розміри цієї зони істотно не змінюються (симптом Стражеска). Під час пальпації живота, особливо глибокої, відзначають болючість. Періодично спостерігають підвищення температури тіла до субфебрильних величин. Перивісцерит може зумовити появу ознак часткової кишкової непрохідності, що потребує повторного оперативного втручання і призведе до подальшого прогресування спайкового процесу. При перигастриті рентгенологічне дослідження виявляє деформацію кукси шлунка, зменшення рухомості петель кишок та поширення їх вище від місця звуження.
Пухлини оперованого шлунка
Рак шлунка або шлунково-кишкового анастомозу у хворих на виразкову хворобу, які перенесли резекцію шлунка чи гастроентеростомію, трапляється рідко.
Рак кукси шлунка частіше розвивається після резекції шлунка за Білльрот II, ніж за Білльрот І, що пов’язують з рефлюксом жовчі в шлунок. Певну роль у розвитку раку кукси шлунка відіграє також анаеробна флора, що перетворює нітрати їжі на канцерогенні нітрозаміни. Рак кукси шлунка розвивається через 20—25 років після резекції шлунка, але можливий і більш ранній розвиток. Як правило, пухлина розташовується в ділянці гастроентероанасто- мозу, а потім поширюється вздовж малої кривини шлунка до кардіального відділу.
Проте деякі вчені вважають, що у хворих, які перенесли резекцію шлунка, є чинники утворення раку. До них належать відсутність хлоридної кислоти, наявність у цих хворих атрофічного гастриту.
Основними симптомами раку кукси шлунка є:
• постійний біль у надчеревній ділянці;
• виражене відчуття важкості в надчерев’ї після "їди, відрижка тухлим;
• зменшення або повне зникнення апетиту;
• прогресивне схуднення хворого;
• наростання слабкості;
• розвиток анемії;
• постійно позитивна реакція Ґреґерсена.
Рак кукси шлунка має форму поліпа або виразки. Для ранньої діагностики раку кукси шлунка надзвичайно важливо вчасно проводити фіброезогас- тродуоденоскопію з обов’язковою біопсією слизової оболонки шлунка.
Завдяки радикальній операції деякі хворі із пухлиною кукси шлунка або шлунково-кишкового анастомозу одужують. Для правильного і своєчасного діагностування захворювання слід ретельно і вдумливо аналізувати всю отримувану інформацію: анамнестичні дані, скарги, загальний стан, дані лабораторно-рентгенологічних і ендоскопічних досліджень.
Хворий після резекції шлунка має перебувати на диспансерному спостеріганні і проходити ФЕГДС 1—2 рази на рік. Надалі ФЕГДС проводять з появою або посиленням "шлункових" скарг.
Діагностика пухлин оперованого шлунка пов’язана зі значними труднощами, оскільки симптоматика раку шлунка може поєднуватися з клінічною картиною інших хвороб оперованого шлунка і таким чином послабити онкологічну настороженість лікаря. Різні деформації, спричинені спайками, рубцями або накладеним анастомозом, роблять рентгенологічну діагностику малоефективною. Гастроскопія також не завжди дає достовірні дані.
У клінічній картині переважають явища дискомфорту, втрата апетиту, наростання слабкості, відрижка повітрям, блювання і нудота, яких не було у хворого тривалий час після перенесеної операції. Больовий синдром зазвичай спричинюється поєднанням пухлини з хронічним панкреатитом або пептичною виразкою. Відзначається виражений дефіцит маси тіла (10—14 кг), помірна гіпохромна анемія (НЬ у середньому 100 г/л), збільшення ШОЕ. Часто наявна клінічна картина непрохідності відвідної петлі пухлинної природи. Загалом поєднання ахлоргідрії, анемії і загального ослаблення організму дають змогу встановити пухлинну природу захворювання.
Постваготомічні синдроми виникають у 15—20% оперованих і пов’язані з тактичними і технічними помилками: до, під час і після операції.
Доопераційні помилки:
1) при встановленні показань до операції (виконання ваготомій за наявності значних анатомо-морфологічних змін в пілородуоденальній зоні; при синдромі Цоллінгера—Еллісона);
2) при визначенні термінів виконання органозберігальних операцій (парасимпатична денервація шлунка за наявності виразок великих розмірів, вираженого запального процесу в тканинах, прилеглих до зони виразки).
Інтраопераційні причини:
1) помилки техніки парасимпатичної денервації шлунка і виконання операцій дренування шлунка (поранення суміжних органів, ушкодження судин черевної порожнини);
2) неврахування варіантів розгалуження блукаючих нервів.
Післяопераційні причини постваготомічних синдромів (ранні, найближчі і пізні) в ранній післяопераційний період пов’язані з:
1) помилками техніки операції (кровотеча в черевну порожнину, перитоніт, набряк стравоходу або стиснення його гематомою, некроз стінки шлунка і стравоходу, кровотеча з ерозованої судини на дні пенетраційної виразки дванадцятипалої кишки тощо);
2) неадекватним веденням післяопераційного періоду (неефективна декомпресія шлунка і стимуляція моторики кишок).
У найближчий термін після операції хвороби ваготомічного шлунка, як правило, зумовлені гіпомоторикою шлунка або дванадцятипалої кишки (га- стро- і дуоденостаз), гіпермоторикою тонкої кишки (демпінг-синдром), дис- координацією рухової активності шлунка і кишок (діарея, дуоденогастраль- ний рефлюкс).
У віддалений період постваготомічні синдроми спричинюються переважно неадекватною або неповною ваготомією, дуоденогастральним рефлюксом, недостатнім дренуванням шлунка тощо.
Органозберігальні операції можуть призводити до розвитку раннього і пізнього демпінг-синдрому.
Ранній демпінг-синдром займає друге місце серед патологічних станів у осіб, які перенесли ваготомію.
Клінічна картина постваготомічного демпінгу не відрізняється від тієї, що її спостерігають у хворих після резекції шлунка. Водночас постваготомічний демпінг-синдром характеризується більш легким перебігом. Зі збільшенням термінів післяопераційного періоду просліджується тенденція до зменшення його клінічних проявів, аж до повного зникнення.
Діагностика постваготомічного демпінг-синдрому Грунтується на аналізі його клінічної картини, результатів рентгенологічних і ендоскопічних досліджень і об’єктивізується провокаційним тестом із глюкозою. Проба вважається позитивною, коли після вживання хворим 150 мл 20% розчину глюкози рівень глюкози в крові збільшується порівняно з нормою в середньому на 10—15%.
Лікування демпінг-синдрому після ваготомії переважно консервативне. Рекомендується повільне, малими порціями вживання їжі з обмеженням кількості простих вуглеводів. У більшості хворих із легким перебігом демпінг-синдрому дотримання таких рекомендацій дозволяє позбутися його. Хворим з важчим перебігом демпінг-синдрому призначають препарати, які поліпшують травлення і всмоктування їжі, сповільнюють евакуацію зі шлунка і моторику кишок. З цією метою пацієнти одержують сік подорожника, плантаглюцид, пепсидил, кислоту хлоридну розведену, ферментативні засоби (фестал, панкреатин, панзинорм та ін.). Використовують також холіноблокатори — атропіну сульфат (0,5—0,75 мл 0,1%, розчин уводять внутрішньом’язово за 10—15 хв до їди), гастроцепін (25 мг 2—3 рази на день за 20—30 хв до їди протягом 2—4 тиж). У пацієнтів з астенічним синдромом доцільно застосовувати ципрогептадин (перитол) по 4 мг перорально 2-3 рази на день за 15—30 хв до їди. При демпінг-синдромі, який поєднується з депресивним станом, призначають циклічний антидепресант амітриптилін, який має холі- ноблокувальну здатність. Амітриптилін уживають усередину по 12,5—25 мг 1—2 рази на день до їди. Доведено позитивний результат при демпінг-синдромі реасексу (містить дифеноксилат і атропін) і лопераміду (імодіуму) — по 1/2 таблетки 1—2 рази на день перед сніданком і обідом протягом 2—3 тиж). До комплексу консервативних заходів включають і препарат L-ДОФА (леводоп) — 125 мг за 15 хв до їди 2 рази на день, який позитивно впливає на порушену при демпінг-синдромі нейрогуморальну регуляцію завдяки збільшенню синтезу в ЦНС дофаміну. Консервативні заходи дозволяють усунути прояви демпінгу легкого ступеня і значно поліпшити стан хворих при демпінг-реакції середнього і тяжкого ступенів. У виняткових випадках тяжкого постваготомічного демпінг-синдрому, що супроводжується виснаженням пацієнтів і порушенням працездатності, показане оперативне лікування.
Діарея належить до специфічних ускладнень ваготомії, частіше розвивається після стовбурової ваготомії і рідше — після селективної проксимальної ваготомії — у 2—10% випадків. Виникнення її пов’язують із посиленням моторики кишок, що супроводжується пришвидшенням пасажу їжі по травному тракту.
Легкі форми діареї зазвичай не потребують спеціального лікування, з часом вони зазнають зворотного розвитку і легко коригуються дієтою. Хворим із перебігом середньої тяжкості і тяжким призначають препарати, що нормалізують моторику травного тракту (бензогексоній, церукал, ганглерон, реглан), знижують абсорбцію жовчних солей у кишках (холестирамін), антихолінергічні засоби (атропін, скополамін, препарати беладони), ферментні препарати (фестал, панзинорм). Виражену антидіарейну дію мають дифеноксикислоти (реасек) і опіоди (імодіум). Ці препарати застосовують по 2-3 таблетки на день протягом 3—10 днів до досягнення ефекту. За наявності дисбактеріозу проводять його корекцію. У разі відсутності ефекту від консервативного лікування деякі хірурги пропонують оперативне втручання.
Гастростаз характеризується порушенням моторно-евакуаторної функції шлунка і є специфічним постваготомічним синдромом, який спостерігають у 2—23% пацієнтів.
Найчастіше гастростаз з’являється в осіб, оперованих з приводу пізніх стадій стенозу, тому що у них вже до операції є порушення моторної функції шлунка. Найчастіше розвитку гастростазу сприяють ушкодження нерва Латарже під час СПВ, аностомозити, дуоденостаз, перигастрит, високе розташування пілородуоденального переходу внаслідок особливостей анатомічного розвитку гастродуоденальної системи на тлі ослаблення рухової активності ваготомічного шлунка, звуження або повне зрощення ГДА.
Діагностика гастростазу і його причин ґрунтується на аналізі скарг, даних анамнезу, результатів рентгенологічного, фіброгастроскопічного і елект- рогастрографічного методів досліджень. Шлунок при гастростазі перерозтяг- нутий, атонічний, містить велику кількість слизу та їжі. Як у ділянці тіла шлунка, так і в пілороантральному відділі спостерігають скупчення газів. Найвірогіднішу інформацію про ступінь гастростазу дає простежування евакуації барієвої суспензії зі шлунка через 6, 12, 24 год.
Інструментальний метод дослідження дозволяє віддиференціювати функціональний гастростаз від органічного. Так, проводячи рентгенологічне дослідження, варто мати на увазі, що органічний гастростаз супроводжується посиленням перистальтики і відсутністю евакуації зі шлунка в будь-якому положенні хворого. Функціональний гастростаз характеризується вільним спорожнюванням шлунка від барієвої суспензії переважно в положенні пацієнта лежачи на правому боці. При фіброгастроскопії в осіб з органічною гастропатією визначають звуження ділянки анастомозу (анастомозит), підвищене скупчення стравохідного хімусу у дванадцятипалій кишці (органічний дуоденостаз), а при функціональному гастростазі — атонію шлункової стінки, виражену антиперистальтику дванадцятипалої кишки. Реєстрація біоелектричної активності шлунка виявляє різке зниження всіх параметрів електро- гастрограм у разі функціональної гастроплегії і підвищення їх — у пацієнтів з органічною гастропатією.
Лікування гастростазу проводять комплексно, з урахуванням його причин. Застосовують постійну фракційну або тимчасову (2—3 рази на добу) декомпресію шлунка. Терміни декомпресії визначаються швидкістю відновлення моторно-евакуаторної функції шлунка. Призначають церукал (1 мл внутрішньом’язово 1—3 рази на день), бензогексоній (0,5—1 мл 2,5% розчину внутрішньом’язово 1—3 рази надень), пітуїтрин (1 мл підшкірно 1—3 рази на день), прозерин (1 мл 0,05% розчину 1—3 рази на день). Внутрішньовенно вводять полійонні розчини, солі калію, хлоридів, 10% розчин ксиліту (0,5 мл на 1 кг маси тіла). Ефективним методом лікування гастростазу є стимуляція рухової активності шлунка діадинамічними і синусоїдальними струмами, йонофорез ацетилхоліну.
У разі значного розширення шлунка, атонії і стоншення його стінки при гастростазі будь-якого ґенезу найкращим методом операції є резекція шлунка. При значному ризику операції в такій ситуації можливе виконання дренувальних операцій на шлунку.
Профілактика гастростазу полягає в правильному виконанні операції, проведенні комплексу консервативних заходів, спрямованих на відновлення рухової функції ваготомованого шлунка з 1-го дня післяопераційного періоду.
Прояви більшості постваготомічних розладів подібні до тих, які спостерігають після резекції шлунка. Після селективної проксимальної ваготомії рецидив виразкової хвороби виникає в 4—14% випадків. З удосконаленням оперативної техніки цей відсоток зменшується і подовжується проміжок часу від оперативного втручання до виникнення рецидиву (нині він коливається в межах 1—8 років). На відміну від рецидивної виразки після резекції шлунка постваготомічна рецидивна виразка часто має малосимптомний і навіть асимптомний перебіг. Після консервативного лікування вона рубцюється у 80% пацієнтів і лише 20% хворих потребують повторної операції (реваготомія, резекція або пілоропластика).
Шлунково-стравохідний рефлюкс-езофагіт, який часто супроводжує виразкову хворобу, особливо дуоденальної локалізації, після операції селективної проксимальної ваготомії внаслідок зниження кислотності шлункового вмісту в більшості випадків виліковується, тому рефлюкс-езофагіт, який виявляють після цієї операції, найімовірніше, був і до неї. Для лікування шлунково-стравохідного рефлюкс-езофагіту застосовують відповідний дієтичний режим, прокінетики (див. "Гастроезофагальна рефлюксна хвороба").
Рефлюкс-гастрит виникає у 5—35% оперованих після резекції, ваготомії, гастроентеростомії і сфінктеропластики внаслідок закидання дуоденальної жовчі в шлунок і дії на його слизову оболонку солей жовчних кислот, ферментів підшлункової залози, лізолецитину. Останній руйнує клітини епітелію шляхом видалення з їхньої структури ліпідів, призводячи до зворотної дифузії Н+ і надходження Na+, що спричинюється до утворення в шлунку ерозій і виразок. Лужне середовище сприяє активному зростанню мікрофлори, активуючи ураження слизової оболонки бактерійним ендотоксином.
Клінічна картина. Хворого турбують відрижка, біль у надчерев’ї, блювання жовчю, втрата маси тіла. Виникають анемія, гіпо-, ахлоргідрія. Діагностика грунтується на фіброгастродуоденоскопії з біопсією слизової оболонки. Гістологічне дослідження біоптатів виявляє хронічне запалення слизової оболонки з явищами метаплазії і зменшенням кількості обкладкових клітин.
При постваготомічному рефлюкс-гастриті істотно знижується базальна і стимульована секреція хлоридної кислоти. При ендоскопічному дослідженні в шлунку виявляють підвищену кількість жовчі, відзначають набряк, гіперемію і кровоточивість слизової оболонки. Лабораторне дослідження свідчить про наявність в шлунковому сокові компонентів дуоденального вмісту.
Лікування лужного постваготомічного рефлюкс-гастриту полягає в зменшенні або усуненні ДГР, скороченні часу контакту дуоденального вмісту зі
шлунковою стінкою. Застосовують засоби, які стимулюють трофічні процеси в слизовій оболонці шлунка (гастрофарм по 2,6 г 3 рази на день за 30 хв до їди, метилурацил по 0, 25 мг 3 рази на день після їди), справляють цитопротекторну дію (сукралфат 6 г на день), прискорюють евакуацію шлункового вмісту (метоклопрамід), зв’язують жовчні кислоти (холестирамін) тощо.
У разі неефективності консервативного лікування показана реконструкція гастроентероанастомозу.
Рефлюкс-езофагіт — ускладнення ваготомії, зумовлене порушенням замикальної функції кардії, виявляють у 3—37% пацієнтів. У понад 6% хворих причиною його розвитку є грижа стравохідного отвору діафрагми і недостатність замикальної функції кардії. Унаслідок регургітації шлункового вмісту відбувається ушкодження слизової оболонки стравоходу різного ступеня вираженості.
При постваготомічному рефлюкс-езофагіті хворі скаржаться на біль за грудниною, печію, гіркоту в роті, стримування, регургітацію під час сну. У разі прогресування захворювання приєднується дисфагія, що пов’язана зі спазмом або стриктурою стравоходу, запаленням прилеглих тканин.
Діагностика рефлюкс-езофагіту носить комплексний характер, вона включає дані клініки і спеціальні методи дослідження (лабораторні, ендоскопічні, рентгенологічні).
Лікування захворювання в більшості пацієнтів консервативне, спрямоване на поліпшення моторики травного тракту і трофіки уражених тканин. При відсутності ефекту, наявності грижі стравохідного отвору діафрагми застосовують операцію відновлення замикальної функції кардії.
Дуоденостаз — рідкісне ускладнення ваготомії. Причинами поствагото- мічного дуоденостазу є недіагностоване до операції хронічне порушення дуоденальної прохідності, артеріо-мезентеральна компресія ДПК, рубцевий процес у ділянці дуоденоєюнального переходу або його високе стояння, інверсія дванадцятипалої кишки. В окремих випадках дуоденостаз розвивається внаслідок технічних погрішностей під час операції: ушкодження кишкової стінки, надмірної мобілізації дванадцятипалої кишки за Мохері, неправильного виконання дренувальних операцій на шлунку.
Специфічні клінічні прояви постваготомічного дуоденостазу відсутні. Хворих турбують почуття важкості, повноти в надчерев’ї і правому підребер’ї, гіркота в роті, нудота, блювання з домішкою жовчі.
Діагностика дуоденостазу ґрунтується на лабораторно-інструментальних методах дослідження. Найінформативнішим є рентгеноскопія (графія) шлунка і дванадцятипалої кишки, завдяки яким виявляють значне розширення останньої з тривалим затримуванням у ній контрастної суспензії.
Лікування дуоденостазу найчастіше консервативне. Однак воно не завжди ефективне, тому за суворими показаннями виконуються операції. Перевагу віддають резекції шлунка з накладенням гастроентероанастомозу "кінець у бік" за Ру або резекції дуоденального кута (операція Робінсона).
Утворення каменів у жовчному міхурі після ваготомії реєструють у 0,9— 1,2% випадків незалежно від виду парасимпатичної денервації шлунка. В одних пацієнтів конкременти в жовчному міхурі клінічно не виявляються, в інших — призводять до розвитку нападу гострого холециститу або холецис-топанкреатиту.
Утворення каменів у жовчному міхурі пов’язують з його постваготоміч- ною атонією і застоєм жовчі.
Ведення пацієнтів з постваготомічним холецистолітіазом залежить від клінічних проявів захворювання. Якщо наявність каменів не проявляється відповідними симптомами, показане диспансерне спостерігання. У разі розвитку хронічного калькульозного холециститу виконують планову операцію. Лікування гострого калькульозного постваготомічного холециститу здійснюється відповідно до загальноприйнятої тактики.
У 0,5—20% випадків після ваготомії, переважно стовбурової і селективної, можуть виникати синдроми мальдигестії (недостатності травлення) і мальабсорбції (недостатності всмоктування). Синдроми зумовлені постваготомічним дефіцитом травних ферментів, зміною структури порожньої і клубової кишок, порушенням транспортних механізмів, рухової функції кишок, розвитком кишкової патогенної мікрофлори.
Синдром характеризується відчуттям важкості в животі, його здуттям, бурчанням, рідкими випорожненнями, слабкістю, підвищеною стомлюваністю. В окремих випадках відзначають трофічні розлади шкіри, волосся, нігтів.
Як правило, в осіб з постваготомічним синдромом мальабсорбції є певні порушення порожнинного і мембранного травлення, а також всмоктування в доопераційний період. Ці зміни констатують за даними визначення активності ферментів порожнинного і мембранного травлення з одночасним вивченням всмоктувальної функції тонкої кишки (D-ксилозним тестом). Зазвичай в осіб з вказаними синдромами відзначають різке пригнічення порожнинного і мембранного травлення. У 80—87% випадків всмоктування речовин порушується як у проксимальних, так і в дистальних відділах тонкої кишки. На відміну від демпінг-синдрому і діареї синдром недостатності травлення зі збільшенням терміну спостереження не має тенденції до зворотного розвитку.
Лікування хворих із синдромами мальдигестії і мальабсорбції починається з консервативних заходів: призначення дієти з підвищеним вмістом білків, жирів, вуглеводів, корекції порушень водного й електролітного обміну кислотно-лужного стану, проведення замісної терапії (шлунковий сік, хлоридна кислота, фестал, панкреатин, панзинорм). Неефективність тривалої терапії, тяжкість клінічних проявів синдромів є показанням до оперативного втручання — тонкокишкової гастродуоденопластики.
Частота дисфагії після операцій ваготомії коливається від 2 до 30%. Останніми роками кількість цих ускладнень значно зменшилася, що пов’язано переважно з відмовою від стовбурової ваготомії і заміною її селективною проксимальною ваготомією (перерізування гілок блукаючого нерва, що стимулюють продукцію хлоридної кислоти та іннервують кардіальний відділ шлунка, тоді як іннервація антрального відділу зберігається). Але навіть при стовбуровій ваготомії дисфагія звичайно є не постійним, а лише інтермітив- ним симптомом, який або спонтанно зникає через декілька років після операції, або піддається консервативній терапії.
Причинами ранньої дисфагії є травма і набряк стінки стравоходу і на- вколостравохідної тканини, порушення функції кардіального пригнічення внаслідок денервації. Рання дисфагія зазвичай не досягає важкого ступеня і самостійно минає через 1—2 міс. Розвиток дисфагії в більш віддалені від ваготомії терміни пов’язують з фіброзом у зоні операції і стенозуванням дистального відділу стравоходу. Пізня дисфагія буває більш вираженою і стійкою.
При дисфагії легкого ступеня рентгенологічними і ендоскопічними методами зазвичай не вдається виявити жодних патологічних змін у стравоході. У тяжких випадках рентгенологічно виявляють субстенотичні розширення і затримання барієвої суспензії в дистальному відділі стравоходу, а ендоскопічно — рефлюкс-езофагіт.
Короткочасна дисфагія раннього післяопераційного періоду не потребує спеціального лікування. При невротичних розладах призначають транквілізатори і седативні засоби. При стійкій дисфагії, що виникла в пізній період, нерідко доводиться вдаватися до бужування стравоходу.
Специфічним ускладненням ваготомії є відчуття наповненості у ділянці надчерев’я, що виникає відразу після їди. Цей симптом спостерігають у третини випадків, і з’являється він одразу після операції. Його виникнення пояснюється як втратою проксимальною частиною денервованого шлунка здатності до адаптогенного розслаблення, так і гальмуванням евакуації не лише твердої, а й рідкої їжі. Цей симптом зазвичай піддається консервативному лікуванню, що полягає у частому споживанні "їжі дрібними порціями, уживанні всередину та в ін’єкціях метоклопраміду (церукалу, реглану), домперидону (мотиліуму), цизаприду (координаксу); інколи проводять промивання шлунка.
Діарея нерідко з’являється зненацька, іноді провокується споживанням молочної їжі і вуглеводів. У легких випадках — рідкі випорожнення до 2—3 разів на день протягом декількох днів. У більш тяжких випадках — дефекація до 10 разів на добу, а період загострення затягується до 1 міс і більше.
Лікування. При загостренні — дієта № 46 і 4в, після нормалізації випорожнень — повноцінне харчування з виключенням продуктів, які погано переносяться хворим. Для уповільнення кишкової пропульсії призначають ре- асек або імодіум протягом 5—7 днів. З метою поліпшення травлення використовують ферменти підшлункової залози; краще переносяться препарати чистого панкреатину, які не містять жовчних кислот.
Демпінг-синдром. Після селективної проксимальної ваготомії, особливо при застосуванні дренувальних операцій, розвивається в 10—15% хворих.
Однак тяжкі форми синдрому спостерігають дуже рідко. Найчастіше він пов’язаний з помилками під час операції, передусім з ушкодженням заднього стовбура блукаючого нерва. Причини розвитку постваготомічного демпінг- синдрому ті самі, що й постгастрорезекційного, — прискорене спорожнювання шлунка, підвищення осмотичного тиску в тонкій кишці, швидке всмоктування вуглеводів з наступним надлишковим утворенням інсуліну, роздратування рецепторного апарату тонкої кишки, що призводить до виділення біологічно активних речовин.
Діагностика і лікування постваготомічного демпінг-синдрому див. "Пост- гастрорезекційний демпінг-синдром".
Діарею після операції селективної проксимальної ваготомії спостерігають рідко. Найчастіше вона зумовлена ушкодженням стовбура блукаючого нерва під час операції. Патогенетичними механізмами такої діареї є підвищення продукування жовчних кислот, особливо урео- і хенодезоксихолевої, тому позитивний ефект буває в разі дотримання безмолочної дієти та призначення холестираміну, антацидних препаратів, які містять гідрат оксиду алюмінію, а також кальцію карбонату, білої глини. Для пригнічення мікробної гіперколонізації призначають антибіотики.
Порушення функції кардії проявляється симптомами ахалазії та рефлюкс- езофагіту і зазвичай перебігає легко. Лікування — консервативне (дієтотерапія, лікарські препарти).
Порушення спорожнення шлунка проявляється клінікою гастростазу. Іноді (окрім функціонального компонента) причиною його служить формування "каскадного" шлунка (3—4%). У разі порушення техніки фундоплікації при СПВ може статися звуження шлунка в середній і верхній третині. Важливе значення в діагностиці має рентгенологічне дослідження.
Якщо шлунок має вигляд пісочного годинника з вираженим порушенням евакуації вмісту, показана операція (резекція шлунка).
Порушення моторики біліарної системи і жовчнокам’яна хвороба частіше виникають після стовбурової ваготомії — дискінезія за атонічним типом (міхур Ашофа, атонія сфінктера Одді і гіпотонія жовчного міхура).
Лікування — консервативне. При жовчнокам’яній хворобі показана операція (відкрита або лапароскопічна холецистектомія).
У післяопераційний період проводять профілактику парезу кишок (декомпресія шлунка, церукал, прозерин, гіпертонічний розчин натрію хлориду внутрішньовенно, клізми), пневмонії (ЛФК, масаж грудної клітки, дихальна гімнастика), тромбоемболічних ускладнень (раннє вставання, еластичне бинтування нижніх кінцівок, контроль за станом системи згортання крові, введення антикоагулянтів). Харчування — з моменту усунення парезу шлунка і кишок, найчастіше з 3-го дня (послідовно призначають стіл № 1а, 16 і 1). Тривалість тимчасової непрацездатності залежить від характеру впливу післяопераційного періоду і становить у середньому 8—12 тиж. Хворий повинен перебувати на диспансерному спостеріганні.
Подальша інформація
Завжди консультуйтеся зі своїм лікарем, щоб переконатися, що інформація, яка відображається на цій сторінці, може бути застосована до ваших особистих обставин. Інформація призначена тільки для медичних фахівців.