Хронічний гломерулонефрит
Поширеність
Хронічний гломерулонефрит — імунозапальне захворювання нирок з первинним і переважним ураженням ниркових клубочків, а також із залученням до патологічного процесу інших структурних елементів ниркової тканини і неухильним прогресивним перебігом з розвитком хронічної ниркової недостатності.
Хронічний гломерулонефрит може бути наслідком гострого гломерулонефриту (вторинно-хронічний) або первинно-хронічним, якщо немає жодних даних про перенесений у минулому гострий процес. У такому разі ранні стадії захворювання часто виявляють під час випадкового дослідження сечі, оскільки виражені клінічні прояви спостерігають лише тоді, коли патологічний процес зайшов далеко. Як для першого, так і для другого типу хвороби характерний тривалий перебіг (роки, а іноді й десятиліття), що закінчується розвитком ниркової недостатності.
Порівняно з гострим гломерулонефритом хронічну форму діагностують у 2—4 рази частіше. Хворі на хронічний гломерулонефрит становлять 2% усіх терапевтичних хворих, а серед померлих його виявляють в 1% усіх розтинів. При епідеміологічних дослідженнях хронічний гломерулонефрит виявляють у 200—250 випадках на 100 тис. населення, трохи частіше у чоловіків (3:2). Є істотні розходження в частоті хронічного гломерулонефриту залежно від віку: на вік 20—50 років приходиться від 80 до 90% хворих. Серед осіб віком понад 60 років захворювання трапляється досить рідко.
Етіологія
Хронічний гломерулонефрит часто є наслідком невилікуваного або вчасно не діагностованого гострого гломерулонефриту, тому причини його виникнення в цих випадках такі самі, як і при гострому гломерулонефриті. Однак Volhard ще в 1936 р. відзначав відсутність гострої фази захворювання в 45% випадків. При цьому етіологічними чинниками гломерулонефриту найчастіше є вогнище тривалої, переважно стрептококової, інфекції, віруси гепатиту, збудники сифілісу та інших інфекцій. Виникнення хронічного гломерулонефриту пов’язують також із тривалим впливом хімічних агентів (зокрема ліків) та деяких інших чинників. Багаторічний латентний перебіг може бути зумовлений змінами біологічних властивостей інфекційних збудників.
Випадки захворювання, коли хронічний гломерулонефрит виникає і розвивається без гострої фази, а в анамнезі відсутні вказівки на перенесений у минулому гострий гломерулонефрит, прийнято визначати як первинно- хронічний гломерулонефрит. Установити причину такого варіанта хронічного гломерулонефриту можна лише в 10—15% випадків.
Серед чинників, які зумовлюють перехід гострого гломерулонефриту в хронічний, можуть мати значення наявність і, особливо, загострення вогнищевої стрептококової та іншої інфекції, повторні переохолодження, особлива дія вологого холоду, несприятливі умови праці і побуту, травми, зловживання алкоголем. При цьому вогнища інфекції розглядають як джерела сенсибілізації організму, що підтримують імунозапальний процес у нирках.
Вторинний хронічний гломерулонефрит може бути одним із проявів системних захворювань сполучної тканини (системного червоного вовчака, ревматоїдного артриту та інших захворювань), а також системного васкуліту, наприклад геморагічного.
Патогенез
Загальновизнано, що в основі розвитку і прогресування хронічного гломерулонефриту лежать імунопатологічні процеси. Розрізняють два варіанти імунологічного генезу хронічного гломерулонефриту:
1) імунокомплексний;
2) автоімунний з антитілами проти базальної мембрани клубочків.
Обговорюється питання про можливу участь у генезі хронічного гломерулонефриту і третього механізму, клітинного, тобто участь Т- і В-лімфоцитів.
З неімунних чинників у патогенезі хронічного гломерулонефриту велике значення надають гіперкоагуляції, підвищенню внутрішньосудинного зсідання крові, випаданню фібрину і продуктів його розпаду в клубочкових капілярах, а також підвищенню в крові концентрації кінінів, серотоніну, гістаміну, реніну, простагландинів тощо. Порушення в системі гемостазу і фібринолізу є однією із важливих патогенетичних ланок розвитку і прогресування гломерулонефриту.
Патологічна анатомія. На ранніх етапах хронічного гломерулонефриту макроскопічно нирки можуть бути мало змінені. Згодом спостерігають прогресивне зменшення їхніх розмірів і маси, ущільнення тканини. Поверхня нирки спочатку гладенька, потім стає дрібнозернистою, капсула, якщо процес зайшов далеко, знімається важко, кіркова речовина стоншується, межа між нею і мозковою речовиною стирається. У термінальній стадії хронічного гломерулонефриту розвивається так звана вторинно-зморщена нирка (див. вклейку, мал. 36).
Мікроскопічно в нирках виявляють гіаліноз і спустошення клубочків, атрофію відповідних канальців. На пізніх стадіях захворювання зберігаються лише поодинокі гіпертрофовані нефрони. В інтерстиціальній тканині виявляють масивні лімфоїдно-плазматичні інфільтрати.
При хронічному гломерулонефриті спостерігаються також різні за характером і ступенем вираженості патологічні зміни з боку судин нирок. Так, у дрібних артеріях і артеріолах розвивається проліферативний ендартерит з подальшим переходом у склероз інтими, звуженням або повною облітерацією просвіту судин. При гіпертонічній формі хронічного гломерулонефриту виявляють артеріологіаліноз і, рідше, артеріолосклероз. Можлива і гіперплазія інтими середніх і великих судин нирки. Унаслідок цих змін прогресивно знижується нирковий кровотік, а згодом відзначають запустіння лімфатичних судин і порушення лімфообігу.
У стромі нирок при хронічному гломерулонефриті розвиваються набряк, клітинна інфільтрація, склероз, які більш різко виражені в мозковій речовині нирок. У кірковій речовині на місці загиблих нефронів з’являються вогнища склерозу, які в міру прогресування захворювання зливаються між собою й утворюють великі рубцеві поля.
Морфологічна класифікація. Прижиттєва пункційна біопсія нирок з гістологічним дослідженням біоптатів за допомогою оптичної та електронної мікроскопії дає змогу детально вивчити гістоморфологічні зміни всіх структурних елементів ниркової тканини на різних етапах патологічного процесу — від ранньої фази до термінальної. Крім визначення морфологічних форм хронічного гломерулонефриту завдяки гістологічним дослідженням біопсійного матеріалу можна оцінювати особливості перебігу і прогноз захворювання, а також вибирати найраціональнішу терапію.
На підставі даних морфологічного дослідження тканини нирки, одержаних шляхом пункційної біопсії, згідно з класифікацією ВООЗ та доповненнями В.В. Серова (1995) і В.А. Варшавського (2000), первинні ушкодження клубочків поділяють на такі форми:
1) мінімальні зміни клубочків (так званий ліпоїдний нефроз);
2) мембранозний гломерулонефрит;
3) інтракапілярний проліферативний гломерулонефрит;
4) мезангіокапілярний (мембранозно-проліферативний) гломерулонефрит;
5) мезангіопроліферативний гломерулонефрит;
6) фокально-сегментарний гломерулосклероз;
7) екстракапілярний гломерулонефрит з півмісяцями;
8) фібропластичний (склерозивний) гломерулонефрит.
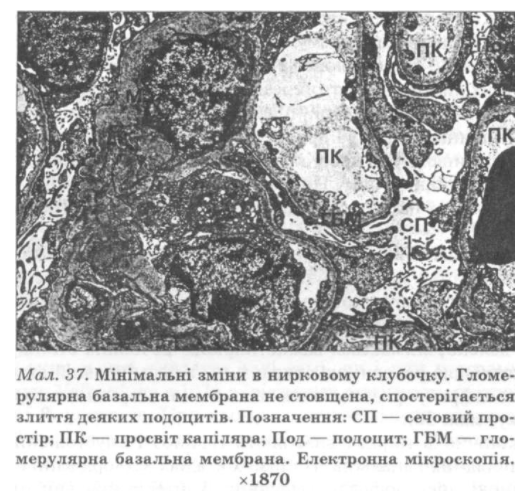
Мінімальні зміни клубочків виявляють тільки за допомогою електронної мікроскопії. Вони неспецифічні і характеризуються злиттям педикул подоцитів, що призводить до зникнення фільтрувальних проміжків між ними (мал. 37). Базальні мембрани не змінені. Будь-яких змін у клубочках при світловій мікроскопії не виявляють (див. вклейку, мал. 38). Під час імуно-флуоресцентного дослідження імуноглобулінів, комплементу і фібриногену в капілярах клубочків не виявляють. Клінічно мінімальні зміни в клубочках проявляються зазвичай у вигляді ідіопатичного нефритичного синдрому або ліпоїдного нефрозу. Установити правильний діагноз цього морфологічного типу гломерулонефриту можна тільки на підставі даних електронно- мікроскопічного дослідження.
Мембранозний гломерулонефрит при світловій мікроскопії (див. вклейку, мал. 39) характеризується дифузним стовщенням, набуханням і розщепленням базальних мембран капілярів клубочків з відкладенням на "їхньому зовнішньому боці депозитів, які складаються з імуноглобулінів G, рідше — А, М та фракції комплементу СЗ; проліферації мезангія не виявляють. Ці зміни можна спостерігати в кількох або в усіх капілярних петлях клубочка, у зв’язку з чим розрізняють вогнищевий і дифузний мембранозний гломерулонефрит.
При цьому внаслідок деполімеризації полісахаридів (зокрема, гіалуронової кислоти), що входять до складу базальної мембрани, збільшуються розміри пор, діаметр яких у кілька разів перевищує нормальний. Фіксація імунокомплексів на базальній мембрані є початком її ушкодження і підвищення проникності гломерулярного фільтра для білків плазми крові.
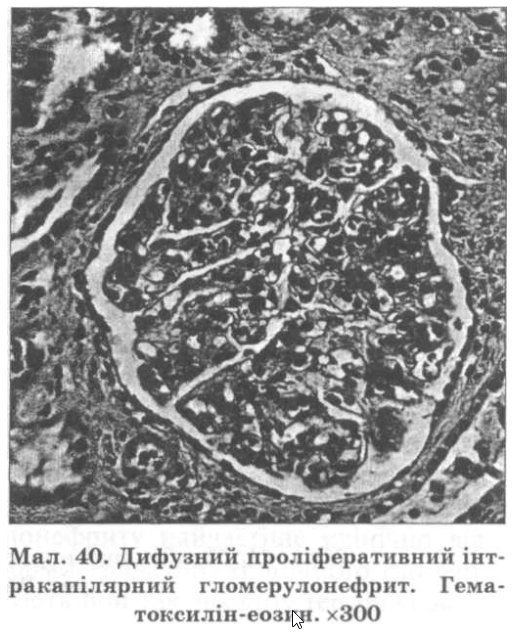
Проліферативний інтракапілярний гломерулонефрит (мал. 40). Характеризується вираженою проліферацією клітин ендотелію і мезангія при порівняно незначних змінах базальної мембрани клубочків. Цей морфологічний тип гломерулонефриту можна визначити при різних клінічних формах хронічного гломерулонефриту.
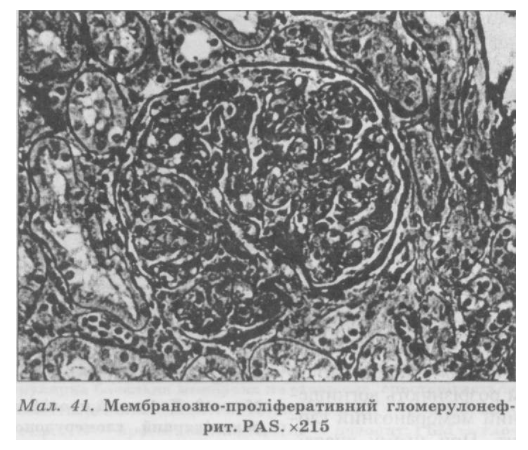
Мезангіокапілярний (мембранозно-проліферативний) гломерулонефрит (мал. 41) характеризується вираженою проліферацією клітин мезангія та особливо його матриксу, більшою чи меншою інфільтрацією моноцитами, внаслідок чого петлі капілярів стиснуті, їхні просвіти звужені і клубочки здаються поділеними на частки. При електронній мікроскопії в мезангіальній ділянці і під ендотелієм виявляють відкладення електроннощільного матеріалу. Виділяють 3 типи мезангіокапілярного нефриту. При І типі (класичному, або субендотеліальному) проліферація мезангія різко виражена з поширенням його матриксу на стінку капілярів під ендотелієм, що створює враження другого контуру або розщеплення базальної мембрани. При електронній мікроскопії під ендотелієм видно великі депозити. Для II типу захворювання характерні електроннощільні відкладення всередині lamina densa різко стовщеної базальної мембрани всіх капілярів. Проліферація мезангія менш виражена.
III тип — мішаний — проліферативний і мембранозний (ближче до І типу). Клінічно він найчастіше проявляється латентною формою гломерулонефриту.
Мезангіопроліферативному хронічному гломерулонефриту властива дифузна проліферація клітин мезангія клубочків і збільшення мезангіального матриксу, а також стовщення і розщеплення базальної мембрани капілярів. У ньому, а іноді і вздовж базальних мембран, найчастіше субепітеліально, відкладаються імуноглобуліни М, G та фракції комплементу С3. Нерідко із імуноглобулінів виявляють тільки імуноглобулін А, що властиве для так званої імуноглобулін-А-гломерулопатії, або хвороби Берже.
У разі фокально-сегментарного гломерулосклерозу склеротичні зміни відзначають тільки в частині клубочків — менше ніж у 80% (фокальний склероз), при цьому уражається не весь клубочок, а тільки якась його частина (сегментарний склероз). Процес починається з кистаме- дулярних клубочків, а потім поширюється на кортикальні. Склерозовані сегменти спаяні з капсулою клубочка. Під час імунофлуоресцентного дослідження в зоні склерозу та субепітеліально знаходять відкладення імуноглобуліну М та фракції комплементу С3. Базальна мембрана вогнища стовщена.
Проліферативний екстракапілярний гломерулонефрит. Характеризується наявністю півмісяців, які формуються внаслідок проліферації клітин епітелію капсули клубочка і заповнення просвіту капсули. При цьому стискуються капілярні петлі клубочка, що призводить до порушення в них кровообігу. Водночас відзначають ексудативні явища і випадання фібрину в порожнину капсули клубочка. Надалі клітини півмісяців зазнають фібропластичних змін з розвитком сполучної тканини і загибеллю клубочка. Екстракапілярний нефрит характеризується несприятливим перебігом.
Фібропластичний (склерозивний) гломерулонефрит — це фінал еволюції багатьох морфологічних типів гломерулонефриту, коли спостерігають запустіння клубочків і розвиток їх гіалінозу. За допомогою світлової мікроскопії виділяють два варіанти: 1) мембранозно-фібропластичний зі склерозуванням базальних мембран, спайками між капілярами і внутрішньою частиною капсули; 2) проліферативно-фібропластичний зі склерозом капілярних петель і, меншою мірою, базальних мембран, спайками в просвіті капсули з утворенням у ній в окремих клубочках фіброепітеліальних та фіброзних півмісяців. У канальцях спостерігають різного ступеня вираженості дистрофічні та атрофічні зміни. За поширенням морфологічних змін розрізняють дифузний і вогнищевий фібропластичний гломерулонефрит.
Головними ознаками дифузного фібропластичного гломерулонефриту є дифузний склероз мезангія, судинних петель клубочків з розвитком гіалінозу і склерозу, з утворенням множинних зрощень між петлями клубочкових капілярів і листками капсули клубочка. При вогнищевому фібропластичному гломерулонефриті названі патологічні зміни виявляють лише в невеликій частині клубочків. Фібропластичному гломерулонефриту найчастіше клінічно відповідають нефротична і гіпертонічна форми тривалого хронічного гломерулонефриту, і, як правило, його діагностують при так званому термінальному нефриті.
Дослідження біоптатів ниркової тканини, отриманих за допомогою прижиттєвої пункційної біопсії нирок, поряд з переважним ураженням клубочків дає змогу виявити також порушення структури канальців, судин, інтерстиціальної тканини. У канальцях виявляють дистрофічні зміни, які переважно локалізуються в епітелії проксимальних відділів, і атрофічні — найчастіше локалізуються в епітелії дистальних відділів канальців. При цьому спостерігають різні види білкової дистрофії (зерниста, гіаліново-краплинна, вакуольна). Атрофію епітелію канальців найчастіше виявляють у дистальних відділах тих нефронів, в яких клубочки не функціонують унаслідок їх гіалінозу і склерозу. Поряд із загиблими, рубцево-зміненими нефронами розвивається компенсаторна гіпертрофія сусідніх нефронів. У міру прогресування хронічного гломерулонефриту все частіше трапляються так звані агломерулярні нефрони зі склерозованими клубочками; атрофічні процеси в канальцях починають переважати над дистрофічними; усе більше нефронів зазнає фіброзного заміщення, відзначають загибель ниркової паренхіми і врешті-решт розвивається вторинно-зморщена нирка.
В Україні користуються клінічною класифікацією хронічного гломерулонефриту, яка запропонована JI.A. Пирогом (2004), а наведена раніше морфологічна класифікація лише її доповнює.
Клінічна картина
Клінічна картина хронічного гломерулонефриту характеризується великим різноманіттям проявів, що залежать від клінічної форми захворювання, перебігу і стану функції нирок. Однак у всіх випадках хронічного гломерулонефриту відзначають неухильне прогресування захворювання, що призводить до розвитку хронічної ниркової недостатності. Хронічний гломерулонефрит має хвилеподібний характер перебігу, коли періоди ремісії змінюються періодами загострення. При загостренні захворювання в більшості випадків клінічна картина хронічного гломерулонефриту нагадує таку при гострому гломерулонефриті: з’являються набряки, артеріальна гіпертензія (якщо у фазі ремісії вони були відсутні), посилюється сечовий синдром. В інших випадках загострення проявляється лише наростанням протеїнурії, гематурії і циліндрурії. Можна спостерігати, особливо при вираженому загостренні, порушення функції нирок.
У період ремісії клінічні симптоми хронічного гломерулонефриту, як і його перебіг, залежать насамперед від клінічної форми захворювання.
Латентна форма (ізольований сечовий синдром) проявляється лише помірно або незначно вираженим сечовим синдромом за відсутності позаниркових ознак захворювання. Добова протеїнурія в більшості випадків не перевищує 1 г, рідше досягає 2 г (але не перевищує 3 г). При загальному дослідженні сечі вона коливається найчастіше в межах 0,033—1 г/л і рідше досягає 2—3 г/л. Для цієї форми хронічного гломерулонефриту характерні незначна еритроцитурія (5—10, рідше 30—50 еритроцитів у полі зору) і циліндрурія.
Набряки відсутні або іноді відзначають пастозність під очима, рідше — на гомілках. AT тривало і стійко зберігається на нормальному рівні, у зв’язку з чим відсутні клінічні, рентгенологічні та електрокардіографічні ознаки гіпертрофії лівого шлуночка серця і зміни з боку судин очного дна. Поява набряків, підвищення AT і наростання сечового синдрому можливі лише в період загострення захворювання. Функція нирок при латентній формі хронічного гломерулонефриту тривалий час (іноді протягом 20—30 років) залишається нормальною, про що свідчать висока відносна густина сечі як в окремих аналізах, так і в пробі Зимницького, нормальні показники клубочкової фільтрації (80—120 мл/хв), вмісту сечовини і креатиніну в крові.
Під час аналізу сечі виявляють протеїнурію, що не перевищує 3 г на добу, еритроцитурію, циліндрурію (гіалінові, зернисті циліндри). У спектрі уропротеїнів переважають альбуміни. У загальному аналізі крові змін немає. При цьому варіанті хронічного гломерулонефриту спостерігають різні морфологічні зміни — від мінімальних до фібропластичних.
Нефротична форма (нефротичний синдром) трапляється у хворих на хронічний гломерулонефрит рідше, ніж латентна. Найхарактернішими ознаками її є масивна протеїнурія (понад 3,5 г за добу), гіпо- і диспротеїнемія, гіперліпідемія (гіперхолестеринемія) і набряки. Серед цих ознак найістотніше клінічне і діагностичне значення має високий рівень протеїнурії, тоді як, наприклад, набряки можуть бути незначними або відсутніми.
Протеїнурія зазвичай перевищує 3 г/л, часто коливається від 3,3 до 33 г/л, досягаючи в окремих випадках 90 г/л і більше. При цьому добова втрата білка із сечею становить 5—30 г, однак у переважної більшості хворих вона не перевищує 10—15 г. Із сечею екскретуються не тільки альбумінові, а й глобулінові, а іноді і великомолекулярні фракції білка. Унаслідок цього протеїнурія може бути високоселективною, що супроводжується екскрецією лише низькомолекулярних білкових фракцій (альбуміни, пре- і постальбуміни), середньоселективною з екскрецією не тільки альбумінів, а й таких глобулінових фракцій, як а,- і а2- швидкі і (3-глобуліни, і низькоселективною (або неселективною), коли із сечею виділяються практично всі або майже всі білкові фракції, що містяться в сироватці крові, у тому числі і такі великомолекулярні, як у- і а2-повільні глобуліни, гаптоглобіни.
Гіпопротеїнемія, що значною мірою зумовлена великою втратою білка із сечею, може бути різного ступеня вираженості: у переважної більшості хворих вона становить 60 г/л і нижче, нерідко досягаючи 50—40 г/л, а в окремих тяжких випадках — 30 г/л і нижче. Диспротеїнемія проявляється насамперед гіпоальбумінемією, яка коливається від 45 до 36%; при вираженому нефритичному синдромі концентрація альбуміну в крові знижується до 20% і нижче. Поряд із гіпоальбумінемією часто спостерігають гіпогамма-глобулінемію, інколи досить значну; із цим пов’язують зниження захисних сил організму і слабку опірність таких хворих до ендо- і екзогенних інфекцій. Зі зниженням вмісту альбумінів певним чином пов’язана наявність гіперхолестеринемії (гіперліпідемії). Унаслідок вираженої гіперхолестеринемії і гіперліпідемії сироватка крові набуває молочного кольору і нагадує рідину лімфатичної протоки.
Важливою ознакою нефротичної форми хронічного гломерулонефриту є набряки, які в більшості хворих бувають вираженими, поширеними, інколи досягають значного ступеня з розвитком асциту, гідротораксу, гідроперикарду (мал. 45). Часто вони резистентні навіть до потужних діуретиків, тримаються іноді місяцями і роками, періодично то зменшуючись, то знову наростаючи. І тільки з розвитком хронічної ниркової недостатності у зв’язку з поліурією вони починають поступово або швидко зменшуватись і навіть зникати, що іноді створює помилкове уявлення про поліпшення стану хворого, до того ж одночасно знижується і протеїнурія.
Обличчя у хворих із нефротичною формою хронічного гломерулонефриту одутле, на кінцівках, особливо нижніх, у ділянці попереку, передньої стінки живота, на статевих органах з’являються значні набряки тістоподібної консистенції (після натиснення пальцями на гомілках, попереку довго зберігаються заглибини). Шкірні покриви бліді, холодні на дотик, сухі, часто облуплюються.
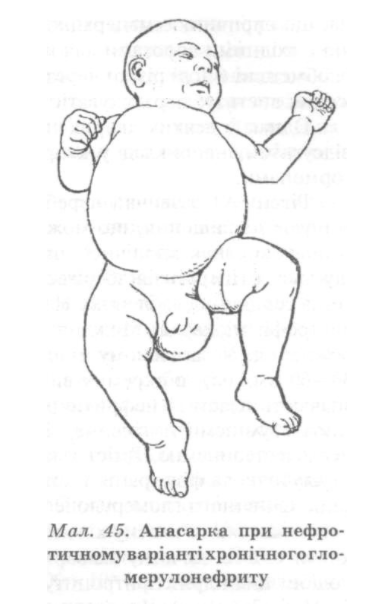
При масивних набряках на шкірі гомілок, стоп, рідше в інших місцях, утворюються тріщини, через які постійно просякає набрякова рідина, що спричинює мацерацію шкірних покривів, а іноді і трофічні виразки, які є вхідними воротами для інфекцій. Хворі трохи загальмовані, мляві, рухи їх обмежені (іноді різко) через великі набряки; скаржаться на слабкість, зниження апетиту, мерзлякуватість.
Однак у деяких хворих набряки можуть бути нерідко вираженими або відсутніми, наприклад у хворих, які лікувалися глюкокортикостероїдними гормонами.
Рівень AT зазвичай перебуває в межах норми, іноді спостерігають його минуще підвищення, що може бути зумовлено загостренням захворювання. З появою ознак хронічної ниркової недостатності рівень AT значно підвищується і гіпертензія зберігається постійно. Пульс стає рідким, а звучність тонів серця — ослабленою. На ЕКГ відзначають зниження вольтажу і ознаки дистрофії міокарда. Можливі диспепсичні явища — нудота, нестійкі випорожнення. У загальному аналізі крові спостерігають збільшення ШОЕ (до 30—60 мм/год), в окремих випадках — невелику нормохромну анемію. Відзначають властиві нефритичному синдрому гіподиспротеїнемію за рахунок гіпоальбумінемії та гіпер-а2- і у-глобулінемії, частіше відносної, а також гіперхолестеринемію. Вміст у крові сечовини, залишкового азоту, креатиніну та клубочкова фільтрація і концентраційна функція нирок у період компенсації хронічного гломерулонефриту перебувають у межах норми. У сечі крім білка виявляють значну кількість циліндрів, особливо гіалінових, які трапляються вже на початку захворювання, пізніше з’являються зернисті і воско- подібні циліндри. Еритроцитурія відсутня або незначна (від поодиноких до 5—15 в полі зору). Частіше, ніж у хворих із сечовим синдромом, виявляють лейкоцитурію, пов’язану як зі змінами інтерстиціальної тканини, так і з приєднанням пієлонефриту (до 8—10% випадків).
При хронічному гломерулонефриті з нефротичним синдромом морфологічно переважають фібропластичні зміни, які поєднуються з мембранозними і мезангіокапілярними. Часто відзначають також мінімальні зміни в клубочках і фокально-сегментарний гломерулосклероз.
У разі приєднання артеріальної гіпертензії виявляють характерні ознаки нефритичного синдрому (масивна протеїнурія, гіпо- і диспротеїнемія, гіпер-холестеринемія і набряки) і гіпертензії (високий рівень AT, зміна судин очного дна, гіпертрофія лівого шлуночка серця та ін.). На очному дні виявляють різного ступеня вираженості ознаки гіпертонічної ретинопатії.
У цій стадії хронічного гломерулонефриту спостерігають різні варіанти морфологічних змін клубочків, але переважають мезангіокапілярний і фібропластичний. Значна частина клубочків не функціонує, решта — гіпертрофовані. Відзначають помітні зміни ниркових артеріол, аж до фібриноїдного некрозу в термінальній стадії.
При всіх клінічних типах хронічного гломерулонефриту можна спостерігати гематурійний компонент — гематурія (сеча кольору м’ясних помиїв) або значна еритроцитурія, коли кількість еритроцитів у сечі перевищує 20 у полі зору, становить 5 • 103 у пробі Нечипоренка або 50 млн на добу в пробі Каковського—Адціса. Появі гематурії часто передують ангіна, гострі респіраторні захворювання, харчові токсикоінфекції, переохолодження, фізичне перенапруження. Еритроцитурію виявляють переважно під час випадкового дослідження сечі, що іноді супроводжується тупим болем у поперековій ділянці. Тривалість гематурії може бути різною — від 1 до 50 днів. Якщо вона велика, то іноді може супроводжуватися дизурійними явищами, зумовленими проходженням згустків крові.
У хворих на хронічний гломерулонефрит із нефротичним синдромом ге- матурійний компонент спостерігають рідко, але за наявності його хронічна ниркова недостатність розвивається відносно пізно — через 7—8 років від початку захворювання або й пізніше. До її виникнення виражене підвищення AT не характерне. Під час морфологічного дослідження ниркових біо- птатів можна виявити всі морфологічні варіанти хронічного гломерулонефриту, але найчастіше (до 86% випадків) трапляється мезангіопроліферативний. Рідше виявляють мембранозний тип і мінімальні зміни клубочків.
Порівняно рідко у дорослих хворих на хронічний гломерулонефрит діагностують первинний гематурійний синдром, який характеризується значною і стійкою гематурією за відсутності набряків, артеріальної гіпертензії і невисокою протеїнурією. Гематурія може іноді досягати значного ступеня і стає помітною макроскопічно (макрогематурія). Однак частіше її виявляють мікроскопічно, коли число еритроцитів у полі зору становить 100 і більше або коли еритроцити більш-менш густо вкривають усі поля зору. Добова екскреція еритроцитів із сечею становить 50—100 • 10б на добу, досягаючи 300—500 • 106 на добу і більше. Протеїнурія ж не перевищує 1 г/л (або 1 г за добу), коливаючись зазвичай у межах 0,033—0,099 г/л, рідше — до 0,99 г/л.
Однак діагноз первинного гематурійного синдрому при хронічному гломерулонефриті установлюють лише в тих випадках, коли виключені всі інші захворювання, які можуть бути причиною гематурії (наприклад, пухлини нирок, сечового міхура, поліпи сечового міхура, сечокам’яна хвороба та ін.).
Мезангіопроліферативний гломерулонефрит характеризується дифузним відкладанням у мезангії імуноглобулінів А, часто разом з імуноглобулінами комплементу С3. Імуноглобулін-А-гломерулопатія (хвороба Берже) — самостійне захворювання, що досить поширене в деяких країнах (Японія, Франція, Італія, Іспанія), де на його частку припадає 20—40% випадків гломерулонефриту. Часте поєднання хвороби Берже з антигенами HLA BW35, HLA DR4 свідчить про роль генетичних чинників у його виникненні. Хворіють переважно молоді чоловіки. Описано два варіанти перебігу цього захворювання. У хворих з першим варіантом мікрогематурію виявляють під час випадкового дослідження сечі і на цьому тлі макрогематурія з’являється рідко.
Другий варіант захворювання розпочинається з появи макрогематурії, що періодично повторюється. Інтервали між окремими епізодами макрогематурії коливаються в широких межах — від 1—2 міс. до кількох років, а їхня кількість варіює від 1 до 15. Поява таких епізодів часто пов’язана з інтеркурентною інфекцією, переважно з ураженням слизових оболонок верхніх дихальних шляхів або з фізичним перенапруженням. Протеїнурія та позаниркові прояви — набряки і артеріальна гіпертензія — виражені більше при першому варіанті, тоді як при другому вони незначні або їх може не бути. У 30—50% хворих у сироватці крові підвищується концентрація імуноглобуліну А. Депозити цього імуноглобуліну виявляють не тільки в мезангії клубочків, а й у стінках капілярів шкіри, що можна використовувати для підтвердження діагнозу.
Діагноз хронічного гломерулонефриту ґрунтується на: 1) стійких змінах сечі за типом сечового або нефротичного синдрому з гломерулярною еритроцитурією та циліндрурією; 2) результатах функціонального дослідження нирок — зниженні клубочкової фільтрації та симетричному порушенні секреторно-екскреторної функції обох нирок, які однаково зменшуються в розмірах, про що свідчать дані радіонуклідної ренографії, УЗД, рентгенологічних досліджень. У частини хворих спостерігають артеріальну гіпертензію. Установити діагноз допомагає наявність в анамнезі даних про перенесений гломерулонефрит або виявлення під час ретельного аналізу медичної документації минущих змін у сечі у зв’язку з гострими респіраторними захворюваннями, ангіною, загостренням тонзиліту. Для підтвердження діагнозу і визначення морфологічної форми захворювання проводять пункційну біопсію нирки.
Перебіг і ускладнення. Загальним для всіх варіантів хронічного гломерулонефриту є неухильний прогресивний перебіг з розвитком хронічної ниркової недостатності. Перебіг хронічного гломерулонефриту у хворих віком понад 40 років значно тяжчий, ніж у молодих, особливо тоді, коли він переходить у гіпертензійну стадію. Однак з віком зменшуються частота і вираженість нефротичного синдрому. Часті ангіни, простудні захворювання, гострі катари верхніх дихальних шляхів, часті загострення хронічної інфекції, особливо тонзиліту, спричинюючи загострення гломерулонефриту, прискорюють його прогресування.
В окремих хворих хронічний гломерулонефрит прогресує швидко уже через 10—14 міс., а іноді і раніше розвивається хронічна ниркова недостатність, що нагадує перебіг гломерулонефриту, який швидко прогресує, з півмісяцями. При цьому захворювання може розпочинатися з гострого нефритичного синдрому або розвивається поступово. У деяких хворих виникає нефритичний синдром. Морфологічні зміни в нирковій тканині локалізуються переважно інтракапілярно і відповідають морфологічному варіанту гломерулонефриту зі швидкою трансформацією (протягом 2 років) у фібропластичний (склерозивний). Можливе приєднання екстракапілярної проліферації з утворенням півмісяців. На відміну від екстракапілярного гломерулонефриту кількість півмісяців невелика — їх виявляють у 50% усіх клубочків, а морфологічні зміни в них мають різний ступінь зрілості, що свідчить про неодночасне залучення клубочків до патологічного процесу.
Диференціальну діагностику хронічного гломерулонефриту проводять у рамках диференціації синдромів — сечового, нефритичного та гіпертензійного.
При типовій клінічній картині і клініко-лабораторних проявах, наявності в анамнезі даних про гострий гломерулонефрит діагноз хронічного гломерулонефриту встановити нескладно. Однак у багатьох випадках, особливо в разі моносимптомного або латентного перебігу захворювання і відсутності в анамнезі інформації про гострий гломерулонефрит, діагностика хронічного гломерулонефриту може бути пов’язана зі значними труднощами. У подібних випадках для уточнення діагнозу доводиться використовувати весь комплекс сучасних клініко-лабораторних, рентгенологічних та інших методів дослідження, аж до прижиттєвої пункційної біопсії нирок.
Загострення хронічного гломерулонефриту із наявністю не тільки сечового синдрому, а й позаниркових ознак захворювання (набряки і артеріальна гіпертензія), а також уперше виявлений хронічний гломерулонефрит з ізольованим сечовим синдромом можуть бути прийняті насамперед за гострий гломерулонефрит. У подібних випадках вирішальне значення в диференціальній діагностиці мають ретельно зібраний анамнез та вивчення наявної медичної документації. Біль в анамнезі може свідчити про перенесені в минулому гострий гломерулонефрит або нефропатію вагітних. Якщо в медичній документації збереглися аналізи сечі за минулі роки і в них виявляли навіть незначні протеїнурію і гематурію, особливо в поєднанні з підвищенням AT, то це свідчить про хронічний перебіг гломерулонефриту.
Про хронічний гломерулонефрит свідчать також зниження клубочкової фільтрації, концентраційної здатності нирок (відносної густини сечі як в окремих аналізах, так і в пробах за Зимницьким та із сухоїдінням), підвищення в крові рівня сечовини, креатиніну. У хворих на гострий гломерулонефрит також можливе незначне і минуще зниження клубочкової фільтрації з невеликою гіперазотемією, але лише в разі бурхливого перебігу захворювання — з вираженої олігурією, артеріальною гіпертензією і набряками. У деяких випадках тільки тривале спостереження за хворим у динаміці дає змогу правильно встановити діагноз.
Частою причиною виникнення сечового синдрому є хронічний пієлонефрит, з яким потрібно диференціювати хронічний гломерулонефрит (табл. 14).
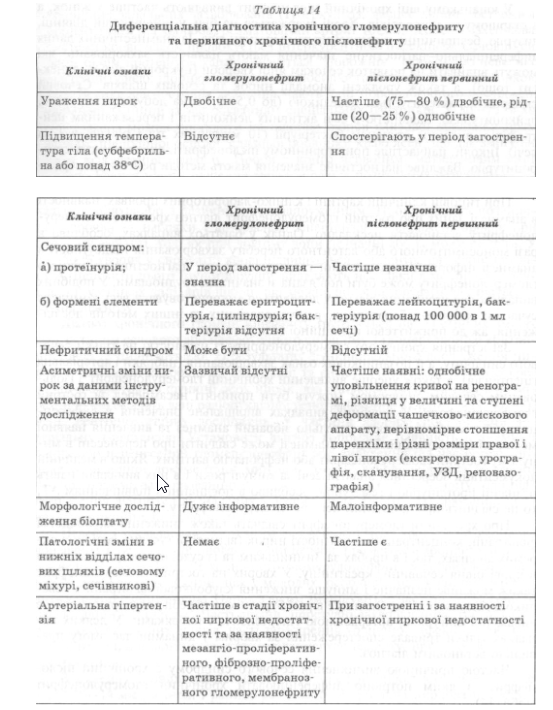
У юнацькому віці хронічний пієлонефрит виявляють частіше у жінок, а в старшому — у чоловіків. Хворі скаржаться на біль у поперековій ділянці, дизурію, безпричинне підвищення температури тіла. Із анамнестичних даних диференціально-діагностичне значення мають наявність захворювань, які можуть впливати на розвиток сечокам’яної хвороби (цукровий діабет, аднексит тощо), а також уроджені аномалії нирок та сечових шляхів. Сечовий синдром характеризується невеликою (до 0,5—0,7 г на добу) протеїнурією, лейкоцитурією, наявністю в сечі активних лейкоцитів і переважанням нейтрофілів, високим ступенем бактеріурії (10 мікробних тіл і більше в 1 мл сечі). Інколи, найчастіше при вторинному пієлонефриті, спостерігають еритроцитурію. Важливе діагностичне значення мають методи рентгеноконтрастного дослідження (екскреторна та інфузна урографія тощо) та УЗД. Певну роль у диференціальній діагностиці відіграють радіонуклідні дослідження (асиметрія ренограм, нерівномірне "заштрихування" сканограм). Морфологічне дослідження ниркової тканини має значення тільки в разі позитивних результатів.
Нерідко гіпертонічна форма хронічного гломерулонефриту неправильно розцінюється як гіпертензійна хвороба через труднощі диференціальної діагностики цих двох різних захворювань, особливо в їхній термінальній стадії і за відсутності даних про тривале спостереження за хворим та аналізів сечі. Про гіпертензійну хворобу можна думати в тих випадках, коли артеріальна гіпертензія за багато років передувала розвитку сечового синдрому і набряків, які в таких хворих зазвичай є наслідком серцевої недостатності. При хронічному гломерулонефриті, навпаки, протеїнурія і гематурія, а також набряки найчастіше передують розвитку артеріальної гіпертензії за багато років або із самого початку поєднуються з підвищенням AT. Крім того, у більшості хворих на хронічний гломерулонефрит сечовий синдром більше виражений, ніж при гіпертензійній хворобі. Рівень AT у хворих на гіпертензійну хворобу порівняно з хронічним гломерулонефритом вищий, зміни з боку серця, судин очного дна і головного мозку більше виражені, гіпертонічний криз, ішемічна хвороба у вигляді стенокардії та інфаркту міокарда трапляються частіше. При гіпертензійній хворобі нирковий плазмоток знижується раніше, ніж величина клубочкової фільтрації, а при хронічному гломерулонефриті, навпаки, раніше зменшується кліренс ендогенного креатиніну.
У деяких хворих правильний діагноз можна встановити тільки на підставі даних прижиттєвої пункційної біопсії нирок.
Для диференціальної діагностики хронічного гломерулонефриту і реноваскулярної гіпертензії, артеріальної гіпертензії при коарктації аорти, феохромоцитомі й альдостеромі (синдром Конна), при синдромі і хворобі Іценка—Кушінга використовують аортографію, ангіографію судин нирок і надниркових залоз, УЗД, рентгенологічні методи дослідження, комп’ютерну томографію, а також визначають у крові та сечі катехоламіни і продукти їхнього обміну (при феохромоцитомі).
Вторинний амілоїдоз нирок (протеїнурійна стадія) найчастіше спостерігають у чоловіків, переважно у віці після 40 років. Він виникає через наявність хронічних запальних захворювань (туберкульоз, абсцес легень, остеомієліт, бронхоектатична хвороба, ревматоїдний артрит тощо), рідше — захворювань системи крові, часом провокується інтеркурентною інфекцією. Сечовий синдром окрім протеїнурії характеризується "порожнім" осадом або невеликою еритроцитурією, що проявляється або посилюється в разі тромбозу ниркових вен. Велике діагностичне значення мають дані морфологічного дослідження ниркової тканини із застосуванням спеціальних барвників. У 50—70% хворих діагноз можна поставити на підставі біопсії слизової оболонки прямої кишки, підшкірної основи, слизової оболонки краю ясен, що дає змогу виявити відкладення амілоїду. Проби з конго червоним, метиленовим синім, синню Еванса мають значення тільки в разі їх позитивних результатів.
Нефропатії при системних захворюваннях сполучної тканини (системний червоний вовчак, ревматична гарячка, вузликовий періартерит та ін.) проявляються насамперед сечовим синдромом і часто виникають на тлі змін інших органів і систем (шкіри, суглобів, серця).
На системний червоний вовчак частіше хворіють молоді жінки, а на вузликовий періартерит — чоловіки віком понад 40—50 років. У сечовому осаді превалюють лімфоцити, циліндри, іноді еритроцити. Виявляють збільшену ШОЕ, при системному червоному вовчаку — також лейкопенію, антинуклеарні антитіла, LE-клітини. Певне диференціально-діагностичне значення має морфологічне дослідження ниркової тканини, одержаної під час пункційної біопсії. В окремих випадках з діагностичною метою проводять біопсію шкіри, лімфатичних вузлів, м’язів.
Діабетичний гломерулосклероз (початкова стадія) частіше виникає у жінок, переважно у віці понад 40 років. Паралельно з розвитком діабетичного гломерулосклерозу знижується глікемія, зменшується або зникає глюкозурія. Для встановлення діагнозу велике значення має виявлення діабетичної ретинопатії, а також морфологічне дослідження ниркової тканини. Діагноз стає більше переконливим, якщо виявляють ознаки системної мікроангіопатії, зокрема ретинопатії з мікроаневризмами і крапковими крововиливами на очному дні, а також симптоми поліневриту. Непрямим підтвердженням гломерулосклерозу є поступове зниження глікемії і глюкозурії без збільшення (або навіть при зменшенні) дози глюкозознижувальних препаратів. Остаточний діагноз хронічного гломерулонефриту або діабетичного гломерулосклерозу встановлюють на підставі даних пункційної біопсії нирок.
Нефропатія вагітних зазвичай розвивається в другій половині вагітності і проявляється тільки помірно вираженим сечовим синдромом або (частіше) ще й набряками і артеріальною гіпертензією. Якщо ці патологічні ознаки виникли вперше і зникають після пологів або переривання вагітності, то їх варто розцінювати як прояв нефропатії вагітних. В інших випадках зміни в сечі (протеїнурія, гематурія, циліндрурія), а іноді набряки і артеріальна гіпертензія зберігаються протягом багатьох років після закінчення вагітності. Такий результат дає підставу думати або про трансформацію нефропатії вагітних у хронічний гломерулонефрит або, що буває частіше, про наявний раніше вчасно не діагностований хронічний гломерулонефрит, загострення якого настало під час вагітності.
Сечокам’яну хворобу нерідко спостерігають у членів однієї родини в різних поколіннях. Вона часто проявляється дизурійними явищами, нападоподібним болем у поперековій ділянці. Іноді змінюється забарвлення сечі (молочно-біла, цегляно-червона, каламутна), відходять конкременти. Сечовий синдром характеризується незначною протеїнурією (0,1—0,3 г на добу), еритроцитурією та білково-еритроцитарною дисоціацією. Важливе діагностичне значення мають дані рентгенологічного дослідження та ультразвукового дослідження нирок, що дають змогу виявити прямі або непрямі ознаки захворювання.
Туберкульоз нирок зазвичай виникає на тлі туберкульозного ураження інших органів (легень, придатків матки тощо). В анамнезі таких хворих, як правило, є вказівки на ознаки туберкульозної інтоксикації (субфебрилітет, слабкість, пітливість тощо), дизурійні явища, біль у поперековій ділянці. Сечовий синдром характеризується переважанням лейкоцитурії і меншою мірою — еритроцитурії над незначною протеїнурією. Під час бактеріоскопіч- ного дослідження сечі мікобактерії туберкульозу виявляють не завжди, тому потрібний посів сечі на спеціальні середовища, біологічна проба на гвінейських свинках. Провідне діагностичне значення мають УЗД, сканування та рентгенологічне дослідження нирок, за допомогою яких виявляють зміни форми та розмір ураженої нирки, її порожнинних відділів, а також вогнища деструкції.
Пухлини нирок спостерігають у різні вікові періоди, але найчастіше — у чоловіків віком після 50 років. Поряд з різними скаргами (біль у поперековій ділянці, субфебрилітет, схуднення, слабкість тощо) у них з’являється протеїнурія, гематурія. Найчастіше — це згустки крові. Інколи в сечовому осаді після спеціального оброблення виявляють пухлинні клітини. У діагностиці пухлин нирок вирішальну роль відіграють методи ультразвукового та рентгенологічного досліджень (екскреторна та інфузна урографія, комп’ютерна томографія, селективна ангіографія тощо), а також радіонуклідне сканування, що дає змогу виявити пухлину навіть невеликих розмірів, та ядерно-магнітно-резонансне дослідження.
Нефронтоз трапляється переважно у молодих жінок. До чинників виникнення захворювання належить швидке схуднення. Хворі часто скаржаться на біль у поперековій ділянці, що посилюється під час ходьби, тряської їзди, підняття тягарів, та дизурійні явища. Під час пальпації живота нерідко вдається пальпувати рухому нирку. Сечовий синдром характеризується невеликою протеїнурією (0,2—0,3 г на добу) та еритроцитурією, вираженість яких збільшується після пальпації нирки та фізичного навантаження. Остаточний діагноз встановлюють після ультразвукового та рентгенологічного дослідження з виконанням знімків у горизонтальному і вертикальному положеннях хворого. Оскільки гіри нефроптозі може бути і гломерулонефрит, у сумнівних випадках слід проводити біопсію нирки. У разі різко вираженого нефроптозу можна спостерігати артеріальну гіпертензію, що часто виникає після переведення хворого з горизонтального положення у вертикальне.
Подагрична нефропатія зазвичай виникає на тлі специфічних змін суглобів, але може бути і першим проявом захворювання, яке найчастіше спостерігають у чоловіків старших вікових категорій. Хворі скаржаться на біль у поперековій ділянці, дизурійні явища. На ранніх стадіях характерні стійка або переміжна протеїнурія та уратурія, невелика кількість еритроцитів, лейкоцитів, циліндрів. Якщо є конкременти, еритроцитурія більше виражена. Характерні різке зниження відносної густини сечі, анемія, гіперуремія. Діагноз подагри встановлюють на підставі типових нападів болю в суглобах з ураженням І плесно-фалангового суглоба або не менш ніж двох інших суглобів, тофусів, підвищення рівня сечової кислоти в крові, виявлення кристалів уратів і сечової кислоти в синовіальній рідині або тканинах.
Мієломна нефропатія може бути дебютом захворювання або з’явитися на тлі інших проявів хвороби. Її переважно спостерігають у чоловіків літнього віку. Поряд із сечовим синдромом, що буває рідше, ніж нефритичний, постійно відзначають анемію, різко збільшену ШОЕ, можна виявити плазматичні клітини в периферійній крові, специфічні зміни мієлограми і кісткової системи. Властиві гіперпротеїнемія, гіпергаммаглобулінемія, гіперкальціємія, поява парапротеїнів. У третини хворих у сечі виявляють альбумін Бенса— Джонса.
"Серцева, або застійна, нирка" характеризується появою сечового синдрому (протеїнурії, циліндрурії, іноді невеликої еритроцитурії) внаслідок зменшення ниркового кровотоку, зумовленого тяжкою недостатністю кровообігу різного генезу; клубочкова фільтрація знижена, виділення Na+ та Сl зменшене. Інколи протеїнурія може бути значно вираженою (до 3—10 г/л), що за наявності набряків неправильно розцінюється як хронічний гломерулонефрит із нефритичним синдромом. При застійній протеїнурії на відміну від нефритичної форми хронічного гломерулонефриту набряки розташовуються переважно на гомілках, попереку і відсутні на обличчі, немає гіперхолестеринемії, не завжди відзначають гіпопротеїнемію. Основною диференціально-діагностичною ознакою є зменшення змін у сечі в міру зниження ознак недостатності кровообігу. Однак слід пам’ятати, що "серцева нирка" може поєднуватися з гломерулонефритом.
Для підгострого бактеріального ендокардиту характерні протеїнурія, гематурія і циліндрурія як наслідок емболії ниркових судин з розвитком інфаркту нирки або вогнищевого гломеруліту. У деяких хворих розвивається дифузний гломерулонефрит з усіма властивими цьому захворюванню ознаками (іноді з типовим нефритичним синдромом). Він часто набуває хронічного перебігу і зберігається навіть після одужання хворого від бактеріального ендокардиту, що призводить до розвитку хронічної ниркової недостатності.
Бактеріальний ендокардит у більшості випадків розвивається у хворих із набутими або вродженими вадами серця, супроводжується температурною реакцією різного ступеня вираженості, нерідко ознобом і пітливістю. Виявляють збільшення селезінки, рідше печінки, ознаки васкуліту (позитивні симптоми джгута, щипка, Лукіна—Лібмана—Етингера); збільшення ШОЕ, часто лейкоцитоз (хоча можлива і лейкопенія), позитивні формолова проба, реакція Вассерманна; у 50—70% випадків із крові після посіву на поживні середовища висівають мікроб — збудник даного захворювання. Діагноз підгострого бактеріального ендокардиту стає переконливішим, якщо крім перерахованих симптомів з’являються емболії в різних судинних ділянках.
Медикаментозні ураження нирок (медикаментозна нефропатія), так само як і гломерулонефрит, характеризуються протеїнурією і гематурією. На відміну від хронічного гломерулонефриту патологічні зміни в сечі виникають на тлі вживання лікарських препаратів і зникають після відміни їх через різні інтервали часу. При медикаментозному ураженні нирок зазвичай спостерігають і інші ознаки непереносимості лікарських препаратів (шкірна алергійна висипка, частіше у вигляді кропив’янки, набряк Квінке, зміни з боку периферійної крові — лейкопенія, еозинофілія, агранулоцитоз тощо).
Полікістоз нирок крім протеїнурії і гематурії (зазвичай незначно виражених) клінічно проявляється артеріальною гіпертензією, що може досягати високого рівня. Ця вроджена патологія нерідко перебігає під діагнозом хронічного гломерулонефриту. Однак диференціальна діагностика полікістозу нирок і хронічного гломерулонефриту за умови ретельного обстеження хворого не становить великих труднощів. Про полікістоз свідчить виявлене пальпаторно і рентгенологічно значне збільшення розмірів нирок з горбистою нерівною поверхнею. Нині найпростішим і найвірогіднішим методом діагностики полікістозу є УЗД нирок. Ретроградну (висхідну) пієлографію, при якій на урограмі виявляють характерну картину: розсунуті, витягнуті і деформовані чашечки на тлі значного збільшення розмірів нирки (урограма має форму дракона), використовують рідко. На сканограмі відзначають ділянки, в яких не накопичуються радіоактивні речовини і які відповідають порожнинам (кістам). У складних випадках використовують комп’ютерну томографію.
Спадковий нефрит може стати причиною сечового синдрому в дітей, підлітків, юнаків та молодих людей у віці до 20—30 років. У цих випадках головною особливістю сечового синдрому є гематурія, зазвичай переміжного характеру. Протеїнурія не перевищує 0,5—1,5 г на добу, причому протеїнурію, як і еритроцитурію, виявляють не завжди або вона може бути єдиною ознакою захворювання. Іноді виявляють лейкоцитурію, яка в поєднанні з бактеріурією свідчить про приєднання пієлонефриту, часто — гіперамінацидурію. При біопсії тканини нирки в окремих випадках виявляються пінисті клітини, які вважають патогномонічною ознакою вираженого нефриту, зокрема синдром Альпорта. Підтвердити діагноз допомагає також наявність аналогічних захворювань нирок у трьох поколіннях, нерідко такі захворювання пов’язані зі змінами в інших органах і системах.
При встановленні діагнозу хронічного гломерулонефриту потрібно виключити і ймовірність так званої фізіологічної (доброякісної) протеїнурії, до якої належать, зокрема, ортостатична (лордотична) протеїнурія, протеїнурія напруження, або "маршова", і застійна протеїнурія.
У клінічній практиці особливо важливе значення в диференціальній діагностиці надають ортостатичній протеїнурії, яку виявляють у юнацькому віці в осіб високого зросту з вираженим прогином уперед поперекового відділу хребта (лордоз). Цей вид протеїнурії найчастіше доводиться диференціювати з латентною формою хронічного гломерулонефриту. Для цього використовують ортостатичну пробу, сутність якої полягає в наступному: спочатку беруть на дослідження сечу, зібрану після сну (без навантаження), а потім пропонують досліджуваному постояти у вертикальному положенні або на колінах не менше ніж 30 хв. із закладеними за голову (на потилицю) руками або втримуючи протягом зазначеного часу руками на рівні попереку ціпок, закладений за спину. У такому положенні збільшується лордоз, і за наявності ортостатичної протеїнурії в сечі, зібраній після закінчення проби, рівень білка істотно перевищує такий у порції сечі, узятої до проведення проби, в якій білка може взагалі не бути. При хронічному гломерулонефриті подібної динаміки вмісту білка в сечі зазвичай не спостерігають.
У разі феохромоцитоми зміни в нирках проявляються невеликою протеїнурією, наявністю поодиноких гіалинових циліндрів, еритроцитів. Нирковий кровотік і клубочкова фільтрація знижуються, період напіввиведення та час досягнення піку на ренограмі подовжуються, ренограми симетричні. Диференціально-діагностичне значення має кризовий перебіг артеріальної гіпертензії з багатьма вегетативними та метаболічними порушеннями (пітливість, підвищення температури тіла, пронос, глюкозурія, гіперглікемія, гіперлейкоцитоз, тенденція до гіперкаліємії та гіперкальціємія). Однак може відзначатись і стійка висока артеріальна гіпертензія, що значно утруднює розпізнавання захворювання. Для діагностики використовують визначення активності катехоламінів у сечі та інструментальні методи візуалізації пухлини.
При гіперальдостеронізмі (хворобі Конна) виявляють стійку лужну реакцію сечі, гіпоізостенурію, ніктурію, невелику протеїнурію, часом лейкоцитурію. Набряки спостерігають тільки в разі серцевої недостатності. Запідозрити це захворювання допомагають стійкий нейром’язовий синдром (м’язова слабкість, тетанія, парестезія тощо), полідипсія, поліурія, стійка гіпокаліємія, гіперкаліурія, метаболічний алкалоз. Діагноз підтверджується в разі виявлення підвищеної екскреції альдостерону із сечею та візуалізація пухлини надниркової залози під час УЗД, комп’ютерної томографії та сканування нирок і надниркових залоз.
Лікування хронічного гломерулонефриту включає призначення дієти, режиму, застосування методів патогенетичного і симптоматичного впливу.
Режим хворих на хронічний гломерулонефрит поза фазою загострення, незалежно від варіанта і стадії, має бути щадним: хворі повинні уникати важкої фізичної праці, переохолодження, перегрівання, праці в гарячих і холодних цехах, на відкритому повітрі в холодну пору року, у нічну зміну. Обмеження в режимі бувають більшими при нефритичному варіанті та при гіпертензивній стадії захворювання. Купання у відкритих водоймищах припустиме тільки для хворих із сечовим синдромом, якщо немає вітру і температура води становить 22—24°С.
У фазі загострення хронічного гломерулонефриту та при всіх інтеркурентних захворюваннях показаний ліжковий режим.
За наявності варіанта з ізольованим сечовим синдромом у фазі ремісії рекомендують дієту без обмеження рідини, з нормальним вмістом білків, жирів, вуглеводів, багату на вітаміни, солі калію, з деяким обмеженням кухонної солі (до 10 г на добу). Через надмірне обмеження солі і рідини може знизитися об’єм циркулювальної плазми, а внаслідок цього — нирковий кровотік та клубочкова фільтрація; у фазі загострення дещо обмежують споживання білка (до 60—80 г на добу), оскільки велика кількість його прискорює склероз клубочків. Обмежують і споживання кухонної солі (до 7—8 г на добу), під суворим контролем водного балансу визначають необхідну кількість рідини.
Хворі з нефритичним варіантом хронічного гломерулонефриту мають одержувати фізіологічну норму білка з додаванням кількості, що втрачається із сечею. Обмежують споживання кухонної солі (6—7 г на добу), жирів тваринного походження (до 1/3—1/2 добової кількості), а також легкозасвоюваних вуглеводів; їжа має включати білки, що містять незамінні амінокислоти, велику кількість вітамінів, калію, заліза, кобальту. Добова кількість спожитої рідини не повинна перевищувати величину добового діурезу більш як на 400—500 мл, а в разі великих набряків слід домагатися негативного водного балансу.
У гіпертензивній стадії хронічного гломерулонефриту обмежують кількість жирів тваринного походження, легкозасвоюваних вуглеводів, натрію хлориду, рекомендують продукти, багаті на калій, вітаміни. Водний режим залежить від функціонального стану серцево-судинної системи.
У разі потреби обмеження натрію хлориду рекомендують ахлоридний хліб, овочеві страви готують у тушкованому і смаженому вигляді, м’ясні і рибні — смажать і тушкують після попереднього відварювання. Для поліпшення смакових якостей їжі дозволяють у невеликих кількостях цибулю, часник, гірчицю, хрін, кмин, неміцний оцет, сушені кріп, петрушку, журавлину, кислі фруктові та овочеві соки (лимонний, журавлинний, аличевий, гранатовий тощо). Протипоказані продукти, які містять багато кухонної солі та ефірної олії, копченості, гострі сири, соління, свіжі кріп і петрушка, а також кава і какао. Категорично забороняються алкогольні напої.
Загальною рекомендацією для всіх хворих на гломерулонефрит має бути відмова від куріння, що підвищує синтез і виділення ендотеліну-1, різноманітні ефекти якого погіршують перебіг гломерулонефриту (стимулює проліферацію фібробластів інтерстицію, сприяє підтриманню перитибулярної вазоконстрикцїї, підвищує тонус ниркових судин, збільшує продукування інтерлейкіну-1, цитокинів, які активізують проліферацію мезангіальних клітин).
Збільшенню протеїнурії і розвитку гломерулосклерозу сприяє ожиріння, тому слід знижувати масу тіла до ідеальної. Гіперліпідемія різко підвищує у хворих на хронічний гломерулонефрит ризик коронарного атеросклерозу, протеїнурію і ниркову недостатність. При підвищенні рівня ліпідів у сироватці крові показана терапія гіполіпідемічними препаратами (нікотинова кислота; інгібітори ГМК-КоА-редуктази: ловастатин, симвастатин тощо; пробукол, йонообмінні смоли).
Антибактеріальна терапія показана в разі загострення захворювання у зв’язку з перенесеною інфекцією, під час санації вогнищ хронічної інфекції, лікування інтеркурентних інфекцій, під час оперативних втручань, зокрема тонзилектомії, а також у разі поєднання гломеруло- і пієлонефриту. З цією метою застосовують антибіотики, які не мають нефротоксичної дії (пеніцилін, оксацилін, ампіцилін, олеандоміцин, кларитроміцин та ін.), в оптимальних дозах протягом 10—15 днів.
Санація вогнищ інфекції у хворих на хронічний гломерулонефрит включає також хірургічне лікування (екстракція каріозних зубів, тонзилектомія тощо). До тонзилектомії вдаються тільки в разі неефективності консервативного лікування хронічного тонзиліту, схильності його до частих загострень, що супроводжуються посиленнями патологічних змін у сечі, а також під час підготовки хворого до імуносупресивної терапії. Особливо суворо слід підходити до показань щодо тонзилектомії у гіпертензивній стадії захворювання за наявності високої некорегованої артеріальної гіпертензії через небезпеку загострення гломерулонефриту і переходу його в ниркову недостатність, а також у разі вираженого нефритичного синдрому.
Патогенетична терапія при хронічному гломерулонефриті показана у разі його загострення, наявності високої протеїнурії, нефритичного синдрому. Найширше застосовують глюкокортикостероїди, які справляють протизапальну та імуносупресивну дію. Перевагу надають преднізолону або метил-преднізолону (метипреду), оскільки в разі їх застосування рідше і пізніше розвивається синдром Іценка—Кушінга. Преднізолон призначають у початковій добовій дозі 1 мг на 1 кг маси тіла, або 60 мг на 1/2 м2 поверхні тіла, всередину. Розподіляти добову дозу слід так, щоб максимум припадав на ранок, менша доза — на обідній час і найменшу частину вживають увечері. У разі значної активності гломерулонефриту можна застосовувати вищі дози і навіть пульс-терапію (1000 мг метилпреднізолону внутрішньовенно щодня протягом 3 днів).
Після одержання вираженого терапевтичного ефекту і стійкого поліпшення лабораторних показників, насамперед зниження протеїнурії, що найчастіше досягається через 3—4 тиж. вживання глюкокортикостероїдів, їх дозу поступово знижують аж до цілковитої відміни препарату. Курс лікування — від 2 до 6 міс. Іноді підтримувальну дозу — 10—20 мг — уживають протягом 6—18 міс.
У разі тривалого перебігу захворювання (понад 2 роки) для вирішення питання про доцільність призначення патогенетичної терапії бажано уточнити морфологічний варіант гломерулонефриту. На позитивний ефект від глюкокортикостеро’їдів слід очікувати, якщо зміни в клубочках мінімальні — при мембранозному і, рідше, мезангіопроліферативному гломерулонефриті. При мезангіокапілярному нефриті, фокально-сегментарному гломерулосклерозі та фібропластичному нефриті таке лікування є малоефективним.
Протипоказаннями до вживання ГКС є хронічний пієлонефрит, амілоїдоз, паранеопластична нефропатія, діабетична нефропатія, склеродермічна нирка, тромбоз ниркових вен з розвитком нефротичного синдрому.
У випадках стероїдорезистентності та стероїдозалежності, а також у разі неможливості призначення достатньо великих доз глюкокортикостероїдів через протипоказання або погану їх переносимість призначають цитостатичні імуносупресанти: циклофосфамід у добовій дозі 2—3 мг на 1 кг маси тіла, азатіоприн по 1,5—3 мг на 1 кг або хлорбутин (лейкеран) по 0,2—0,3 мг на 1 кг маси тіла. На відміну від глюкокортикостероїдів цитостатичні імуносупресанти можна успішно застосовувати навіть у хворих зі значною давністю захворювання, наявністю нефротичного синдрому, артеріальної гіпертензії та початкових ознак хронічної ниркової недостатності. Лікування проводять під суворим контролем аналізів крові протягом 4—8 тиж. у стаціонарі і в разі ефективності продовжують його в амбулаторних умовах протягом 4—6 міс., використовуючи половинну добову дозу препарату. Якщо кількість лейкоцитів знижується до 3 • 109/л, лікування слід припинити. Для зменшення цитопенічного ефекту цитостатичних імуносупресантів їх варто поєднувати з преднізолоном у невеликих (20 мг на добу), а іноді й у вищих (50—60 мг на добу) дозах.
Застосування антикоагулянтів і дезагрегантів грунтується на важливій ролі внутрішньоклубочкової коагуляції в патогенезі гломерулонефриту. Гепарин (по 20 000—30 000 ОД на добу внутрішньовенно або внутрішньом’язово за 2—4 рази), фраксипарин (підшкірно), дипіридамол (курантил, персантил) по 200—400 мг на добу всередину або ацетилсаліцилову кислоту (250—325 мг одноразово всередину після їди) призначають хворим із нефритичним синдромом або із сечовим синдромом у фазі загострення, особливо в разі раннього переходу захворювання в гіпертензивну стадію (при помірній артеріальній гіпертензії), за наявності вираженої гіперкоагуляції, підвищеної концентрації продуктів деградації фібриногену і фібрину в плазмі крові та сечі, стійких набряках, що не піддаються лікуванню преднізолоном, цитостатичними імуносупресантами і сечогінними засобами. Призначення антикоагулянтів і дезагрегантів можна поєднати з терапією глюкокортикостероїдами та імуносупресантами. Як дезагреганти використовують також пентоксифілін (0,2—0,3 г на добу), тиклопідин (0,25 г 2 рази на добу). Дезагреганти призначають протягом 2—6 міс. і довше.
У разі вираженої активності нефриту буває ефективним плазмаферез, особливо у хворих із системними захворюваннями сполучної тканини.
Терапію хронічного гломерулонефриту можна проводити селективними імунодепресантами (циклоспорин А, мікофенолат-мофетил).
Вплив циклоспорину А на імунну відповідь зумовлений пригніченням як активності Т-хелперів, так і продукування інтерлейкіну-2, проліферації цитотоксичних Т-клітин, а також побічно (через пригнічення Т-клітин) активізації В-клітин. Препарат показаний при частих рецидивах нефротичного синдрому або стероїдорезистентному нефротичному синдромі, розвитку ускладнень стероїдної і цитостатичної терапії. Початкова доза циклоспорину А для дорослих становить 5 мг на 1 кг маси тіла. Зниження протеїнурії спостерігають протягом 1—3 міс. У подальшому дозу ГКС доцільно знизити до 30— 40 мг на добу.
До побічних ефектів дії циклоспорину А відносять нефротоксичність, артеріальну гіпертензію, гіпертрофію ясен, гіпертрихоз, гепатотоксичність, залежність від препарату.
Мікофенолат-мофетил (інгібітор інозинмонофосфатдегідрогенази, що виснажує запаси гуанозинових нуклеотидів у клітині) селективно інгібує проліферацію Т- і В-лімфоцитів, продукування антитіл та утворення цитотоксичних Т-лімфоцитів. Препарат призначають по 0,5 г 2 рази на день.
Для лікування хворих на хронічний гломерулонефрит застосовують препарати 4-амінохінолінового ряду (резохін, делагіл, хлорохін, плаквеніл), які за механізмом своєї дії близькі до імунодепресантів. В умовах стаціонару ці препарати призначають у дозі 0,5—0,75 г на добу протягом 3—6 тиж., а потім у підтримувальних дозах (0,25 г) протягом кількох місяців або навіть років. Однак у разі тривалого їх застосування можливі побічні явища (посилення гематурії, диспепсичні явища, дерматит, порушення зору, депігментація волосся, пригнічення гемопоезу), що обмежує їх застосування.
Хворих на хронічний гломерулонефрит із мінімальною активністю лікують також НПЗП (індометацин, вольтарен, ібупрофен та ін.), протизапальна дія яких пов’язана з пригніченням синтезу простагландинів, гальмуванням агрегації тромбоцитів, відкладенням фібрину в клубочкових капілярах і зниженням проникності базальних мембран. Однак під впливом цих препаратів знижуються клубочкова фільтрація, нирковий плазмотік, зменшується екскреція натрію із сечею і підвищується AT.
НПЗП використовують при помірному загостренні гломерулонефриту у хворих із латентною і гематурійною формами, менше показані вони при не- фритичному синдромі та мішаній формі хронічного гломерулонефриту (вміст загального білка в крові не менше ніж 55 г/л, альбумінів — не менше ніж 30 г/л, коли протягом короткого часу бажано знизити протеїнурію або неможливо провести лікування ГКС і цитостатиками). Оптимальна терапевтична доза індометацину (метиндолу) і вольтарену становить 25 мг 4—6 разів на добу протягом 4—8 тиж.; у підтримувальних дозах (50—75 мг) препарати впродовж тривалого часу застосовують амбулаторно.
Можливі побічні дії — головний біль, диспепсичні явища, біль у надчеревній ділянці, утворення шлунково-кишкових виразок, розвиток артеріальної гіпертензії, рідко — катаракта, глаукома.
Хворі на мембранозний гломерулонефрит без нефротичного синдрому зі збереженою функцією нирок не потребують імунодепресивної терапії. Вони мають перебувати під диспансерним спостеріганням для контролю AT, протеїнурії і креатиніну. Якщо протеїнурія перевищує 1,0—2,0 г на добу, показані інгібітори АПФ, а в разі підвищення холестерину — гіполіпідемічні препарати.
У разі мембранозного гломерулонефриту з нефритичним синдромом можна застосовувати альтернувальне вживання великих доз ГКС — по 2 мг на 1 кг маси тіла преднізолону через день протягом приблизно 2 міс. з подальшим зниженням дози або поєднанням глюкокортикостеро’їдів із цитостатичними імуносупресантами — до 6 міс. Ця комбінація особливо ефективна у стероїдорезистентних хворих з початковими явищами хронічної ниркової недостатності.
При гіперліпідемії, яку часто виявляють у хворих на хронічний гломерулонефрит з нефритичним синдромом, призначають гіперліпідемічні препарати: симвастатин, ловастатин, флувастатин у дозі 10—60 мг на добу протягом 4—6 тиж. з подальшим зниженням дози.
У разі імуноглобулін-А-гломерулопатії в більшості випадків достатнім є лише спостереження. Досить рідко спостерігають перебіг, який швидко прогресує. У таких хворих можуть бути ефективними ГКС, зокрема пульс-терапія ГКС або/і цитостатиками.
За умови мезангіокапілярного гломерулонефриту ГКС в альтернувальному режимі (преднізолон у розрахунку 1,5—2 мг на і кг маси тіла всередину через день) ізольовано або в поєднанні з цитостатичними імуносупресантами застосовують, але загалом вони малоефективні і, за деякими даними, можуть прискорити розвиток склерозу в уражених клубочках. Уповільнити його прогресування іноді дає змогу тривале (протягом 1 —3 років) застосування дезагрегантів: ацетилсаліцилової кислоти (0,3—1 г на добу), що пригнічує цикло-оксигеназу, разом з дипіридамолом та інгібітором фосфодіестерази тромбоцитів (по 75—225 мг на добу). Проте ефективність такої терапії ще остаточно не доведена. У разі фібропластичного (склерозованого) гломерулонефриту з майже тотальним склерозом клубочків патогенетична терапія не показана у зв’язку з її неефективністю і навіть імовірністю несприятливого впливу на патологічний процес.
При тяжких формах хронічного гломерулонефриту — мембранозній, проліферативно-мембранозній, а також при екстракапілярному нефриті рекомендують так звану чотирикомпонентну терапію, що складається з комбінації цитостатика, антикоагулянтів, антиагреганта і преднізолону в наведених вище дозах. Лікування триває в оптимальних дозах 6—8 тиж. і більше.
Симптоматична терапія відіграє важливу роль у лікуванні хворих на хронічний гломерулонефрит, її застосовують як монотерапію у хворих без ознак активності процесу, а якщо вони є, її поєднують з патогенетичною. Симптоматичне лікування включає застосування сечогінних, антигіпертен- зивних препаратів і терапію серцевої недостатності.
Сечогінні засоби застосовують при значних набряках у хворих з нефротичним синдромом і/або недостатністю кровообігу. Невеликі набряки можуть минати в разі дотримання ліжкового режиму і дієти. У хворих із нерізко вираженими, але тривалими набряками можна застосовувати рослинні сечогінні засоби: відвар бузини, волошки синьої, астрагалу, листя берези, суниці, брусниці. Тіазидові похідні (гіпотіазид, езидрекс по 25—100 мг одноразово тощо) показані за наявності нефритичного синдрому, особливо в разі артеріальної гіпертензії. У зв’язку з менш вираженою калійуретичною дією широко застосовують фуросемід (лазикс), який призначають як усередину, так і парентерально — від 40—80 до 600 мг на добу. Менш доцільним є застосування етакринової кислоти (урегиту), яка зменшує вторинну рефрактерність щодо інших сечогінних засобів, а також ступінь протеїнурії, але має виражену калійуретичну дію. Препарат призначають усередину, починаючи з 50 мг, у разі потреби підвищуючи дозу до 200 мг на добу.
У хворих з тяжким нефротичним синдромом зі збереженою функцією нирок сечогінний ефект за умови застосування зазначених препаратів часто вдається отримати лише на тлі високобілкової дієти, обмеження споживання кухонної солі, патогенетичної терапії. Нерідко такі заходи доводиться поєднувати з парентеральним уведенням білкових препаратів (плазми крові, альбуміну), що підвищують онкотичний тиск плазми крові, а якщо немає артеріальної гіпертензії, то в комбінації з осмотичними діуретиками (10—20% розчин манітолу з розрахунку 0,5—1 г на 1 кг маси тіла тощо). Якщо у хворого не виявлено хронічної ниркової недостатності, раціональним є поєднання або послідовне застосування перелічених раніше препаратів з антагоністами альдостерону (альдактон А, верошпірон по 75—200 мг на добу за З рази після їди), які справляють також калійзберігальну дію.
За наявності хронічної ниркової недостатності препаратом вибору є фуросемід. У разі набряків, резистентних до всіх видів діуретичної терапії, застосовують гемодіаліз у режимі ультрафільтрації, що дає змогу за одну 2— 3-годинну процедуру видалити до 2—3 л рідини.
Раціональне лікування артеріальної гіпертензії — це значною мірою профілактика прогресування хронічного гломерулонефриту та запобігання розвитку тяжких ускладнень (інсульту, інфаркту міокарда тощо). У гіпертензивній стадії хронічного гломерулонефриту слід прагнути до нормалізації рівня AT під контролем самопочуття хворих.
Виражену пролонговану антигіпертензивну і слабку діуретичну дію має індапамід (арифон, індапрес), який за фармакологічними властивостями близький до тіазидних діуретиків. Антигіпертензивний ефект препарату зберігається у пацієнтів з артеріальною гіпертензією при порушеній функції нирок. Індапамід призначають по 2,5—5 мг усередину 1 раз на добу в ранкові години.
За наявності серцевої недостатності антигіпертензивні та сечогінні препарати поєднують із серцевими глікозидами, широко використовуючи периферійні вазодилятатори, особливо інгібітори АПФ. У тяжких випадках доцільно вдаватися до ультрафільтрації та внутрішньовенного введення неглікозидних інотропних агентів, антагоністів альдостерону.
У хворих з гематурійним компонентом рекомендують призначати мембраностабілізувальні препарати: задитен (кетотифен), делагіл, плаквеніл, унітіол (донатор сульфгідрильних груп).
Як антигіпертензивну терапію застосовують інгібітори АПФ (мають ан- типротеїнурійну і нефропротекторну дію, тому що, сповільнюючи внутрішньоклубочкову гіперфільтрацію і гіпертензію, уповільнюють темпи прогресування хронічної ниркової недостатності): каптоприл по 50—100 мг на добу, еналаприл по 10—20 мг на добу, раміприл по 2,5—10 мг на добу; блокатори кальцієвих каналів: верапаміл у дозі 120—320 мг на добу, дилтіазем у дозі 160—360 мг на добу, ісрадипін та ін.
Лікування хронічного гломерулонефриту у хворих із хронічною нирковою недостатністю — симптоматичне.
Санаторно-курортне лікування хворих на хронічний гломерулонефрит рекомендують багато клініцистів. Позитивний вплив жаркого і сухого клімату на перебіг цього захворювання ґрунтується на зниженні його активності, поліпшенні показників функціонального стану нирок, водно-електролітного і білкового обміну. Хворих з ізольованим сечовим синдромом і початковою артеріальною гіпертензією, а також із нетяжким нефритичним синдромом у період ремісії можна лікувати на курорті Байрам-Алі.
Поліпшення перебігу гломерулонефриту з ізольованим сечовим синдромом і невеликою артеріальною гіпертензією (не вище ніж 170/100 мм рт. ст.) спостерігають після санаторного лікування в умовах Південного берега Криму. Тут можна лікувати також початковий, неповний нефритичний синдром за умови застосування дозованої аерогідротерапїї в спеціальному павільйоні.
Санаторно-кліматичне лікування протипоказане в разі різко вираженого нефритичного синдрому з явищами загальної дистрофії, стійкими великими набряками, слабкістю, з високою артеріальною гіпертензією та явною серцевою недостатністю, а також у разі ускладнення захворювання хронічною нирковою недостатністю (навіть початковою) та розладами мозкового кровообігу.
Прогноз
Прогноз при хронічному гломерулонефриті залежить від віку хворого, клінічного варіанта і стадії захворювання. З усіх клінічних форм хронічного гломерулонефриту латентна форма, особливо в дітей і юнаків, найбільш прогностично сприятлива: компенсація ниркових функцій і працездатність хворих при дотриманні профілактичних заходів зберігаються протягом багатьох років і навіть десятиліть. Оскільки ця форма хронічного гломерулонефриту трапляється найчастіше, своєчасне виявлення таких хворих, правильне їх працевлаштування і диспансерне спостерігання за ними мають важливе практичне значення. З віком у разі частих загострень хронічних вогнищ інфекції, а також у хворих із нефритичним варіантом, особливо за наявності гематурії, прогноз погіршується. В ангіпертензивній стадії він кращий, ніж у гіпертензивній. Особливо обтяжують прогноз такі ускладнення, як артеріальна гіпертензія та нефритичний синдром. Тривалість життя хворих при цьому становить 3—5, максимум 8 років. Однак завдяки ретельному і наполегливому лікуванню, правильному працевлаштуванню хворих в окремих випадках можна домогтися продовження життя. Алергійні реакції і "нашарування" пієлонефриту також негативно позначаються на перебігу захворювання.
Прогресивний перебіг захворювання частіше спостерігають при високій протеїнурії, особливо неселективній, і поєднанні її з гематурією. Прогностично несприятливими є порушення функціонального стану нирок — зменшення величини клубочкової фільтрації, порушення добового ритму діурезу тощо.
Менш сприятливим, але все-таки порівняно повільним перебігом і тривалим періодом компенсації функцій нирок характеризуються проліферативний, мембранозний і проліферативно-мембранозний типи гломерулонефриту. Найбільш несприятливі за перебігом і прогнозом — проліферативно-фібропластичний і особливо фібропластичний типи гломерулонефриту.
Первинна профілактика гломерулонефриту полягає насамперед у зміцненні і загартовуванні організму, підвищенні його опірності до інфекції. Заняття фізичною культурою, водні процедури підвищують стійкість організму до несприятливих умов зовнішнього середовища, зокрема до охолодження і впливу вологого холоду, до простудних захворювань. Варто оберігатися від контактів із хворими на стрептококові інфекції. При захворюванні на ангіну, загостреннях хронічного тонзиліту, фарингіті та інших вогнищевих стрептококових інфекціях необхідні ліжковий режим і звільнення від роботи протягом 7—10 днів, призначення на цей термін сульфаніламідних препаратів або антибіотиків. Як під час, так і через 10—30 днів після захворювання слід здати на аналіз сечу, щоб не пропустити імовірної патології нирок, у тому числі і гострого гломерулонефриту.
Первинна профілактика хронічного гломерулонефриту тісно пов’язана із запобіганням і успішним лікуванням хворих на гострий гломерулонефрит, оскільки в більшості випадків хронічний гломерулонефрит є наслідком невилікуваного або вчасно не діагностованого гострого гломерулонефриту, і наступним тривалим диспансерним спостеріганням за ними. У деяких хворих як гострий, так і хронічний гломерулонефрит починаються і перебігають безсимптомно (латентні форми), і тільки аналіз сечі виявляє протеїнурію і гематурію. Тому при всіх звертаннях хворих у поліклініку, а також при влаштуванні на роботу, направленні на курорт, після ангіни та інших стрептококових захворювань в обов’язковому порядку потрібно проводити дослідження сечі з метою вчасного виявлення гломерулонефриту з атиповим початком.
Вторинна профілактика гломерулонефриту має бути спрямована на запобігання рецидиву гострого гломерулонефриту і переходу його в хронічний гломерулонефрит, а також на збереження протягом тривалого часу компенсації ниркових функцій і працездатності хворих.
Вторинна профілактика має включати такий комплекс заходів: правильне працевлаштування хворих, дотримання ними відповідного режиму праці і відпочинку, призначення дієти відповідно до нозологічної форми захворювання, його клінічного варіанта і функції нирок, санацію вогнищ інфекції, запобігання інтеркурентним захворюванням і лікування їх. У разі потреби варто продовжити в підтримувальних дозах розпочату в стаціонарі патогенетичну терапію. Із цією метою хворих на гострий гломерулонефрит після виписування зі стаціонару без позаниркових ознак захворювання і з нормальними аналізами сечі звільняють від роботи терміном до 2 тиж.; за наявності залишкових явищ (мікропротеїнурія, мікрогематурія) тривалість тимчасової непрацездатності збільшується до 1—1,5 міс., а в разі тривалого перебігу — до 2—3 міс.
Загальний час непрацездатності з урахуванням 2-місячного перебування в стаціонарі становить від 2—3 міс. при сприятливому перебігу захворювання до 4—6 міс. при тривалому перебігу, особливо у хворих з нефритичним синдромом і таких, що лікувалися ГКС або імунодепресантними препаратами. Особи цієї групи повинні бути влаштовані на роботу, не пов’язану з переохолодженням, особливо дією вологого холоду, і перегріванням (у гарячих цехах), без важкого фізичного навантаження і тривалого перебування на ногах; вони мають бути звільнені від поїздок у відрядження, особливо довготермінові. їм слід рекомендувати в перші 3—6 міс. щодня протягом 1—2 год дотримувати ліжкового режиму, тобто перебувати в горизонтальному положенні. Протягом 6—12 міс. не рекомендують тривалу ходьбу, рухливі спортивні ігри, плавання.
Хворим, яких лікували в стаціонарі масивними дозами ГКС, у разі приєднання інтеркурентного захворювання або після травми, операції поряд з антибіотиками та іншими методами лікування варто призначати преднізолон у дозах 15—30 мг на добу.
Потрібна велика обережність при введенні вакцин і сироваток, тому що після щеплень можливий рецидив захворювання, особливо в осіб зі схильністю до алергійних реакцій.
Якщо хворим потрібно продовжувати в підтримувальних дозах розпочате в стаціонарі лікування метиндолом (амбулаторно в дозах 50—75 мг на добу) у поєднанні з курантилом (75—100 г на добу) протягом 3—12 міс., то при цьому обов’язковим є ретельний контроль за їхнім станом, рівнем AT, аналізами сечі і крові.
Хворі на хронічний (компенсований) гломерулонефрит з латентним перебігом (ізольованим сечовим синдромом), що мають найбільш сприятливий прогноз, можуть виконувати роботу за своїм фахом, якщо вона не пов’язана з імовірністю переохолодження і великим фізичним навантаженням, з нічними змінами. Харчування має бути різноманітним і повноцінним як щодо вмісту білків, жирів і вуглеводів, так і вітамінів. Істотних обмежень у вживанні кухонної солі не рекомендують, але все-таки їжа має бути слабосолоною. Дозволяється застосовувати в помірних дозах цибулю, часник, петрушку та інші смакові приправи (перець, хрін, гірчиця тощо). Періодично, особливо навесні, варто проводити курси вітамінотерапії (вітаміни С, В6, В,, В,2, ас- корутин, нікотинова кислота).
Хворі на хронічний гломерулонефрит мають потребу в постійному багаторічному диспансерному спостеріганні. Лише в разі стійкої і повної клінічної та клініко-лабораторної ремісії, що настає завдяки наполегливій патогенетичній терапії впродовж 5 років, хворих можна зняти з диспансерного обліку. Однак вони і надалі повинні дотримувати заходів профілактики і проводити контрольні аналізи сечі під час і після інтеркурентних захворювань.
Крім того, диспансеризація хворих на хронічний гломерулонефрит передбачає дотримання термінів обстеження і виконання необхідних лабораторних та інструментальних досліджень.
При хронічному гломерулонефриті терміни і обсяг виконання необхідних досліджень залежать від клінічної форми захворювання та його перебігу.
У хворих із латентною та гематурійною формами диспансерне обстеження здійснюють два рази на рік. При цьому вимірюють AT, досліджують очне дно, проводять ЕКГ, аналіз сечі загальний, на добову протеїнурію, за Нечипоренком або за Каковським—Аддісом, Зимницьким, аналіз крові загальний і на вміст холестерину, загального білка і білкових фракцій, сечовини, креатиніну, калію, натрію, кальцію, натрію хлориду, визначають клубочкову фільтрацію за кліренсом ендогенного креатиніну. Однак у разі посилення гематурії потрібно проводити загальні аналізи сечі і крові один раз у 2— 4 тиж., а з появою макрогематурії — ще частіше; показана консультація уролога чи госпіталізація в урологічне або нефрологічне відділення для уточнення причини гематурії.
При гіпертонічній формі хронічного гломерулонефриту виконують такий самий обсяг досліджень, що і при латентній і гематурійній формах гломерулонефриту. Однак у зв’язку з потребою контролювати рівень AT і дію гіпотензивних засобів диспансерний огляд хворих цієї групи проводять один раз у 1—3 міс. (залежно від вираженості гіпертензивного синдрому).
Диспансерне обстеження хворих з нефритичної формою хронічного гломерулонефриту здійснюють щомісяця або один раз у 2 міс., але не рідше ніж один раз у квартал. Особливу увагу звертають на вираженість набрякового синдрому, об’єм добового діурезу, рівень добової протеїнурії, гіперхолестеринемії, гіпо- і диспротеїнемії. Інколи хворі з нефритичним синдромом тривалий час уживають сечогінні засоби, у зв’язку з цим потрібний ретельний контроль за електролітним складом крові, насамперед за концентрацією в ній калію.
При мішаній формі хронічного гломерулонефриту терміни диспансерного обстеження і обсяг досліджень такі самі, що й при нефритичному синдромі. Особливу увагу звертають на рівень AT, стан очного дна, вираженість набряків і протеїнурії, а також на стан азотовидільної функції нирки, оскільки при цій формі хронічного гломерулонефриту вона порушується швидше, ніж при інших. Потрібно не рідше ніж один раз у 3—6 міс. досліджувати клубочкову фільтрацію і вміст у крові сечовини і креатиніну.
Медико-соціальна експертиза
Хворі з ізольованим сечовим синдромом і нетяжким нефротичним синдромом в ангіпертензивній стадії можуть виконувати розумову і неважку фізичну роботу, не пов’язану з охолодженням та перенапруженням, без нічних змін. У разі прогресивного перебігу захворювання, стійких великих набряків, артеріальної гіпертензії, серцевої недостатності вони потребують переведення на інвалідність.
Працездатність у більшості хворих із нефритичною формою хронічного гломерулонефриту істотно знижена, а іноді через виражений набряковий синдром і взагалі втрачена. Такі хворі мають потребу в направленні на МСЕК для встановлення групи інвалідності. Вони повинні уникати найменшого переохолодження, простудних захворювань і різних інфекцій, до яких досить схильні з огляду на зниження захисних можливостей організму і які можуть бути причиною летального кінця.
Подальша інформація
Завжди консультуйтеся зі своїм лікарем, щоб переконатися, що інформація, яка відображається на цій сторінці, може бути застосована до ваших особистих обставин. Інформація призначена тільки для медичних фахівців.