Хронічний гастрит
Епідеміологія та етіологія
Хронічний гастрит — це захворювання, що характеризується запально-дистрофічними змінами в слизовій оболонці шлунка з порушенням її фізіологічної регенерації, зменшенням кількості залозистих клітин, а в разі прогресування — атрофією залозистого епітелію з наступним розвитком кишкової метаплазії і дисплазії, розладом секреторної, моторної і нерідко інкреторної функцій шлунка, що лежить в основі порушення процесу травлення.
Епідеміологія. За даними статистичних досліджень, на хронічний гастрит (ХГ) в різних країнах, у тому числі і в Україні, страждає від 30 до 50% працездатного населення. Оскільки в старших вікових групах частота цього захворювання неухильно збільшується, ХГ є не лише поширеним захворюванням системи травлення, а й досить актуальною проблемою сучасної гастроентерології.
ХГ — поняття клініко-морфологічне. Практична значущість цього захворювання визначається не стільки відповідними клінічними проявами, скільки його роллю як попередника більш важких уражень органів травлення, у тому числі і шлунка (виразкова хвороба, рак). ХГ однаково часто зустрічається і як основне захворювання, і як супутнє при багатьох захворюваннях системи травлення та інших органів і систем.
Етіологія. В основі розвитку ХГ лежить генетично зумовлений дефект репарації слизової оболонки шлунка у відповідь на ушкоджувальну дію різних зовнішніх та внутрішніх чинників.
До зовнішніх чинників, які безпосередньо травмують слизову оболонку шлунка, належать тривале порушення режиму харчування, їда всухом’ятку, вживання надмірно гарячої і грубої їжі, зловживання спеціями, алкоголем, дефекти жувального апарату, що спричиняє систематичну травматизацію слизової оболонки шлунка недостатньо подрібненою "їжею, безконтрольне вживання деяких медикаментів, особливо НПЗП, глюкокортикоїдів, сульфаніламідних препаратів тощо. У разі схильності до алергійних реакцій ушкоджувальний вплив на слизову оболонку шлунка можуть здійснювати різні харчові алергени: цитрусові, суниці, томати, шоколад, какао.
Токсичну, іритативну і корозійну дію щодо слизової оболонки шлунка спричинює нікотин (у запеклих курців) та деякі професійні чинники: металевий, силікатний, вугільний пил, пари кислот та основ, робота в гарячих цехах, контакт з продуктами синтетичної хімії.
Серед ендогенних чинників ХГ найбільш значними є НР-інфікованість (у хворих на ХГ типу В, який становить близько 80—90% усіх ХГ), генетична схильність (ХГ типу А, питома вага якого серед ХГ становить 5—10%), рефлюкс жовчі в шлунок (призводить до розвитку так званого хіміотоксичного ХГ, який становить близько 5%). Інші ендогенні чинники впливають на слизову оболонку шлунка через нервово-рефлекторні, гуморальні і токсичні механізми, які наявні при захворюваннях центральної нервової і вегетативної систем (арахноїдит, посттравматична енцефалопатія, гіпоталамічний синдром, невротичні стани, вегетоневрози), патології ендокринних залоз (цукровий діабет, тиротоксикоз, гіпотироз та ін.), хворобах обміну речовин (анемія, ожиріння, гіповітамінози), хронічних інфекційно-запальних захворюваннях (тонзиліт, карієс зубів, аднексит, холангіт, гепатит, холецистит, панкреатит, бронхоектазія), а також при серцевій і дихальній недостатності, що перебігає з явищами тканинної гіпоксії, захворюваннях нирок з розвитком хронічної недостатності.
Патогенез
Повідомлення про зв’язок ХГ з мікроорганізмами, виділеними австралійськими вченими B.J.Marshall і I.R.Warren із слизової оболонки шлунка хворого на ХГ й умовно названими Campylobacter pylori, з’явилися в 1983 р. У 1989 р. їх перейменували на Helicobacter pylori (HP), оскільки подібність цих мікроорганізмів до кампілобактерій є досить сумнівною.
Бактеріальний ХГ (тип В) є найпоширенішим (понад 80% усіх випадків ХГ). Ураження локалізується переважно в антральному відділі. Згідно з рекомендаціями Сіднейської класифікації, його називають HP-асоційованим ХГ. Такий ХГ виявляють майже в усіх випадках виразкової хвороби, тому його розглядають як одну з причин утворення виразки. Супутніми етіологічними чинниками можуть бути зловживання алкоголем, гостра їжа, нерегулярне харчування, паління. ХГ типу В розвивається в осіб молодого віку. Секреторна функція при цьому не порушена або навіть підвищена на початку захворювання, гіпоацидний стан спостерігають за відсутності гастринемії, що є суттєвою відмінністю ХГ типу В від ХГ типу А.
HP притаманні унікальні властивості, які дозволяють їм виживати в умовах агресивного шлункового вмісту (мал. 81). Так, їх виявляють у воротарі шлунка під шаром слизу, де наявний оптимальний рівень рН (3—6). Це сприяє виживанню HP, які мають адгезивні властивості стосовно покривно-ямкового епітелію слизової оболонки шлунка. Оптимальний для HP рівень рН підтримується завдяки виділенням цими бактеріями ферменту уреази, який гідролізує сечовину шлункового соку до вуглекислого газу й аміаку. Останній утворює навколо бактерій захисну "хмарку", нейтралізуючи хлоридну кислоту. Несприятливим для існування HP є середовище з рН нижче від 3 і вище від 7.
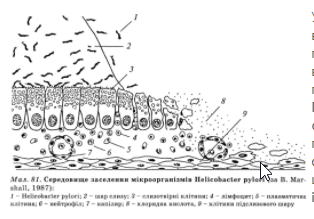
Унаслідок тривалого персистування HP у слизовій оболонці в ній виникають певні зміни. Зокрема збільшується кількість лімфоцитів, поліморфноядерних нейтрофільних фанулоцитів, які інфільтрують власну пластинку слизової оболонки; крім того, зростає число плазматичних клітин, які продукують специфічні для HP IgG і IgA. При цьому збільшення кількості клітин, які продукують IgA, супроводжується запальною реакцією, а скупчення клітин, які продукують IgG, збігається з вогнищами атрофії. Ураховуючи цю фазність у появі антитіл різного класу, можна припустити, що процеси запалення та атрофії пов’язані, мають спільне інфекційно-імунне походження і є фазами одного патологічного процесу.
Морфологічною особливістю рН-асоційованого ХГ є наявність у слизовій оболонці шлунка мікроорганізмів Helicobacter не тільки у вегетативній, але і в коковій формі. HP являє собою спіралеподібні бактерії зі джгутиками по 4—7 на одному кінці.
Терміном "атрофічний гастрит" визначається група специфічних станів слизової оболонки, що супроводжуються втратою власних залоз в одному або в декількох відділах шлунка. Після прийняття Сіднейської системи виділяють два варіанти атрофічного гастриту: автоімунний (розвивається виключно в тілі шлунка) і мультифокальний (розвивається як у тілі шлунка, так і в його антральному відділі).
В основі розвитку автоімунного ХГ (тип А) лежить утворення автоантитіл до парієтальних гландулоцитів (обкладкових клітин), які виробляють у шлунку хлоридну кислоту, і внутрішнього чинника. Унаслідок атрофії цих клітин розвиваються ахлоргідрія і компенсаторна гіпергастринемія, порушується всмоктування ціанокобаламіну і виникає В12-дефіцитна анемія.
Хронічний мультифокальний атрофічний гастрит (тип АВ), або змішана форма гастриту, зустрічається переважно у хворих похилого віку і зумовлений здебільшого тривалою HP-інфекцією на тлі впливу на слизову оболонку шлунка інших чинників (тривалі періоди незбалансованого і недостатнього харчування, уживання переважно солоної їжі, недостатній вміст у харчовому раціоні свіжих овочів і фруктів тощо). При цьому у значної частини клітин ДНК ушкоджується і вони зазнають апоптозу, не встигнувши диференціюватися. Установлено, що підвищення в апоптозних клітинах вмісту цитоке- ратину-1 свідчить про наявність у них глибоких мутацій. Можна припустити, що клітина, в якій накопичилися ушкодження ДНК (мутації), у певний момент набуває іншого фенотипу. Це опосередковано підтверджується тим, що у хворих на атрофічний гастрит часто виявляють кишкову метаплазію і дисплазію, тобто наявні клітини з цілком іншим фенотипом, що фактично і є причиною зниження секреції хлоридної кислоти при цьому типі ХГ.
Хіміко-токсичний індукований ХГ (тип С) зумовлений закиданням у шлунок кишкового вмісту лужної реакції, а також впливу на слизову оболонку шлунка, переважно антрального відділу, хімічних подразників, медикаментів тощо. Морфологічні зміни при цьому часто носять вогнищевий характер, тому тривалий час зберігається нормальна шлункова секреція.
Серед різних варіантів гастриту типу С у клінічній практиці найбільше значення мають рефлюкс-гастрит і гастрит, асоційований з уживанням НПЗП.
Рефлюкс-гастрит (лужний рефлюкс-гастрит) спричинюється постійною травматизацією слизової оболонки антрального відділу шлунка жовчю, що закидається під час дуоденогастрального рефлюксу, а також спостерігається після часткової резекції шлунка, гастроентеростомії, ваготомії, холецистектомії, при порушеннях дуоденальної прохідності, недостатності воротаря. Крім жовчі необхідною умовою розвитку гастриту є наявність хлоридної кислоти.
Жовчні кислоти, маючи детергентні властивості, сприяють солюбизації ліпідів мембран поверхневого епітелію. Такий ефект залежить від концентрації, рівня кон’югації і гідроксилювання жовчних кислот і, що дуже важливо, від рН у порожнині шлунка. При низьких значеннях рН слизову оболонку ушкоджують лише тауринові кон’югати, інші в таких умовах преципітують. При високих показниках рН, що особливо характерно для культі резектованого шлунка, некон’юговані і дигідроксильні жовчні кислоти мають значно більші ушкоджувальні властивості, ніж кон’юговані і тригідроксильні. Унаслідок постійного ушкодження слизової оболонки шлунка кишковим вмістом відбуваються дистрофічні, некробіотичні і некротичні зміни епітелію, що є початком утворення ерозії. З часом наростають атрофічні зміни слизової оболонки шлунка, які супроводжуються прогресуванням проліфе- ративних процесів і розвитком дисплазїї різного ступеня вираженості, що збільшує ризик появи раку.
Нерідко гастрит типу С є наслідком уживання НПЗП, які спричинюють як суб’єктивні ознаки шлункової диспепсії, так і морфологічно верифіковану НПЗП-гастропатію, що включає в себе гастритоподібні зміни, ерозії і виразки, об’єднані єдиним патогенезом. При цьому найчастіше уражається антральний відділ шлунка, рідше — ампула (цибулина) дванадцятипалої кишки. Ураховуючи те, що у світі понад 30 млн людей щодня вживають НПЗП, побічні дії цих препаратів виявляють досить часто (за даними різних авторів, від 25 до 45% випадків).
НПЗП ушкоджують слизову оболонку шлунка через різні механізми: зменшують продукування шлункового слизу і бікарбонатів, збільшують вироблення хлоридної кислоти і пепсиногену, знижують кровотік у слизовій оболонці шлунка, стимулюють апоптоз епітеліальних клітин, посилюють утворення вільних радикалів, ФНП і збільшують гемотаксис нейтрофілів, впливають на внутрішньоклітинний вміст кальцію, знижують утворення глютатіону, роз’єднують окиснювальне фосфорилювання. Здатність НПЗП ушкоджувати слизову оболонку верхнього відділу травного тракту зумовлена тим, що ці препарати блокують як фермент циклооксигеназу-2 (ЦОГ-2), що бере участь в активації запальних реакцій, так і циклооксигеназу-1 (ЦОГ-1), що сприяє виробленню простагландинів (насамперед ПГЕ2 і ПІ2), які забезпечують захист слизової оболонки шлунка. Таким чином, під впливом НПЗП рівновага між чинниками захисту й агресії порушується на користь останніх. Чинниками ризику розвитку НПЗП-гастропатій, у тому числі і НПЗП-інду- кованого гастриту, є: похилий вік (один із найбільш значущих чинників), виразкова хвороба і виразкові кровотечі в анамнезі, супутні захворювання серцево-судинної системи, легень, печінки та інших внутрішніх органів, тривале вживання діуретиків та інгібіторів АПФ, високих доз НПЗП, одномоментне вживання декількох НПЗП, НПЗП і глюкокортикоїдів, НПЗП й антикоагулянтів, перші 3 міс вживання НПЗП. За вираженістю ушкоджувальної дії на слизову оболонку шлунка найпоширеніші НПЗП утворюють такий ряд: ацетилсаліцилова кислота > індометацин > піроксикам > вольтарен > бруфен. У цьому аспекті перевагу мають ЦОГ-2-селективні (мелоксикам, німесулід) і високоселективні (целекоксиб, рофекоксиб) НПЗП.
Роль НР-інфікованості в розвитку НПЗП-гастропатій оцінюють неоднозначно. Є дані про те, що ерадикація HP і виліковування від антрального гастриту перед лікуванням НПЗП дозволяє знизити частоту розвитку гастропатії. Водночас встановлено протилежний факт: інфекція HP, індукуючи вироблення ендогенних простагландинів у слизовій оболонці шлунка, дає цитопротекторний ефект і прискорює загоєння НПЗП-гастропатій. При морфологічному дослідженні виявляють еозинофільну інфільтрацію слизової оболонки, а також фовеолярну гіперплазію, збільшення непосмугованих м’язових клітин у власній пластинці.
На відміну від рефлюкс-гастриту, НПЗП-індукований гастрит (див. вклейку, мал. 82) не має вираженого порушення клітинного відновлення і має інший передраковий потенціал, що вимагає розмежування цих варіантів хімічного гастриту.
У міру прогресування захворювання всі форми ХГ призводять до розвитку дифузної атрофії слизової оболонки й ахлоргідрії.
Класифікація. У МКХ-10 хронічний гастрит займає рубрики:
К29 Хронічний гастрит.
К29.3 Хронічний поверхневий гастрит.
К29.4 Хронічний атрофічний гастрит.
К29.6 Інші гастрити.
Найбільш поширеною клінічною класифікацією ХГ є так звана Сіднейська система з доповненням Х’юстонської робочої групи (1994) і врахуванням Німецької класифікації ХГ (1989).
Класифікація хронічного гастриту
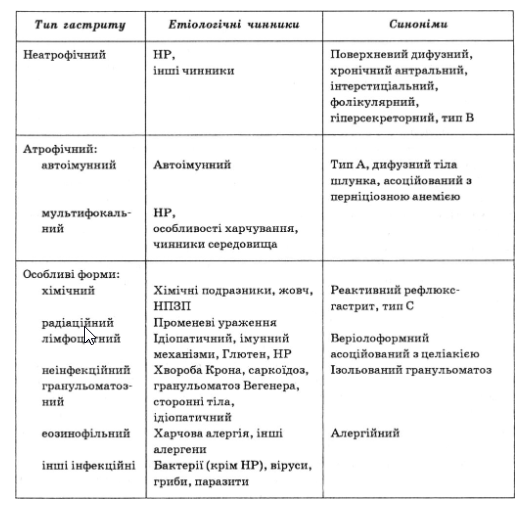
Клінічна картина ХГ неспецифічна і значною мірою визначається типом, характером і поширенням патологічного процесу.
Автоімунний атрофічний гастрит (тип А) найчастіше має сімейний характер і часто поєднується з автоімунними ендокринопатіями (автоімунний тироїдит, тиротоксикоз, гіперпаратироідизм, цукровий діабет І типу, хвороба Аддісона та ін.).
Синдром гіповітамінозу патогенетично пов’язаний з недостатністю всмоктування, проявляється ознаками дефіциту різних вітамінів, частіше групи В (заїди в кутиках рота, підвищене злущування шкіри, випадання волосся, ламкість нігтів тощо) і зустрічається виключно у хворих на автоімунний гастрит і атрофічний пангастрит із секреторною недостатністю.
Диселектролітний синдром також є одним із проявів недостатності всмоктування переважно у хворих на атрофічний гастрит зі зниженою секреторною функцією шлунка.
Дефіцит внутрішнього чинника призводить до вираженого порушення всмоктування вітаміну В12 і розвитку мегалобластної (В12-дефіцитної) анемії, що проявляється блідістю шкіри і слизових оболонок, субіктеричністю склер, слабкістю, запамороченням голови, болем у серці, пекучим болем на кінчику язика від гострої їжі. Язик стає яскраво-червоним, гладеньким і блискучим ("лакований"), печінка помірно збільшена. Характерним є ураження центральної нервової системи, переважно за типом статевого фунікулярного мієлозу: зниження або відсутність рефлексів, атаксія, парестезії. Вважається, що найчастіше саме ця форма гастриту перероджується в рак.
Мультифокальний атрофічний гастрит не має специфічних проявів і може перебігати безсимптомно. Хворі рідко скаржаться на больовий синдром, переважають симптоми шлункової (переливання в надчеревній ділянці після їди, відрижка, зригування гіркуватою рідиною, нудота, металевий присмак у роті, зниження апетиту) і кишкової (бурчання і переливання в животі, метеоризм, нестійкі випорожнення, діарея, втрата маси тіла) диспепсії. Біль у надчеревній ділянці виникає відразу після іди, частіше тупий, не іррадіює, посилюється під час ходьби і в положенні стоячи. Відзначають зв’язок болю і диспепсичних розладів з характером харчування. Біль частіше виникає після споживання гострої, грубої, смаженої, копченої, жирної їжі, концентрованих наварів, холодного молока або молочних продуктів.
У більшості випадків мультифокальний атрофічний гастрит не впливає на загальний стан хворих. Для нього не типова швидка втрата маси тіла або розвиток анемії в короткий термін. Такий латентний перебіг пояснюється тим, що порушення функції шлунка компенсується печінкою, підшлунковою залозою і кишками. Однак у цих хворих досить часто спостерігається астеноневротичний синдром.
Хронічний гелікобактерний антральний гастрит (тип В) з підвищеним кислотопродукуванням часто поєднується з хронічним дуоденітом, зазвичай асоціюється з виразкоподібним варіантом диспепсії. У пацієнтів цієї категорії відзначають больовий синдром, характерний для виразкової хвороби дванадцятипалої кишки:
• біль, який виникає через 1,5—2 год після їди, а іноді і через більший проміжок часу (пізній біль);
• голодний біль, який виникає через 6—7 год після їди (частіше вранці);
• нічний біль;
• біль локалізується в надчеревній ділянці, зникає або зменшується після їди;
• біль також може виникати або посилюватися відразу або невдовзі після їди.
Нерідко хворі скаржаться на печію і відрижку кислим, особливо в разі поєднання з гастроезофагального рефлюксною хворобою.
Апетит частіше не порушений, відзначають схильність до закрепів. Виявляють болючість під час пальпації в надчеревній ділянці, більше справа.
З часом, особливо у пацієнтів старших вікових категорій, атрофічний процес поширюється проксимально від антрального відділу до тіла шлунка (див. вклейку, мал. 83), що веде до розвитку дифузної форми (пангастриту) і супроводжується зміною класичної виразкоподібної клінічної картини гелікобакгерно- го антрального гастриту на клініку дифузного атрофічного гастриту (тип АВ), який проявляється переважно симптомами диспепсії. Хворі скаржаться на відчуття важкості, повноти в надчеревній ділянці, швидкого насичення, а також відрижку повітрям або, у разі вираженого процесу, пухлини. Характерним симптомом є нудота. Іноді відзначають тупий біль у надчеревній ділянці, який посилюються після їди. Можливий неприємний, часто металевий, присмак у роті. Апетит знижений. Синдром недостатності травлення і всмоктування, властивий атрофічному ХГ, зумовлений як надмірно швидким просуванням харчової маси по кишках внаслідок секреторної недостатності, так і наявністю ентероколіту, який нерідко супроводжує цю форму ХГ.
Прискорення просування харчових мас по кишках утруднює травлення їх ферментами підшлункової залози і тонкої кишки. Клінічними проявами цього стану є метеоризм, буркотіння в животі, періодичний пронос після споживання молока і жирів, схуднення (частіше поступове і помірне), гіпо- протеїнемія, переважно за рахунок альбумінів. Однак наявність у хворого на ХГ вираженої кишкової диспепсії свідчить про можливість розвитку первинної патології підшлункової залози і кишок.
Під час об’єктивного обстеження виявляють обкладений білим нальотом язик, дифузну болючість при пальпації в надчеревній ділянці.
У більшості хворих рефлюкс-гастрит перебігає безсимптомно. Однак часом виникають біль у надчерев’ї, нудота, блювання з домішками жовчі, з’являються схильність до втрати маси тіла й анемії, ознаки демпінг-синдрому.
Завдяки ендоскопії шлунка виявляють вогнищеву гіперемію, набряк слизової оболонки, забарвлений у жовчний колір шлунковий сік, зяючий воротар, з якого до шлунка порціями надходить жовч (див. вклейку, мал. 84). На тлі рефлюкс-гастриту часто розвиваються гіперпластичні поліпи і карцинома шлунка.
Клінічна симптоматика НПЗП-гастропатій включає нудоту, блювання, шлунково-стравохідний рефлюкс, інколи — діарею. Досить часто, навіть за наявності виразки стравоходу, больовий синдром відсутній або слабко виражений, що пов’язано зі знеболювальним ефектом НПЗП.
Методи обстеження
Безпосередній огляд хворих на ХГ має невелику діагностичну цінність. Лише огляд язика може дати деяку інформацію. У хворих на ХГ часто спостерігають білий або жовто-білий наліт на язиці з відбитками зубів на його бічних поверхнях. Класичною ознакою автоімунного гастриту типу А з перніціозною анемією є гунтерівський глосит, який характеризується появою спочатку яскравих запальних ділянок, афтозних висипань або тріщин, частіше в ділянці кінчика язика і бічних поверхонь, а потім - згладженістю та атрофією сосочків — лакований язик (див. вклейку, мал. 85).
Аускультація і перкусія теж практично не допомагають у діагностиці цього захворювання і лише у хворих на гастрит з секреторною недостатністю під час аускультації живота визначають збільшення кишкових шумів (посилена кишкова перистальтика).
Під час пальпації живіт частіше м’який, іноді дещо здутий. Під час глибокої пальпації у хворих на ХГ типу А або атрофічний пангастрит нерідко визначають помірну дифузну болючість у надчеревній ділянці, а при НР-асоційованому ХГ — локальну болючість у пілородуоденальній зоні (ділянці воротаря шлунка і дванадцятипалої кишки).
Урахування зазначених симптомів має важливе значення не стільки для діагностики ХГ, скільки для розмежування його з іншими ураженнями шлунка і насамперед з виразковою хворобою, поліпозом і раком; до того ж ці захворювання досить часто поєднуються з ХГ.
Діагностичне значення дослідження шлункової секреції також невелике, оскільки у хворих нерідко відсутня залежність між станом секреції і морфологічними змінами слизової оболонки шлунка. Установлено, що вогнищевий характер ураження слизової оболонки суттєво не впливає на секреторну функцію шлунка.
Однією з особливостей автоімунного гастриту є збереження протягом тривалого часу пепсинотвірної функції на достатньому рівні. Відносна стабільність ферментоутворення в умовах формування атрофічного гастриту знижує діагностичну значущість визначення пепсину в шлунковому соку.
До основних методів функціональної діагностики у хворих на ХГ належать дослідження шлункової секреції тонким зондом і внутрішньошлункова рН-метрія.
ХГ властива різноманітність моторно-евакуаторних порушень, для визначення характеру яких використовують рентгенологічне дослідження (мал. 86). Так, у хворих на ХГ із секреторною недостатністю частіше спостерігають послаблену констрикторну функцію воротаря, що призводить до прискореної евакуації вмісту шлунка, тоді як пілороспазм і затримання евакуації - рідкісні явища.
Основним методом, який дає змогу провести не тільки візуальну, а й морфологічну оцінку слизової оболонки шлунка, визначити поширеність патологічного процесу, нині є фіброгастроскопія з прицільною біопсією. Однак навіть у хворих з поширеним гастритом вираженість морфологічних змін слизової оболонки різних відділів шлунка неоднакова, тому для діагностики ХГ біоптати беруть з різних ділянок шлунка.
За результатами гістологічного дослідження біоптатів слизової оболонки шлунка виділяють такі форми ХГ:
1) поверхневу (катаральну);
2) інтерстиціальну (ураження залоз без атрофії);
3) атрофічну;
4) атрофічну з ознаками перетворення залоз за пілоричним або кишковим типом;
5) атрофічно-гіперпластичну (змішану);
6) гіперпластичну;
7) поліпозну.
У початкових стадіях ХГ найчастіше має вогнищевий характер, але навіть на цьому етапі розвитку хвороби в пілороантральному відділі поряд з кишковою метаплазією відзначають поширення залоз воротаря на малій кривині в проксимальному напрямку. У разі подальшого прогресування ХГ морфологічні зміни поширюються майже на весь орган. Неатрофічні форми ХГ переважають у пілороантральному відділі (тип В), атрофічні — у тілі шлунка (тип А).
Для встановлення етіопатогенетичного варіанта ХГ обов’язковим є визначення НР-інфікованості, що має важливе значення для проведення диференціальної діагностики як різних варіантів ХГ, так і HP-асоційованих захворювань.
Таким чином, клінічний діагноз ХГ повинен включати:
1) етіологічне і патогенетичне визначення форми;
2) гастроскопічну і морфологічну характеристики;
3) локалізацію: поширений, обмежений (антральний або фундальний);
4) стан кислототвірної і кислотонейтралізувальної функцій;
5) фазу перебігу: загострення, затухання загострення, ремісія;
6) наявність ускладнень.
Диференціальну діагностику різних варіантів ХГ проводять насамперед з функціональною (невиразковою) шлунковою диспепсією, виразковою хворобою, доброякісними пухлинами і раком шлунка, а також з іншими захворюваннями органів травлення.

Функціональній невиразковій диспепсії властивий тривалий, багатолітній, часто хвилеподібний перебіг без помітного прогресування і відсутності морфологічних змін з боку слизової оболонки і так званих симптомів тривоги: дисфагії, лихоманки, "безпричинного" схуднення, лімфаденопатії, анемії, позитивної реакції на приховану кров, збільшення ШОЕ тощо. Наявність таких симптомів дозволяє припустити розвиток більш тяжких і прогностично серйозніших патологічних змін, ніж хронічний гастрит і функціональна диспепсія.
Особливу увагу слід звернути на хворих, у яких вперше з’явилися скарги, характерні для дисмоторної диспепсії (швидка насичуваність, відчуття важкості у верхній половині живота). Нерідко це перші клінічні прояви раку шлунка, які можуть поєднуватися з помірним нестійким болем, що не зникає вночі.
Основним методом диференціальної діагностики функціональної диспепсії, хронічного перебігу виразкової хвороби і раку шлунка є ендоскопія з гастробіопсією і наступним гістологічним дослідженням біоптатів.
Лікування хворих на ХГ частіше проводять в амбулаторних умовах, але в разі вираженого загострення (біль, стійка шлункова диспепсія, схуднення), загрози розвитку ускладнень (кровотечі з множинних ерозій, перигастрит) і складності диференціальної діагностики (поліпозний, ригідний антральний гастрит, хвороба Менетріє) пацієнта потрібно госпіталізувати.
Визначаючи тактику лікування, необхідно враховувати фазу хвороби, клінічний і морфологічний варіант гастриту, особливості секреторної і мо- торно-евакуаторної функції шлунка.
Основні принципи лікування під час загострення ХГ такі:
1) нормалізація режиму і характеру харчування;
2) нормалізація функціонального стану центральної нервової системи;
3) усунення професійних та інших шкідливостей;
4) антибактеріальна (HP-асоційований ХГ) або імуносупресивна терапія (автоімунний гастрит);
5) дія на змінену слизову оболонку шлунка з метою її захисту і посилення репаративних процесів;
6) корекція порушень шлункової секреції;
7) корекція розладів моторної функції та кишкового травлення;
8) лікування супутніх захворювань травного каналу та інших органів і систем з метою запобігти загостренню ХГ надалі.
Раціональна дієтотерапія є одним із основних методів лікування хворих на ХГ. У період загострення незалежно від характеру секреторних розладів провідну роль відіграє принцип щадіння слизової оболонки шлунка (переважно призначають дієту № 1а). Хворим слід споживати їжу 5—6 разів на день, невеликими порціями. Температура страв повинна бути помірною; харчові продукти треба ретельно обробляти механічно (готують пюре, слизисті супи, парові котлети, суфле та ін.). Виключають страви, які подразнюють слизову оболонку. Хворим на ХГ із секреторною недостатністю забороняють продукти, що посилюють процеси бродіння в кишках (незбиране молоко, виноград та ін.), а також їжу, для засвоєння якої потрібне велике напруження травних процесів (тваринні тугоплавкі жири, сметана тощо). Хворих на ХГ зі збереженим чи підвищеним кислотопродукуванням послідовно переводять на дієту № 16 і їв. У подальшому харчування таких хворих повинне бути повноцінним, але з харчового раціону виключають соління, маринади, гострі приправи, наваристі м’ясні і рибні супи, смажені страви, алкогольні напої; рекомендується обмежувати вживання кухонної солі, міцного чаю, кави. Важливим є ретельне пережовування їжі.
Хворим на ХГ із секреторною недостатністю показана функціональна стимуляція залоз дна шлунка, яку з ліквідацією ознак загострення поступово посилюють шляхом призначення дієти № 2. Вона багата на вітаміни, екстрактивні речовини і передбачає обмеження грубої рослинної клітковини. Зокрема, не використовують сирі овочі і фрукти (з них готують пюре), інші харчові продукти також подрібнюють, добре проварюють чи просмажують. Екстрактивні речовини стимулюють кислотопродукування і поліпшують апетит, часто знижений у цієї категорії пацієнтів, особливо при атрофічній формі ХГ. Не показані чорний і білий свіжий хліб, свіжі вироби з тіста, жирні сорти м’яса і риби, гострі, солоні страви, холодні напої. Незбиране молоко, напої, що спричиняють бродіння, хворі на ХГ із секреторною недостатністю переносять погано, але можна рекомендувати чай, каву з молоком, каші і пюре на молоці. Для запобігання подальшому прогресуванню атрофічних змін слизової оболонки шлунка хворі повинні дотримуватися режиму харчування, виключити чинники, що подразнюють слизову оболонку. У період стійкої ремісії дозволяють більш розширену дієту: негострі сорти сиру, нежирну шинку, фрукти і овочі в більшій кількості (однак капустою, виноградом та іншими продуктами, що посилюють бродіння в кишках, зловживати не слід), зелень, фруктові та овочеві соки, нетверді яблука, очищені груші.
У разі поєднання ХГ із запальними процесами у жовчних шляхах і печінці (хронічний холецистит, ангіохоліт, хронічний гепатит), особливо за наявності водночас коліту зі схильністю до проносу, потрібно на початку лікування рекомендувати механічно і хімічно щадну дієту № 5а. Овочі і фрукти дають вареними і протертими. Забороняють продукти і страви, що містять грубу рослинну клітковину: квасолю, горох, капусту, огірки, редьку та ін. Помідори і свіжий томатний сік більшість хворих переносять добре. Загальну кількість жирів обмежують до 60 г (35—40 г тваринних і 15—20 г рослинних). Тугоплавкі жири не рекомендують, бо вони особливо погано розщеплюються. Більш суворе обмеження кількості жирів небажане, оскільки вони стимулюють жовчовиділення. Крім того, олії мають ліпотропні властивості (містять незамінні жирні кислоти), а також запобігають виникненню закрепу, зумовленого споживанням протертої, механічно щадної їжі.
Більшості хворих на ХГ із секреторною недостатністю у фазу ремісії показана дієта № 15 з деякими змінами відповідно до віку пацієнта. Ця повноцінна дієта з достатньою для людини, яка професійно не займається фізичною працею, енергетичною цінністю (3000—3200 кал) містить 120—130 г білка (у тому числі 60 г тваринного), 100 г жирів (65—70 г тваринних), 400-450 г вуглеводів, подвоєну порівняно з нормою кількість вітамінів (ретинолу — 2 мг, кислоти аскорбінової — 100 мг, тіаміну — 4 мг, рибофлавіну — 4 мг, нікотинової кислоти — 30 мг) і достатню кількість мікроелементів (кальцію — 0,8 г, фосфору — 1,6 г, заліза — 15 мг, кухонної солі — 10—12 г). Кулінарне оброблення різноманітне. Виключають харчові продукти із вмістом великої кількості грубої рослинної клітковини, а також жирну їжу, страви з великою кількістю спецій, надмірно солоні. Не рекомендують споживати свіже здобне тісто, міцну каву, морозиво, заварний крем; забороняють алкогольні напої, прянощі. Здебільшого хворі на ХГ добре переносять цю дієту; деяке здуття живота, що інколи спостерігають у перші дні, згодом минає.
Після закінчення курсу лікування хворим на ХГ показане повноцінне харчування з виключенням продуктів, які можуть сприяти загостренню. При цьому хворим на ХГ типу В рекомендують обмежувати переважно грубу, гостру і сокогінну їжу, а хворим на ХГ типу А — грубу, з подразними властивостями їжу і таку, що сприяє процесам бродіння в кишках.
Медикаментозне лікування призначають залежно від етіологічного і патогенетичного типу гастриту. Так, у лікуванні ХГ типу В, особливо його антральної форми, основними принципами є знищення HP у слизовій оболонці шлунка за допомогою антибактеріальних препаратів, усунення запалення, корекція секреторної функції тощо.
Для усунення HP-інфекції у хворих на ХГ проводять антибактеріальну ерадикаційну терапію відповідно до рекомендацій Маастріхтської угоди II (2000), згідно з якими обов’язковими показаннями до проведення такої терапії є: атрофічний гастрит; гастрит культі шлунка після резекції з приводу раку шлунка; наявність в інфікованого HP прямих родичів, які мають або перенесли рак шлунка; бажання самого хворого після детальної консультації з лікарем (це показання не є беззаперечним і підлягає подальшому обговоренню).
Відносним (рекомендованим) показанням до проведення антигелікобак- терної ерадикаційної терапії є НПЗП-гастропатія. У Маастріхтській угоді II підкреслюється, що ерадикація HP знижує частоту виразок, пов’язаних із застосуванням НПЗП, якщо вона була проведена до початку вживання НПЗП.
Антигелікобактерна терапія являє собою систему, що включає як терапію першої лінії, так і резервну (терапію другої лінії), якщо лікування схемою першої лінії буде неефективним.
У терапії першої лінії поєднують ІПН або ранітидин — вісмуту цитрат у стандартній дозі (омепразол — 20 мл, лантропазол — 40 мг, рабепразол - 30 мг, езомепразол — 20 мг) 2 рази на день у поєднанні з кларитроміцином по 500 мг 2 рази на день і амоксициліном по 1000 мг 2 рази на день або метронідазолом по 500 мг 2 рази на день, як мінімум протягом 7 днів.
У разі відсутності ерадикації HP після проведення описаного вище лікування рекомендується друга (резервна) лінія — "четвертна" терапія (квадри- терапія): ІПН, колоїдний субцитрат (або субсаліцилат) вісмуту, тетрациклін або ампіцилін, метронідазол.
Антибіотикотерапію проводять на тлі вживання продуктів функціонального харчування, які містять живі лакто- і біфідумбактерії (ейканол, ейфітол — усередину по 3—4 г на день у капсулах).
У разі неефективності резервної схеми подальше лікування проводять індивідуально.
Хворим із антральною формою ХГ типу В у разі загострення з наявністю болю і диспепсичних розладів призначають антихолінергічні засоби з переважною периферійною дією: ін’єкції метацину (1 мл 0,1% розчину), платифіліну (1—2 мл 0,2% розчину), гастроцепіну (2 мл 0,5% розчину) або пероральне вживання цих препаратів відповідно по 0,002, 0,005 і 0,025 г (за 15-30 хв до їди, 2-3 рази на день протягом 2—3 тиж). При больових відчуттях у надчеревній ділянці і посиленій моториці шлунка призначають бускопан по 10 мг 2—3 рази на день (антихолінергічний препарат) або міогенні спазмолітики: дюспаталін (мебеверину гідрохлорид) по 200 мг 2 рази на день або но-шпу форте. Водночас призначають антацидні обволікальні і в’яжучі препарати: альмагель, альмагель А (1—2 ложки-дозатори 3 рази на день за 30 хв до іди і 4-й раз — безпосередньо перед сном), фосфалюгель (по 16 г 3 рази на день за 30 хв до їди), маалокс (по 10 мл 3 рази на день через 1—2 год після їди і 4-й раз — безпосередньо перед сном), вікалін або вікаїр (по 1—2 таблетки через 1,5—2 год після їди і на ніч), вінілін (по 20—30 мл через 2 год після їди 1 раз на день). З цією ж метою використовують магнію карбонат основний (1—2 г), магнію окис (0,5—1,5 г) і вісмуту нітрат основний (0,5—1,5 г), які також призначають у міжтравний період 3—4 рази на день. Хворим із больовим ерозивним гастритом з підвищеною секрецією холінолітики спочатку призначають підшкірно 2—3 рази на добу, а після усунення больового синдрому переходять на пероральне вживання препарату.
Комбіноване застосування холінолітичних і гангліоблокувальних засобів зменшує потребу в антацидах і сприяє зняттю болю, зумовленого спастичним скороченням воротаря і порушенням перистальтики шлунка та дванадцятипалої кишки. Комплекс лікування хворих на ХГ типу В, особливо із супутнім дуоденітом і виразкоподібною клінікою, включає також призначення седативних засобів і транквілізаторів. Останнім часом у хворих ХГ з підвищеною кислотопродукувальною функцією шлунка, особливо у хворих на ерозивний гастрит, застосовують блокатори Н2-рецепторів.
У разі метеоризму і болю в животі доцільно призначати метеоспазмін (альверину цитрат 60 мг, симетикон 300 мг) по 1 капсулі перед їдою.
Локальну протизапальну дію на слизову оболонку шлунка справляє настій квіток ромашки (1 столова ложка квіток на 1 склянку окропу). Його вживають по 1 склянці 2—3 рази на день за 1 год до іди. Цим настоєм (1 л) можна вранці промивати шлунок. Його протизапальні властивості зумовлені наявністю в квітках ромашки діючої речовини азулену. Такі самі властивості має витяжка з квіток липи, яку вживають до іди.
Як протизапальний засіб застосовують також алантон (препарат дев’ясилу високого) по 0,1 г 2—4 рази на день за 30 хв до їди; калефлон (екстракт з квіток нагідок) по 0,1—0,2 г (1—2 таблетки) 3 рази на день після іди; плантаглоцид (полісахариди листя подорожника, каротин, вітамін С, репантин гіркоти, дубильні речовини) у гранулах по 1 чайній ложці в 1/4 склянки теплої води 2—3 рази на день за 30 хв до їди; настої звіробою, м’яти, деревію.
Позитивно впливають на обмінні процеси в слизовій оболонці шлунка: деринат (натрієва сіль нативної ДНК) по 5 мл внутрішньом’язово через день (5—10 ін’єкцій); карнітину хлорид по 1/2—2 чайні ложки 20% розчину (0,5- 2 г) 2 рази на день протягом 1—3 міс; рибоксин по 0,2 г 3 рази на день за ЗО хв до іди протягом 3—4 тиж; етаден (метаболіт аденіну) по 10 мл 1% розчину 1—2 рази на день внутрішньом’язово протягом 2—3 тиж; олія шипшини та олія обліпихи по 1 чайній ложці 3 рази на день за 30 хв до іди протягом 3—4 тиж.
У фазу загострення, що затихає, хворим на гастрит типу В показані лужні маломінералізовані води (боржомі, слов’янська, березівська, єсентуки № 4 і № 20, лужанська), які вживають негазованими, теплими за 1—1,5 години до іди (аби запобігти подразненню слизової оболонки шлунка) великими ковтками (вода швидко надходить із шлунка в кишки і гальмує шлункову секрецію). Основною метою у лікуванні хворих на ХГ типу А є вибір раціональної за- місної терапії, усунення запального процесу та інших проявів захворювання.
Хворим на ХГ із секреторною недостатністю призначають засоби заміс- ної терапії (хлоридна кислота, натуральний шлунковий сік, абомін, ацидинпепсин, пепсидил, сугаст-2 та ін.), препарати, що стимулюють секреторну функцію шлунка (сік подорожника, плантаглюцид, препарати кальцію, гірка настойка, апетитний чай, настій трави полину гіркого, трави золототисячнику, кореня кульбаби та інших лікарських рослин), і такі, що переважно впливають на тканинний обмін, трофіку і процеси регенерації слизової оболонки шлунка (метил-урацил, натрію нуклеїнат, вітаміни, ферменти тощо).
З першого дня лікування призначають натуральний шлунковий сік по 1 столовій ложці на півсклянки води невеликими ковтками під час їди і поліферментні препарати (креон, панзинорм, фестал, абомін, мексаза) по 1 таблетці відразу після іди або під час їди. Застосування хлоридної кислоти у фазу загострення захворювання, особливо за наявності ерозій на слизовій оболонці шлунка, протипоказане.
Розведена хлоридна кислота і таблетовані препарати (ацидин-пепсин, бетацид, пепсидил, сальпепсин) призначають тільки після затухання гострих явищ запалення. Хворим на ХГ із секреторною недостатністю призначають стимулювальні (невеликі) дози хлоридної кислоти (10—15 крапель розведеної кислоти на півсклянки води під час іди), а хворим на ахлоргідрію - замісні (великі) дози хлоридної кислоти (20—40 крапель у поєднанні з пепсином по 0,5—1 г). У подальшому, після значного зменшення вираженості диспепсичних явищ замісну терапію можна припинити, враховуючи компенсаторні можливості системи травлення. Лише небагатьом хворим, переважно із супутнім панкреатитом і ентероколітом, потрібне тривале лікування ферментними препаратами.
Для посилення трофічних процесів у слизовій оболонці шлунка призначають препарати, які поліпшують мікроциркуляцію (нікошпан, нікотинамід, компламін, теонікол), синтез білка (метилурацил по 0,5 г 3 рази на день), репаративні процеси (екстракт алое, вітаміни групи В та аскорбінову кислоту, солкосерил по 2 мл 1—2 рази на день та ін.). Якщо порушення травлення і кишкового всмоктування первинно зумовлені ахілічним гастритом, супроводжуються анорексією і зниженням маси тіла, за умови виключення нео- бластичного процесу показане курсове лікування анаболічними стероїдами (ретаболіл, неробол, силаболін, феноболін). Процеси внутрішньоклітинного відновлення епітеліоцитів посилює кобаламід (до 300 мг на добу), який у поєднанні з модульованими струмами покращує не тільки гістологічну структуру слизової оболонки шлунка, а й гемодинаміку, нормалізує порушену рухову функцію.
Хворим на ХГ типу А недоцільно призначати антихолінергічні препарати, оскільки у них завжди наявна секреторна недостатність. У разі болю і виражених диспепсичних проявів внутрішньом’язово вводять метоклопрамід (церукал, реглан) — по 2 мл 0,5% розчину 2 рази надень; сульпірид (еглоніл, догматил) — по 2 мл 5% розчину 1—2 рази на день; но-шпу — по 2 мл 2% розчину 2 рази на день або галідор — 2 мл 2,5% розчину. У міру ліквідації гострих явищ переходять на пероральне вживання зазначених препаратів.
Замість антацидних засобів хворим на ХГ типу А призначають обволікальні і в’яжучі засоби рослинного походження, які мають також протизапальні властивості: настій листків подорожника по 1 столовій ложці або плантаглюцид у вигляді гранул по 0,5—1 г перорально 2—3 рази на день перед їдою протягом 3—4 тиж. Сприятливий ефект спостерігають і в разі застосування інших лікарських рослин: ромашки, деревію, м’яти, звіробою, валеріани (містять речовини протизапальної та протиспазматичної дії).
Перспективним для лікування хворих на ХГ типу А є сукральфат (антепсин, вентер, алсукрал) — по 1 г 3 рази на день у міжтравний період і на ніч протягом 2—3 тиж. Ці препарати мають протизапальні властивості, здатні посилювати репаративні процеси, їх можна застосовувати для мо- нотерапії ХГ.
Лікування рефлюкс-гастриту базується на потребі нейтралізувати подразну дію жовчі та її компонентів на слизову оболонку шлунка, забезпечити адекватне випорожнення шлунка або видалити з нього жовч. Рекомендують часте харчування невеликими дозами з індивідуальною дієтою; у разі демпінг-синдрому хворі іноді споживають їжу в положенні лежачи. Застосовують препарати, які прискорюють спорожнення шлунка (прокінетики): метоклопрамід (церукал, реглан), цизаприд (координакс, препульсид), домперидон (мотиліум), лоперамід (імодіум), перитол. Рекомендують засоби, які утворюють захисну плівку (цитопротектори): сукральфат (вентер), сафалкон, антациди (альмагель, маалокс, фосфалюгель, гастерин-гель та ін.), які не лише знижують кислотність шлунка, а й зв’язують жовчні кислоти і лізолецитин. Для переведення жовчі у водорозчинну форму, яка менше подразнює слизову оболонку шлунка, застосовують урсофальк або урсосан (препарати ведмежої жовчі). Періодично з профілактичною метою призначають вітаміни А, Е, С. Хворим зі змішаною формою гастриту (типи В і С) показана антигеліко- бактерна ерадикаційна терапія. У лікуванні НПЗП-індукованого гастриту ці препарати бажано відмінити, а якщо це неможливо, — використовувати селективні інгібітори ЦОГ-2 (мелоксикам, целебрекс та ін.) або комбінований препарат артротек (50 мг диклофенаку натрію і 0,2 мг мізопростолу).
Мізопростол є препаратом вибору в лікуванні хворих НПЗП-гастропатіями (призначають по 0,2 мг усередину 3 рази на день під час їди і перед сном). Цитопротекторну дію на слизову оболонку шлунка чинять також сукральфат і де-нол, хоча й меншою мірою, ніж мізопростол. У разі підвищеного кислотопродукування до комплексу лікування НПЗП-індукованого гастриту слід включити ІПН (омепразол, лансопразол, пантопразол, рабепразол, езомепразол).
Із фізіотерапевтичних методів використовують електрофорез новокаїну або дикаїну для тамування болю в надчеревній ділянці і помірні теплові процедури (грілка, парафінові чи озокеритові аплікації), а також діатермію на надчеревну ділянку. Однак слід пам’ятати, що деякі пацієнти погано переносять теплові процедури і діатермію (переважно хворі на ХГ з підвищеною секреторною функцією, в яких посилення кровообігу і трофічних процесів у тілі шлунка може сприяти підвищенню кислотно-пептичної активності).
У лікуванні хворих на ХГ велике значення має психотерапія. Лікар повинен сповістити пацієнту необхідні дані про хворобу, зокрема про принципи її лікування, переконати його у відносній безпеці захворювання. Останнє особливо важливе для пацієнтів похилого віку, оскільки в них нерідко спостерігають канцерофобію. Збудливим хворим показані седативні засоби (валеріановий чай, броміди, тазепам та ін.), а також загальний електрофорез брому за Вермелем, електросон.
Широко застосовують у лікуванні хворих на ХГ оксигенотерапію (кисневий намет і киснева піна).
Мінеральні води хворим на ХГ призначають з урахуванням рівня кислотопродукування:
• хворим з підвищеною секреторною функцією шлунка рекомендують мінеральні води малої, рідше середньої мінералізації, переважно кислі (бере- зівська, боржомі, єсентуки № 20, нарзан, луганська, поляна квасова, слов’янська, смирновська) по 1 склянці швидко, великими ковтками, 3—4 рази на день за 1—1,5 години до їди; температура води 38—45 °С;
• у разі нормального кислотопродукування — ті самі мінеральні води слід пити по 1 склянці повільно, невеликими ковтками, 3—4 рази на день за 45-60 хв до їди; температура води 28—40 ’С;
• при зниженому кислотопродукуванні в шлунку призначають мінеральні води високої мінералізації (єсентуки № 4 і 17, миргородська, куяльник 6) по 1-1,5 склянки, повільно, великими ковтками, 3—4 рази на день, за 15—30 хв до іди, температура води 18—25 "С.
Курортне лікування подовжує фазу ремісії, тому воно показане всім хворим на ХГ у стадії ремісії, за винятком тих випадків, коли діагноз викликає сумніви і не можна повністю виключити рак шлунка.
В Україні для лікування хворих на ХГ використовують широко відомі курорти: Березівські Мінеральні Води, курорти Закарпаття (санаторії "Поляна", "Шаян" та ін.), Прикарпаття (Моршин, Трускавець), Миргород тощо. Можна рекомендувати хворим лікування в Єсентуках, Желєзноводську, Боржомі, Друскінінкаї.
Профілактика ХГ пов’язана з модифікацією способу життя (відмова від паління, надмірного вживання алкоголю), раціональною організацією харчування, запобіганням інфікуванню HP, безпечним застосуванням за наявності показань НПЗП. У раціоні осіб, схильних до надмірної секреції, слід обмежити сокогінні страви і періодично проводити курси антацидної терапії. Для запобігання формам ХГ, пов’язаним із впливом ендогенних чинників, необхідно систематично і своєчасно лікувати основне захворювання. Вторинна профілактика спрямована на недопущення рецидивів захворювання і зводиться до раціонального лікування загострення ХГ.
Профілактика НПЗП-гастропатій полягає у виявленні осіб, які мають великий ступінь ризику розвитку цієї патології, з метою обмежити застосування ними даної групи препаратів, домогтися нормалізації способу життя, дотримання режиму харчування, виключити шкідливі впливи на шлунок (паління, міцні алкогольні напої тощо).
Працездатність
Хворим на ХГ легкого ступеня, без порушень секреторної функції, коли больовий і диспепсичний синдроми виражені нерізко, рекомендована робота, не пов’язана зі значним фізичним напруженням, яка дозволяє дотримуватись дієтичного режиму харчування.
Хворим на ХГ із середньою тяжкістю перебігу доступна робота з помірним фізичним і нервово-психічним напруженням, яка дозволяє в повному обсязі дотримуватися рекомендацій щодо харчування. Протипоказана робота в складі експедицій, геологорозвідувальних партіях, у нічну зміну, у гарячих цехах. Виключається контакт зі свинцем, ртуттю, заковтування парів основ, вугільного і бавовняного пилу та ін. Хворі за висновком JIKK можуть бути переведені на іншу роботу.
Для хворих на ХГ тяжкої форми з ознаками атрофії слизової оболонки, різко вираженою секреторною недостатністю до викладених вище протипоказань слід додати переохолодження, вібрацію, контакт з фосфором, що значно звужує коло доступних професій.
Диспансеризація
Диспансерне спостерігання за хворими на ХГ — важливий чинник у профілактиці різних ускладнень. Хворим на ХГ забороняють вживати алкогольні напої і палити. У комплексі реабілітаційних заходів велике значення має санаторно-курортне лікування (див. вище). Хворих на ХГ обстежують не рідше ніж 2 рази на рік. Протирецидивне медикаментозне лікування також проводять 2 рази на рік тривалістю 3—4 тиж в осінньо-весняний період. З диспансерного обліку хворих знімають через 3 роки після останнього загострення.
Постійному диспансерному спостеріганню підлягають хворі з формами ХГ, які відносять до передракових станів: ригідний антральний гастрит, фундальний гастрит типу А, гастрит перебудови за кишковим типом (кишкова метаплазія), атрофічно-гіперпластичний гастрит, хвороба Менетріє, гастрит при анемії Аддісона—Бірмера, поліпозний гастрит, медіогастральні виразки на тлі вираженого антрального гастриту.
Прогноз у хворих на ХГ за умови ранньої діагностики і раціонального лікування добрий. Прогноз погіршується в разі прогресування ХГ типу А, у хворих на атрофічний пангастрит у зв’язку з розвитком В12-дефіцитної анемії, секреторної недостатності шлунка і пов’язаних з нею порушень кишкового травлення і всмоктування, а також у разі трансформації передракових станів шлунка в рак.
Подальша інформація
Завжди консультуйтеся зі своїм лікарем, щоб переконатися, що інформація, яка відображається на цій сторінці, може бути застосована до ваших особистих обставин. Інформація призначена тільки для медичних фахівців.