Эпидемиология и этиология
Врожденные пороки сердца (ПВС) - это аномалии структуры и (или) функции сердечно-сосудистой системы, возникающих вследствие нарушения ее эмбрионального развития.
Эпидемиология. ПВС встречаются примерно в 1% младенцев, родившихся живыми. В это число не входят две распространенные аномалии - прирожденный нестенозований двустворчатый аортальный клапан и пролапс митрального клапана. У взрослых частота ПВС - около 0,2%. Это обусловлено тем, что только 10-15% детей, преимущественно с более легкими нарушениями без выраженных нарушений гемодинамики, достигают юношеского возраста без хирургической коррекции. Вследствие этого у взрослых чаще всего встречаются дефект межпредсердной перегородки, некоторые варианты дефекта межжелудочковой перегородки и стеноз устья легочной артерии, реже - открытый артериальный проток, коарктация аорты и недостатки тетрады Фалло.
Этиология ПВС обусловлена взаимодействием генетических факторов и факторов внешней среды. В клинике установлена связь их возникновения с корью, реже - другими вирусными инфекциями, хроническим злоупотреблением алкоголем и употреблением некоторых лекарств (талидомида и др..). В семейных случаях преобладает аутосомно-рецессивный тип наследования, но может случаться и доминантный.
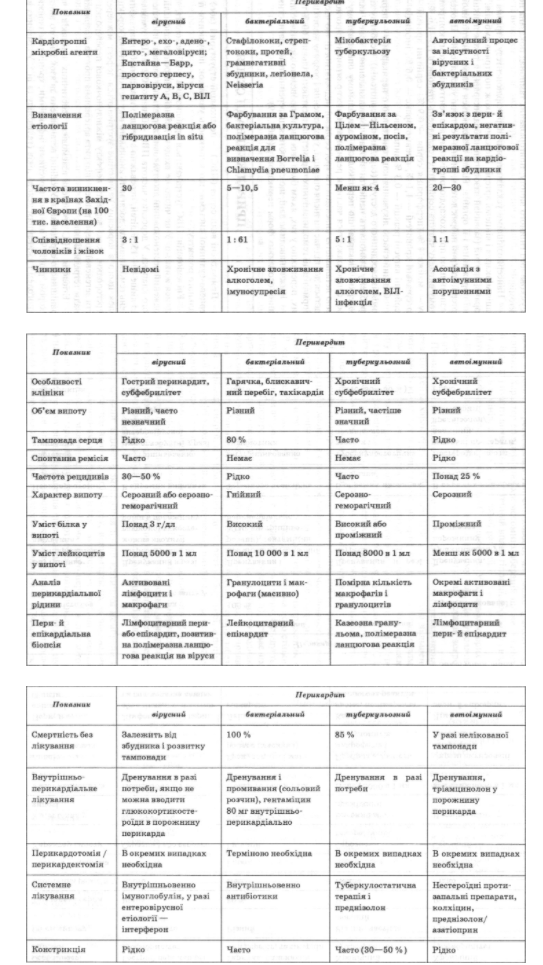
Таблица 19
Дифференциальная диагностика и лечение особых форм перикардита
Характер специфических хромосомных аберраций еще не установлен. В эксперименте выявлено тератогенное влияние гипоксии, дефицита и избытка некоторых витаминов, а также ионизирующей радиации.
Пато-и морфогенетические механизмы ПВС у взрослых . У многих больных с ПВС жалобы появляются в юношеском и даже зрелом возрасте. Это обусловлено прогрессированием функциональных и морфологических изменений сердца и сосудов, в частности таких:
1. Повышение легочного сосудистого сопротивления. Артериальная (прекапиллярных) легочная гипертензия характерна для многих ПВС. Она обусловлена увеличением легочного кровотока и сопротивления легочных артериол сначала через спазм, а затем - вследствие прогрессивного склероза с тромбозом и облитерацией просвета под влиянием полицитемии, гипоксемии и ацидоза. Высокая легочная гипертензия с резким повышением легочного сосудистого сопротивления у больных с ПВС с наличием патологического сообщения между большим и малым кругом кровообращения, что приводит к возникновению право-левого, т.е. вено-артериального выброса крови и появления цианоза, называется синдромом Эйзенменгера.
2. Преобразование гипертрофии миокарда с компенсаторной в патологическую. Развитие гипертрофии миокарда является важнейшим механизмом долговременной адаптации сердца к хроническому перегрузки объемом или сопротивлением. Гиперфункция миокарда из-за повышения его систолического напряжения в (о = Р х r/2h, где Р - давление, г - радиус желудочка и h - толщина его стенки) активизирует генетический аппарат мышечных клеток, вследствие чего у них увеличивается синтез белков. Гипертрофия, развивающейся (увеличение h), устраняет эту гиперфункции, и напряжение стенки нормализуется. Это не означает, однако, что функциональные возможности гипертрофированной мышечной ткани действительно нормальные. В гипертрофированном миокарде нарушаются процессы энергообеспечения и утилизации энергии, что приводит к развитию обратимой, а затем и необратимой дистрофии кардиомиоцитов, увеличение удельной плотности интер-стициального фиброза и заместительного склероза.
Основные механизмы
Основные механизмы развития недостаточности гипертрофированного миокарда:
а) на органном уровне: уменьшение плотности симпатической иннервации сердца, что приводит к нарушению сократимости и расслабления миокарда
б) на уровне ткани: уменьшение коронарного резерва в состоянии покоя из-за отставания роста капилляров от увеличения массы кардиомиоцитов и увеличения диффузной расстояния для кислорода
в) на уровне клетки: относительное уменьшение площади клеточной мембраны и, следовательно, мощности систем ионного транспорта, ответственных за сочетание возбуждения с сокращением и расслаблением, уменьшение соотношения количества митохондрий и миофибрилл вследствие короткого периода жизни митохондрий, нарушает энергообеспечения гипертрофированного миокарда
г) на молекулярном уровне: увеличение соотношения между легкими, живут долго, и тяжелыми, что живут недолго (кратко), цепями в головках молекул миозина миофибрилл, что приводит к снижению АТФазного активности и вследствие этого - скорости превращения химической энергии АТФ в механическую.
3. Развитие кальциноза пораженных клапанов.
4. Разрыв хорд измененных клапанов, который увеличивает их дисфункцию.
Физиологической реакцией организма на хроническую гипоксемию является эритроцитоз, что особенно характерно для "синих" ПВС и может достигать 6-7 • 10 И2 /л. Он способствует улучшению доставки кислорода к тканям, что сопровождается, однако, резким повышением вязкости крови. Послнэ часто приводит к тромбозам в различных органах, в том числе в легких и уменьшения клубочковой фильтрации в почках.
Больные с ПВС, как и с приобретенными пороками сердца (НВС), имеют повышенный риск заболеть инфекционный эндокардит (эндартериит). Это обусловлено хронической травматизацией эндокарда (эндотелия) турбулентным кровотоком, сопровождается отложением на нем тромботических масс и создает благоприятные условия для оседания микроорганизмов при транзиторной бактериемии.
Классификация ПВС
Анатомические классификации ПВС очень громоздки и непригодны для практического применения. Практически больных с ПВС зависимости от легочного кровотока делят на 3 группы: 1) с неизмененным легочным кровотоком (стеноз устья аорты, коарктация аорты и др..) 2) с увеличенным кровотоком (дефекты межпредсердной и межжелудочковой перегородок, открытый артериальный проток и др.). , 3) с уменьшенным легочным кровотоком (стеноз устья легочной артерии, тетрада и триада Фалло и др..). Эта классификация, однако, весьма условна. Так, в поздних стадиях дефектов перегородок сердца при развитии высокой легочной гипертензии направление выброса крови может измениться и легочный кровоток уменьшится. У части больных с тетрадой Фалло в случае незначительной выраженности стеноза легочной артерии кровоток в малом круге кровообращения не изменен.
В клинической практике ПВС разделяют на "белые", или ацианотични, и "синие", сопровождающиеся цианозом. Такое разделение также довольно относителен, так как естественное развитие некоторых "белых" пороков предусматривает их трансформацию в "синие" (например, синдром Эйзенменгера).
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.