Факторы риска
Токсическая нефропатия - функциональные или /и морфологические изменения почек, вызванные фармакологическими, химическими или биологическими агентами, которые поступают в организм (через рот, дыхательные пути, во время инъекций и т.п.).
Острая токсическая нефропатия чаще всего возникает при острых экзогенных отравлений хлорированными углеводородами, уксусной эссенцией, этиленгликолем, соединениями тяжелых металлов. Кроме нефротоксического действия эти вещества обладают гепатотоксические и гемолитические свойства и могут приводить к острой почечной недостаточности и шока.
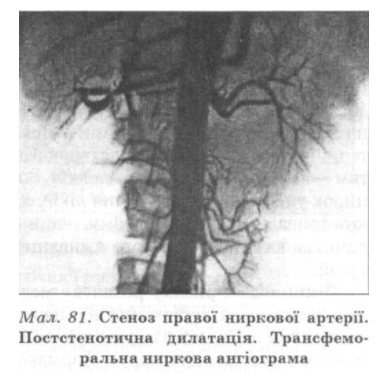
По легкой степени нефропатии наблюдают лишь незначительные изменения в моче - небольшую протеинурию, эритроцитурией, - что исчезают в течение нескольких дней под влиянием антидотной и дезинтоксикационной терапии.
Применение различных лекарственных средств в практической медицине может вызывать различные клинические синдромы: острую и хроническую почечную недостаточность, гломерулярные и тубулоинтерстициальные поражения почек, нарушение водно-электролитного обмена. Некоторые из них часто имеют обратный характер, иногда приобретают признаки заболеваний почек, объединенных общим понятием - медикаментозная нефропатия. Она составляет 10-20% всех заболеваний почек вследствие применения лекарств, которые выводятся преимущественно почками и имеют длительный контакт с их тканями. Иногда медикаментозная нефропатия возникает уже после первого употребления лекарственного средства вследствие идиосинкразии.
Факторами риска развития лекарственной нефропатии является отсроченные аллергические заболевания или наличие аллергических реакций; одновременное применение лекарств, которые взаимодействуют между собой, нарушение функции почек, модулирующего фармакодинамику и фармакокинетику лекарственного средства вследствие болезни почек или у людей старшего возраста; нефротоксичность лекарственных препаратов.
Развитие медикаментозной нефропатии обусловлен также спецификой почечного кровотока (25% сердечного выброса), метаболической и транспортной функцией канальцевых клеток с многочисленными ферментными системами, большой поверхностью эндотелия.
Механизмы нефротоксического действия лекарственных препаратов сводятся к трем основным вариантам:
• прямая нефротоксическое действие препаратов (блокада внутриклеточных метаболических и транспортных процессов)
• развитие иммунных реакций клеточного или гуморального типа, в том числе аллергических
• влияние на почечную гемодинамику и гормональную регуляторную систему почек.
Лекарственные средства вызывают различные поражения почек: острый канальцевый некроз и развитие ОПН, острый и хронический интерстициальный нефрит, острый и хронический медикаментозный гломерулонефрит, некроз почечных сосочков с рецидивами острой почечной недостаточности; двусторонний кортикальный некроз, внутришньоканальцеву обструкцию, поражения мочевых путей (нефролитиаз, нефрокальциноз, геморрагический цистит), ретроперитонеальный фиброз; функциональную почечную недостаточность. Ниже приведены поражение почек вследствие применения лекарственных препаратов.
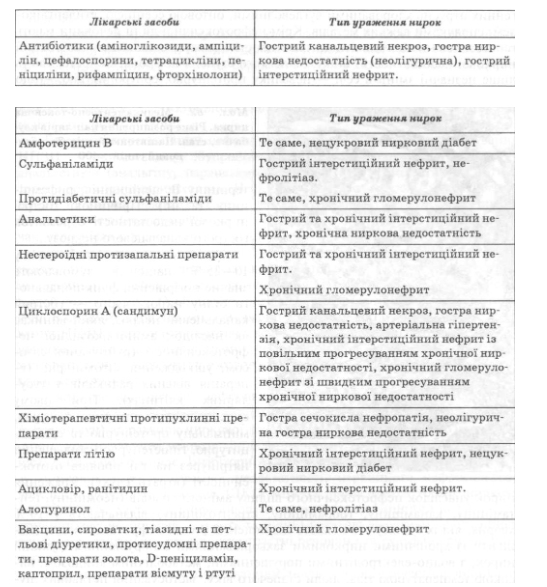
Чаще медикаментозные нефропатии возникающие при применении анальгетиков, антибиотиков, сульфаниламидов, вакцин и сывороток, НПВП, мочегонных средств, витаминов, рентгеноконтрастных веществ, химиотерапевтических противоопухолевых препаратов, иммунодепрессантов, фторированных анестезивних средств и т.п. .
Острые медикаментозные поражения почек на фоне терапевтических доз препаратов клинически проявляются снижением функции почек вследствие нарушений гемодинамики (артериальная гипертензия или гиповолемия, которые наблюдают при лечении диуретиками, гипотензивными препаратами) вплоть до развития острой почечной недостаточности, которая в большинстве случаев является спонтанно обратной, однако некоторые больные с олигурией требуют гемодиализа.
Чаще к возникновению острой почечной недостаточности приводит применение антибиотиков (аминогликозидов, ампициллина, цефалоспоринов, тетрациклинов, амфотерицина В, пенициллинам, рифампицину и др..). Причиной острой почечной недостаточности является развитие острого канальцевого некроза.
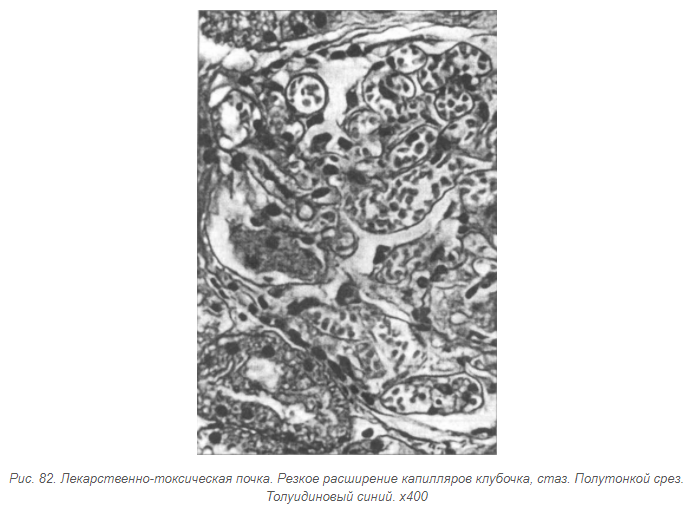
Аминогликозидные антибиотики в 10-25% пациентов обусловливают значительное ухудшение функционального состояния почек, часто - острый канальцевый некроз, который возникает как следствие Аминогликозидный нефротоксичности (разрушение лизосом , повреждения митохондрий, генерация свободных радикалов в тубулярных клетках). При этом наблюдают умеренную олигурии, минимальную протеинурию и эритроцитурией, гипостенурию и увеличенный натрийурез на фоне проявлений ототок-сичности (потери слуха). Поражение почек вследствие нефротоксического влияния аминогликозидов (неомицин??, Гентамицина, канамицина, тобрамицина, стрептомицина) отмечают у 10% больных, которые их получают и имеют повышенный риск нефротоксичности (пациенты с хроническими почечными заболеваниями с нарушением функций почек, водно-электролитными нарушениями, метаболическим ацидозом, высокой температурой тела, люди старческого возраста, применение петлевых диуретиков, блокаторов кальциевых каналов, цефалоспоринов, рентгеноконтрастных веществ) (рис. 82).
Острый интерстициальный нефрит чаще всего развивается в результате лечения антибиотиками (тетрациклинами, пенициллином, полусинтетическими пенициллинами, рифампицином, цефалоспоринами, фторхинолонами), сульфаниламидами. Первые признаки острого интерстициального нефрита могут появиться как через несколько дней, так и через несколько недель антибактериальной терапии. Клинически острый интерстициальный нефрит проявляется полиурией, умеренной тубулярный или смешанной протеинурией, эритроцитурией, Абактериальный лейкоцитурии, нарастанием азотемии (неолигуричнои ОПН). Повышенный натрийурез приводит к развитию состояния потери соли (артериальной гипотонии, дегидратации, метаболического ацидоза). Больные жалуются на резкую мышечную слабость, приступы ортостатической коллапса. Развитие канальцевого ацидоза приводит гиперкалиемию, что требует срочных врачебных мероприятий. В тяжелых случаях могут развиться некротический папиллит и синдром Фанкони.
Острый интерстициальный нефрит
Острый интерстициальный нефрит может возникать вследствие применения НПВП - индометацин, ибупрофен, вольтарен, пироксикам, реже - анальгетиков (анальгина, парацетамола, фенацетина, фенилбутазона, ингибиторов простагландинсинтетазы). Нефропатия возникает у лиц, употребляющих НПВП на фоне заболеваний и состояний, характеризующихся пониженной почечной перфузией (болезни печени, особенно цирроз, системная красная волчанка, состояние после оперативного вмешательства, алкоголизм, при гиповолемии и гипонатриемии, состояниях, которые могут быть вызваны применением диуретиков , сердечной недостаточностью, артериальной гипертензией). Чаще всего острый интерстициальный нефрит вследствие лечения НПВП наблюдают у женщин и пожилых людей. Особенностью его клинического течения является значительная протеинурия. В отдельных случаях гемодинамические сдвиги, которые бывают при употреблении НПВП (задержание натрия и воды, снижение почечного кровотока и скорости клубочковой фильтрации), приобретают выраженный характер и могут дать толчок развитию острого кортикального некроза и острой почечной недостаточности.
Острые медикаментозные нефропатии с острой почечной недостаточностью возникают и в случае применения других лекарственных препаратов. Циклоспорин А (сандимун) за счет почечной вазоконстрикции вызывает развитие острого кортикального некроза, иногда - обратную ОПН, которая быстро проходит. Ингибиторы АПФ, обычно на фоне двустороннего стеноза почечных артерий, сердечной недостаточности, первичного нефросклерозу вследствие значительного снижения СКФ могут вызывать острую почечную недостаточность. Способность вызывать острый интерстициальный нефрит и ОПН имеют тиазидные и петлевые диуретики, аллопуринол, ацикловир, ранитидин, рентгеноконтрастные вещества и сульфаниламидные препараты.
Нефропатия, связанная с употреблением анальгетиков, чаще возникает у женщин старше 40 лет, составляет от 2 до 25% всех заболеваний почек, которые заканчиваются ХПН (анальгетическое нефропатия) . У 80% больных диагностируют некротизивний папиллит, который может привести к обструктивной ОПН, но в большинстве из них нефропатия имеет бессимптомное течение или развивается хронический интерстициальный нефрит, который морфологически имеет признаки тубулоинтерстициального поражения, а также характеризуется некрозом сосочков и микроангионефропатиею, трансформируется в склероз сосудов. Механизм поражения почек анальгетиками связан с прямым токсическим воздействием анальгетиков на мозговой слой почек, угнетением синтеза простагландинов, нарушением процессов окисления в эпителии канальцев т.д.. Клинически медикаментозная нефропатия, вызванная употреблением анальгетиков, проявляется мочевым синдромом с умеренной протеинурией, эритроцитурией и Абактериальный лейкоцитурии. У 25% больных анальгетической нефропатией наблюдают лейкоцитурию, связанную с присоединением инфекции мочевых путей. Появление гематурии свидетельствует о некроз сосочков, а ее устойчивый характер - о развитии карциномы почек. Значительная протеинурия при анальгетической нефропатии может развиться вследствие поражения клубочков, чаще всего в виде фокально-сегментарного гломерулосклероза. Часть больных жалуются на мышечную слабость и судороги, обусловленные развитием канальцевого ацидоза, в некоторых лиц наблюдают закисление мочи с последующей кальцификацией почек, образованием камней и развитием остеодистрофии. Все пациенты жалуются на жажду и выраженную полиурию.
Для больных хронический интерстициальный нефрит, вызванный анальгетиками, характерна артериальная гипертензия, может иметь злокачественный характер и стать причиной развития острой почечной недостаточности. Заболевание прогрессирует медленно. Анальгетическое нефропатия сопровождается признаками поражения других органов и систем: рецидивирующим стоматитом, язвой желудка, анемиями различного генеза, генерализованным атеросклерозом и ИБС,поражением кожи (повышенная пигментация), нервно-психическими расстройствами (головная боль, расстройства личности, психозы и т.п.), преждевременным старением. Лечение начинается с отмены анальгетического средства и заключается в назначении обильное питье, коррекции электролитных нарушений.
Сандимунова нефропатия - хронический интерстициальный нефрит, развивающийся в пересаженной почке или в почках лиц, которым трансплантирована сердце, печень. Обычно эта нефропатия возникает у людей, получающих высокие дозы препарата (10-15 мг на 1 кг массы тела), реже - при употреблении низких доз сандимуну (5 мг на 1 кг массы тела). Нефротоксичность цитостатического средства заключается в прямой повреждающему действию его на эндотелий сосудов почек и тромбоциты, сужении под его влиянием приносящих артериолы клубочка, развития апоптоза клеток канальцевого эпителия и интерстициального фиброза. Значительную роль играет объем - натрийзалежна гипертензия, которая формируется на фоне длительного применения сандимуну, гиперурикемия и другие метаболические нарушения. Несмотря на раннее развитие сандимуновои нефропатии (2-4-й год лечения) с артериальной гипертензией и прогрессивным интерстициальным фиброзом, хроническая почечная недостаточность прогрессирует медленно. Быстрый и прогрессивный течение хронической почечной недостаточности свидетельствует о поражении клубочков, чаще всего в виде фокально-сегментарного гломерулосклероза. Факторами развития последнего является высокая некорегована гипертензия и значительная протеинурия.
Важными профилактическими мерами для предотвращения развития сандимуновои нефропатии является назначение средних или малых доз препарата, применение блокаторов кальциевых каналов, предсердного натрийуретического пептида. Похожую нефропатию вызывает лечение такролимусом - цитостатиками, который используется в трансплантологии.
Хроническая токсическая нефропатия, которая может возникнуть в случае применения препаратов лития у пациентов с психическими заболеваниями и диффузным токсическим зобом, а также на фоне применения амфотерицина В или дифенилгидантоина, проявляется развитием несахарного почечного диабета за счет накопления препаратов в клетках собирательных трубочек, взаимодействия с циклического аденозинмонофосфата (цАМФ), что приводит к дисрегуляции транспорта воды антидиуретическим гормоном (АДГ).
нефротоксического эффекта многих веществ связан с образованием метгемоглобина. Ниже приведены агенты, обусловливающие образование метгемоглобина.
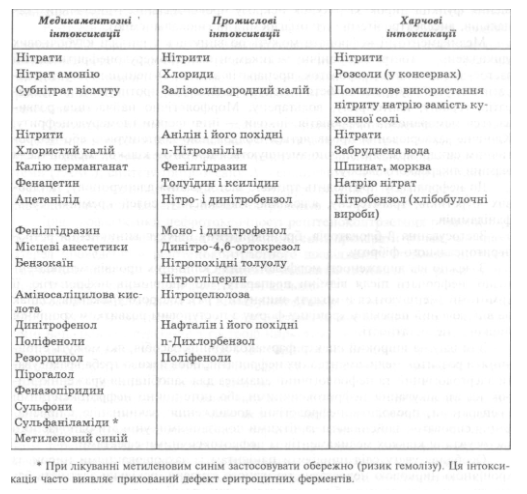
Медикаментозная нефропатия
Медикаментозная нефропатия иногда возникает после применения вакцин и сывороток у лиц с заболеваниями почек или склонных к аллергическим реакциям, особенно в случае использования поливалентных препаратов, а также вследствие употребление химиотерапевтических противоопухолевых препаратов (цисплатина, метотрексата и др.)., на фоне чего возникает гиперурикемия и повышается экскреция мочевой кислоты. Кристаллы мочевой кислоты, которые плохо растворяются, вызывают обтурацию дистальных канальцев и собирательных трубочек, что часто приводит к неолигуричнои ОПН. Для профилактики возникновения нефропатии при лечении противоопухолевыми препаратами нужно поддерживать высокую скорость мочеиспускания (употребление большого количества щелочных напитков для поддержания рН мочи более 7,0), назначать аллопуринол в дозе 300-600 мг в сутки. Цисплатин - химиотерапевтический препарат, нефротоксичность которого зависит от дозы. Наблюдают нарушения функции почек за счет некроза проксимальных и дистальных канальцев, диселектролитемию (гипомагниемия и гипокальциемия).
Медикаментозные нефропатии могут развиться в виде клубочковых повреждений - острые и хронические медикаментозные гломерулонефриты на фоне применения вакцин, сывороток, препаратов золота, D-пеницилламину, препаратов висмута и ртути, антидиабетических сульфаниламидов, противосудорожных препаратов, героина, каптоприла, вольтарен. Морфологически чаще всего развивается Мембранозная нефропатия, иногда - другие формы гломерулонефрита. Клиническое заболевание проявляется изолированной протеинурией или нефротическим синдромом, значительно уменьшаются в течение нескольких месяцев после отмены лекарственного средства.
В нефролитиаза приводит длительное применение аллопуринола, петлевых диуретиков, триамтерена, алюминия гидрокисиду, солей кремния, сульфаниламидов.
Применение (С-блокаторов, бромокриптина индуцирует возникновения ретро-перитонеального фиброза.
зависимости от выраженности морфологических и клинических проявлений медикаментозной нефропатии после отмены препарата, вызвавшего нефропатию, ее симптомы уменьшаются и могут исчезнуть в случае острого поражения. Однако не исключен переход в хроническую форму с постепенным развитием хронической почечной недостаточности.
Учитывая широкий спектр фармакологических средств, которые могут вызвать развитие медикаментозных нефропатий, обязательно надо учитывать аллергологический и нефрологический анамнез для предотвращения поражения почек на фоне лечения нефротоксичными или потенциально нефротоксичными препаратами, проводить нефрологические исследования; вакцинацию и назначения сывороток осуществлять по четким показаниям; избегать одновременного применения нескольких меди?? Аменти с нефротоксичными эффектами.
Особое внимание следует уделять пациентам с заболеваниями почек, с хронической почечной недостаточностью различной степени, поскольку способность многих лекарств связываться с белками плазмы при уремии ниже, чем у здоровых, а степень этого нарушение пропорционален степени почечной недостаточности. Увеличение фракции несвязанного лекарственного средства может усилить фармакологический, в частности нефротоксический, эффект введенной дозы препарата. При хронической почечной недостаточности в крови накапливаются активные метаболиты лекарственных средств, которые не выводятся почками. В случае первых проявлений нефротоксичности медикаментозное средство следует отменить, провести симптоматическую (диуретики, гипотензивные, дезинтоксикационные препараты в виде инъекций, ретроградное промывание мочевых путей и т.д.) и противоаллергическое (антигистаминные средства, кортикостероиды) терапию. Установлено, что риск нефротоксичности крупнейший в пожилых людей, при хронической недостаточности кровообращения и циррозе печени, хронических заболеваниях почек в стадии хронической почечной недостаточности, различных заболеваниях, сопровождающихся нарушениями обмена (сахарный диабет, подагра, гиперлипидемия), при алкоголизме и наркомании.
Рентгеноконтрастные вещества относятся к редким причинам медикаментозной нефропатии, которая обычно проявляется обратной ОПН. Однако опасность ее возникновения существенно повышается у пациентов с острыми и хроническими заболеваниями почек, желтухой, сахарным диабетом. Непосредственным провокационным фактором часто бывает гиповолемия.
Ведущий механизм нефротоксичности рентгеноконтрастных веществ - нарушение почечной гемодинамики (вследствие вазоконстрикции и гипоксии мозгового слоя почек через активацию ренин-ангиотензин-альдостероновой системы (РААС), синтеза тромбоксана и эндотелина), а также прямое токсическое повреждение канальцевого эпителия, гиперурикозурия и гипероксалурия с последующей внутришньоканальцевою обструкцией.
Для профилактики нефротоксичности рентгеноконтрастных веществ следует применять низькоосмолярни неионогенных препараты (гипак, омнипак). Перед проведением рентгеноконтрастного исследования целесообразно провести гидратацию путем введения изотонического раствора натрия хлорида, назначить антагонисты кальция.
Острый медикаментозный гломерулонефрит развивается после введения вакцин и сывороток, пенициллина, сульфаниламидов, амфетамина, героина; в части случаев он протекает с острой почечной недостаточностью, нередко - с очаговым некрозом клубочков и вероятностью хронизации . Описаны случаи быстрого прогрессирования гломерулонефрита после длительного употребления гидра-лазину при лечении D-пеницилламином.
При дифференциальной диагностике медикаментозных поражений почек, протекающих с острой почечной недостаточностью, важное установить сам факт медикаментозной ОПН, так как основным терапевтическим вмешательством является отмена препарата (хотя при аллергических нефритах может быть эффективным назначение высоких доз преднизолона). Главными дифференциально-диагностическими признаками могут быть следующие:
• диурез при острой почечной недостаточности и остром интерстициальный нефрит обычно сохранен (неолигурична ОПН), при остром гломерулонефрите и обструкции мочевых путей часто обнаруживают олигурии - анурию
• экскреция Na + при канальцевом некрозе и интерстициальный нефрит обычно повышена (низкое содержание Na + в моче свидетельствует о том, что препарат не имеет прямой тубулотоксичнои действия)
• при остром интерстициальный нефрит часто развиваются другие экс-траренальни признаки гиперсенсибилизации: повышение в крови уровня Иммуноглоб-на Е, сенсибилизация Т-лимфоцитов крови к лекарственным препаратам
• выраженная протеинурия характерна для острого гломерулонефрита
• следует оценивать характер лекарственного препарата и иметь представление об основной механизм его действия.
В случае хронического употребления алкоголя может развиться иммунокомплексный нефрит, вызванный образованием комплексов, состоящих из алкогольного гиалина и антител, принадлежащих к классу иммуноглобулинов А. Морфологически для него характерен мезангиопролиферативный нефрит с выраженным тубулоинтерстициального компонентом. Алкогольный нефрит протекает латентно с небольшой протеинурией, безболезненной эритроцитурией, а иногда и гематурией, повышением уровня иммуноглобулина А в сыворотке крови. У части больных отмечают гиперурикемией. Нефротический синдром развивается редко. Артериальная гипертензия возникает поздно и обычно бывает умеренной. Рано снижаются концентрационная функция почек и клубочковая фильтрация. Процесс прогрессирует медленно и хроническая почечная недостаточность развивается через 10 лет, а то и позже, и только у 30-40% больных, а в случае воздержания от дальнейшего употребления алкоголя возможен обратное развитие процесса. Его обострение вызывает обычно употребления алкоголя. Диагноз алкогольного нефрита основывается преимущественно на анамнестических данных и наличия алкогольного поражения других органов и систем - панкреатита, гепатита, цирроза печени, поражения миокарда, пол?? Невропатии. Тяжесть клинических проявлений зависит от длительности алкоголизма. Нужно проводить дифференциальную диагностику с заболеваниями, сопровождающимися выраженной эритроцитурией или гематурией. Основным лечебным мероприятием является как можно раньше прекращения употребления любых алкогольных напитков.
Существует также связь между злоупотреблением героином и иммунокомплексным гломерулонефритом и рабдомиолизом, вследствие чего развивается хроническая почечная недостаточность.
У рабочих, занятых на производстве, связанном с воздействием нефротоксических веществ - тяжелых металлов (свинец, никель, кобальт, медь, висмут, золото и др.)., нефтепродуктов, четыреххлористого углерода, антифриза, диеты-ленгликолю т.п., а также у крестьян, которые имеют дело с ядохимикатами и инсектицидами, также нередко развивается токсическая нефропатия. Риск ее возникновения и скорость прогрессирования напрямую зависят от продолжительности контакта с этими ядовитыми веществами и степени загрязненности ими производственных помещений, почвы и атмосферы. Они поступают в организм преимущественно через органы пищеварения и дыхания, реже - через кожу.
Большинство тяжелых металлов накапливается в проксимальных отделах нефронов в связи с их транспортировкой или наличием участков связывания, например сульфгидрильных (SH) групп. Токсическое действие свинца наблюдается при пищевых отравлениях, промышленных воздействиях, употреблении загрязненной воды, вина или других алкогольных напитков, на горнорудных предприятиях, при вдыхании дыма или продуктов сгорания бензина со свинцовыми добавками. Тетраэтилсвинец проникает через интактную кожу и легкие. Хроническое свинцовое отравление проявляется сморщенными почками, уремией, артериальной гипертензией, анемией с базофильной зернистостью, энцефалопатией, периферийной невропатией и синдромом Фанкони. При остром отравлении возможен спастические боли в животе (свинцовая колика).
Среди биологических факторов, приводящих к развитию токсической нефропатии, важнейшее значение имеют грибы, яды змей, укусы насекомых, афлатоксин.
Почти при всех токсичных нефропатиях поражаются преимущественно канальцы и интерстициальная ткань почек по типу хронического интерстициального нефрита, вместе с изменениями других органов и систем организма определяет в каждом конкретном случае клиническую картину заболевания.
Ранние признаки, позволяющие заподозрить токсическое нефропатию, обусловленные нарушением функции почек. Снижаются почечный плазмотик и клубочковая фильтрация, увеличивается экскреторная фаза ренограмы. Впоследствии, обычно после многолетнего контакта с токсинами, наблюдают отклонения в пробах Зимницкого. Появляются никтурия, полиурия и изогипостенурия. В моче обнаруживают следы белка, в случае количественного исследования мочевого осадка - небольшую эритроцитурией и цилиндрурия.
Лечение. Токсические нефропатии вследствие острых отравлений при тяжелом течении нуждаются в неотложной помощи с учетом вида этиологического фактора, характера поражения почек и их функционального состояния. На начальном этапе особенно важно провести антидотного терапию и форсированное удаление токсических веществ из организма. С этой целью назначают внутримышечно унитиол из расчета 1 мл 5% раствора на 10 кг массы тела через 6-8 ч в течение 1-х суток, через 8-12 ч - в течение 2-х суток и еще 5 дней по 1-2 инъекции в сутки. Этот препарат достаточно эффективен при отравлении препаратами ртути, мышьяка, золота. Его применяют также для нейтрализации токсического воздействия меди, хрома, висмута, никеля, кобальта, полония, телурию и др..
Для обезвреживания действия большинства металлов применяют комплексоны, например кальций-динатриевая соль этилендиаминтетрауксусной кислоты. Вводят по 20 мл 10% раствора в 500 мл изотонического раствора натрия хлорида или 5% раствора глюкозы внутривенно капельно, повторно - до 40 мл в сутки в течение 3-4 суток. При отравлении растворимыми соединениями свинца, фосфора, ртути, фтора вводят натрия тиосульфат (30% раствор по 30-50 мл внутривенно). Полезно употреблять этиловый спирт (30% раствор по 50-100 мл внутрь через 3-4 ч до состояния легкого опьянения), если причиной токсической нефропатии был этиленгликоль или метиловый спирт.
Если токсин попал в пищеварительный канал, нужно промыть желудок и кишки, использовать послабляющие средства, энтеросорбенты. При сохраненной водовидильнои функции почек надо форсировать диурез под тщательным контролем водного баланса. В случае уменьшения диуреза при острой почечной недостаточности в одигоануричний стадии применяют гемодиализ, перитонеальный диализ, гемосорбцию, замещения крови и весь комплекс лечебных мероприятий, рекомендованных при токсической нефропатии и его опасных осложнениях.
Лечение хронических токсических нефропатий заключается прежде всего в прекращении контакта с токсинами. Нужно полноценное питание, обогащенное витаминами, особенно аскорбиновой кислотой. Для повышения выделение токсинов назначают растительные мочегонные средства, не раздражающие паренхиму почек, - цветки и листья земляники, ежевики, брусники, хвощ полевой, черноплодная рябину, кукурузные рыльца и др.. Рекомендуют также пектин, энтеросорбенты, щелочные минеральные воды невысокой минерализации (поляна квасова, Лужанская, Березовская, вода источника № 4 в Моршине и др..).
Антидотная терапия в меньших дозах, чем в случае острых отравлений, помогает освободить от токсинов сульфгидрильные группы ферментов и таким образом улучшить обменные процессы. Для абсорбирования токсинов в кишечнике применяют пищевой пектин и различные энтеросорбенты. Восстановлению тканевых и клеточных структур способствуют аскорбиновая и глута-меновая кислоты, витамин В,, глюкоза и другие общеукрепляющие средства.
В случае хронической почечной недостаточности назначают соответствующее лечение.
Прогноз при условии раннего распознавания токсической нефропатии и прекращение контакта с токсинами благоприятный. Серьезный прогноз в случае нефропатий, вызванных кремнием, арсенат водорода, таллием, кадмием.
Профилактика
Профилактика состоит в строгом соблюдении мер гигиены труда, борьбе с загрязнением воздуха, воды и почвы, производственных и жилых помещений.
Лучевые поражения почек возникают вследствие однократного чрезмерного радиационного облучения или попадания чрезмерного количества радионуклидов в организм человека, а также при длительном внешнем радиационном облучении, особенно контактном, когда облучается 2/3 поверхности почки. Нефроны поражаются при наличии в тканях человека дозы свыше 2 Гр. При острой лучевой болезни почки поражаются значительно меньше, чем в случае контактного поясничного облучения опухолей внутренних органов человека.
Патогенез поражений почек при лучевой болезни сложен. Это не только местный травмивного влияние радиационного облучения на почки, а также нарушения обмена веществ, которое обусловлено преимущественно изменением активности многих ферментов вследствие повреждения радиацией структуры сульфгидрильных групп, входящих в их состав, вазомоторные нарушения, которые часто возникают у пациентов с лучевой болезнью и ведут к циркуляторной гипоксии. Радиационное облучение часто сопровождается автоимунизациею организма. Будучи главным местом отложения иммунных комплексов, почка особенно чувствительна к иммунологического повреждения. Особые мезангиальных клеток (2% клубочковых и 5% мезангиальных клеток) экспрессируют молекулы, которые соединяются с антигеном и активизируют лимфоциты для клеточных иммунных реакций. Мезангий представляет собой место инвазии моноцитов, фагоцитов и других биологически активных клеток, которые мигрируют из крови. Иммунологические процессы, происходящие в мезангии, могут влиять на физиологическое состояние сосудов и кровоснабжение, например путем стимуляции ангиотензиновую рецепторов, возможно при участии лимфокинов. Эпителиальная клетка капилляра (Подоцит) является местом локализации рецептора для комплемента (С 3 ). Развитие и прогрессирование интерстициального фиброза происходят вследствие реакции интерстиция на коллапс стромы, а также непосредственного влияния облучения на строму.
Патологическая анатомия . Морфологические изменения почек напоминают острый или хронический нефрит. В острый период заболевания почки набухают, несколько увеличиваются, возникают кровоизлияния в корковом и мозговом веществе почек, которые имеют вид точек и полосок. Эпителий нефронов набухает, структура его нарушается. Часто обнаруживают распространенное поражение клубочков в виде гиалиновой облитерации капиллярных петель, некроза фибриноидного или геморрагического типа, иногда с пролиферацией эпителия капсулы и ранним ее фиброзом. Выраженные дегенерация и атрофия канальцев, диффузный интерстициальный фиброз, фибриноидный некроз артериол и межчастичных артерий. Радиационный нефрит, вызванный попаданием радионуклидов в организм, протекает тяжелее, чем обусловлен внешним облучением. В частности, раньше развиваются и более обнаружены склеротические изменения почек (фиброз интерстиция и капсулы клубочков, увеличение размеров почек, паренхима которых заменяется фиброзной тканью).
Клиническая картина
Типичными для лучевой болезни являются изменения картины крови: анемия, диспротеинемия. При небольших дозах облучения (менее 0,7 Гр) и отсутствия контактного воздействия радиации на почку изменения функций почек незначительны и проявляются лишь при исследовании клубочковой фильтрации, почечного плазмоток, суточного диуреза (сначала увеличивается, а затем уменьшается), появляется незначительное протеинурия. При больших дозах общего облучения и непосредственном воздействии его на почку, инкорпорации нуклеотидов, которые выделяются почками, протеинурия увеличивается и становится длительной, возникают эритроцитурия, лейкоцитурия, цилиндрурия; наблюдают удлинение экскреторной сегмента радиограммы. В латентный период отмечают временное уменьшение этих сдвигов, которые потом не только возобновляются, но и усугубляются. Заболевание может перейти в хроническую форму или (у 30-40% больных) вызвать острую почечную недостаточность с высокой летальностью. При хронической лучевой болезни поражения почек характеризуется менее выраженной стадийностью, чем при острой, и нарастает медленнее. Изменения функции почек имеют смешанный клубочково-канальцевый характер. Хронический лучевой нефрит может проявляться лишь мочевым синдромом, а также гипертензивным синдромом и /или нефротическим синдромом, прогрессируя к хронической почечной недостаточности на фоне развития нефросклерозу. Хронический радиационный нефрит редко протекает доброкачественно, чаще через 2-4 года вследствие хронической почечной недостаточности наступает смерть.
Диагноз основывается на анамнестических данных. Во значительного внешнего облучения или инкорпорация радионуклеотидив (особенно полония и урана) с последующими изменениями функции почек и объема суточной мочи.
Для своевременного распознавания лучевого нефрита у лиц, подвергшихся радиационному воздействию, нужно, помимо методов, применяемых для диагностики лучевой болезни, использовать нефрологический диагностический комплекс. Особое внимание следует обратить на изменения объема, цвета и других свойств мочи, ритма мочеиспускания (никтурия), наличие отеков, артериальной гипертензии.
Выявление мочевого синдрома (протеинурия, эритроцитурия, диселектролитемия т.п.), нарушений почечной гемодинамики, парциальных функций почек, гиперазотемии, метаболического ацидоза и других симптомов позволяет распознать лучевой нефрит и обусловленную им почечную недостаточность .
Дифференциальная диагностика
Особенностью лучевого нефрита то, что он реже сопровождается нефротическим синдромом, чаще бывает гипертензивный синдром. Смерть вследствие хронической почечной недостаточности может наступить уже через 2-3 года от начала заболевания. Решающее дифференциально-диагностическое значение имеют анамнестические и радиометрические данные о влиянии радиационного фактора.
Прогноз благоприятный (вплоть до полного выздоровления), если доза внешнего облучения была небольшой и отсутствует инкорпорация радионуклеотидив. В других случаях прогноз плохой.
При острой лучевой болезни, вызванной внешним облучением от 50 до 100 Гр, смерть больного наступает через 3-8 суток после облучения, а при дозе облучения 10-50 Гр - через 2 -3 нед. Доза в 1-10 декабря приводит типовую форму лучевой болезни, на фоне которой может возникнуть интерстициальный или острый серозный пиелонефрит, что значительно отягощает прогноз.
Лечение радиационных поражений почек заключается в своевременном и эффективном лечении лучевой болезни с дополнительной коррекцией нарушений функций пораженных почек и назначении средств, способствующих выведению из организма инкорпорированных радионуклеотидив, и применением вместе с антибиотиками противогрибковых препаратов.
Больные острым лучевой нефрит и с обострением хронического лучевого нефрита должны быть госпитализированы в специализированные клиники.
Назначают диету с ограничением или исключением поваренной соли, экстрактивных веществ, специй (с модификациями в зависимости от синдромов), постельный режим, средства, применяемые при лучевой болезни и остром нефрите (энтеросорбенты, радиопротекторы, комплексы витаминов и аминокислот, галаскорбин, противовоспалительные, антигеморрагический, седативные, гипосенсибилизувальни препараты, стимуляторы гемопоэза, антибиотики, иммуномодуляторы).
В тяжелых случаях назначают кортикостероиды, проводят гемотрансфузии, гемосорбцию, гемодиализ, применяют другие активные методы лечения. Назначают при необходимости симптоматические средства - гипотензивные, мочегонные и др.. Если изолированно поражена только одна почка с резким нарушением функций, может быть эффективной нефрэктомия, но сначала надо убедиться в интактности контралатеральной почки.
Профилактика заключается в предотвращении внешнему облучению и проникновению радионуклидов в организм, а также в применении радиопротекторов и средств индивидуальной и коллективной защиты лицами, которые работают с радиоактивными веществами. Во время проведения лучевого лечения опухолей нужно защитить почки от попадания их в поле облучения.
Лица, которые имеют контакты с радиоактивными веществами, должны находиться под постоянным тщательным диспансерным наблюдением.
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.