Эпидемиология, этиология, патогенез
Пневмония - острое инфекционное заболевание преимущественно бактериальной этиологии, характеризующееся очаговым поражением респираторных отделов легких и наличием внутриальвеолярной экссудации.
Эпидемиология. В Украине в 2004 г., по данным официальной статистики, заболеваемость взрослых пневмонией составила 4,0 на 1 тыс. населения, а смертность - 12,8 на 100 тыс. населения, то есть умерло около 3% из тех, кто заболел пневмонией. Однако эти показатели не в полной мере отражают уровень настоящей заболеваемости и смертности.
Заболеваемость негоспитальную пневмонию взрослых (возраст старше 18 лет) составляет от 1 - 11,6 случая на 1 тыс. лиц молодого и среднего возраста к 25-44 - на 1 тыс. лиц старших возрастных групп (65 лет). У лиц старших возрастных групп при наличии сопутствующих заболеваний (злокачественные новообразования, алкоголизм, сахарный диабет, заболевания почек и печени, сердечно-сосудистые заболевания и др.). В случае тяжелого течения негоспитальной пневмонии этот показатель достигает 15-30%.
Этиология. Пневмония - заболевание инфекционного происхождения. Инфекция может быть бактериальной, вирусной, смешанной. Типичные бактериальные возбудители - S. pneumoniae, Н. influenzae, М. pneumoniae, С. pneumoniae, Legionella sp., грамотрицательные энтеробактерии; вирусы - гриппа, аденовирусы, ретикулосинтициальни вирусы, ассоциации микроорганизмов. Однако возбудитель обнаруживают не у всех больных пневмонией. Через недостаточную информативность и значительную длительность традиционных микробиологических исследований микробиологическое оценки возбудителя затруднено у 50-70% больных. Патогенный спектр различают у больных в зависимости от возраста, наличия сопутствующей патологии, тяжести заболевания, места, где заболел пациент, - во время пребывания в лечебном учреждении по поводу лечения заболевания различных органов и систем, в доме престарелых или в обычных условиях.
Патогенез. Чаще возбудитель попадает в респираторные отделы легких ингаляционным путем. Развитие заболевания связывают с врожденными или приобретенными нарушениями элиминации инфекционного агента, нарушениями мукоцилиарного клиренса, дефектами системы сурфактанта, ослаблением защитных механизмов иммунной системы. В патогенезе воспаления легких важную роль играют нарушения проходимости бронхов, ограничение подвижности грудной клетки и диафрагмы, снижение кашлевого рефлекса. Эти факторы могут предшествовать началу пневмонии или развиваться во время ее течения.
Факторами риска пневмонии, особенно тяжелой, могут быть состояния, когда нарушены глотательный, носоглоточный, кашлевой рефлексы; масочный наркоз; ИВЛ алкогольная интоксикация, состояние сознания. Все это может способствовать аспирации инфицированного материала (рвотные массы, носоглоточный слизь и т.п.).
Попадая в дыхательные пути, отдельные возбудители (например, некоторые типы пневмококков) вызывают воспалительный отек, размножаются в этом питательной среде, распространяются через поры Конна в соседние альвеолы - развивается альвеолярная пневмония. Другие микроорганизмы, что выделяют экзотоксины (например стафилококк), предопределяют первичное воспаление бронха, его укупорки слизисто-гнойными пробками, вследствие чего возникают мелкие инфицированные ателектазы легочной ткани - развивается бронхопневмония.
Небронхогенне инфицирования наблюдают редко: при попадании инфекции в случае травмы грудной клетки, при септическом метастазировании в легкие из гнойного очага внелегочной локализации.
Патологическая анатомия . Патологический процесс начинается с сосудистой реакции: повышается сосудистая проницаемость, экссудат заполняет септальный пространство и альвеолы. В рассасывании экссудата участвуют макрофаги, они также стимулируют пролиферацию фибробластов, что особенно выражено при затяжного процесса, в случае развития пролиферативных процессов с переходом в пневмосклероз.
Классификация
В Украине, как и во многих странах мира, применяют классификацию пневмонии с учетом условий возникновения заболевания, путей инфицирования легких, а также состояния иммунной реактивности организма больного. Согласно этой классификации выделяют следующие виды пневмонии:
-негоспитальная (внебольничная, распространенная, амбулаторная)
-госпитальная (нозокомиальная)
-аспирационная
-пневмония у лиц с тяжелыми нарушениями иммунитета (врожденный иммунодефицит, ВИЧ-инфекция, ятрогенная иммуносупрессия).
Главное значение имеет разделение пневмонии зависимости от места инфицирования негоспитальную и госпитальную (нозокомиальную).
соответствии с национальными и международными соглашениями по ведению больных пневмонией, негоспитальную пневмонию определяют как острое заболевание, возникшее во внебольничных условиях и сопровождается симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, вероятно гнойного, боль в груди, одышка) и рентгенологическими признаками новых очагово-инфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.
Госпитальная (нозокомиальная) пневмония - заболевание, характеризующееся появлением на рентгенограмме новых очагово-инфильтративных изменений в легких через 48 ч и более послегоспитализации в комплексе с клинической симптоматикой, подтверждающую их инфекционное происхождение (новая волна лихорадки, гнойная мокрота или гнойные выделения из трахеи и бронхов, лейкоцитоз и др.)., при условии исключения инфекций, находящихся в инкубационном периоде при госпитализации больного.
Пневмонию также различают по степени тяжести: пневмония с легким, средней тяжести и тяжелым течением. Пневмонию легкой и средней степеней тяжести объединяют в одну группу - пневмонию с нетяжелым течением, поскольку объем диагностических и лечебных мероприятий у таких больных почти одинаков. Отдельно выделяют пневмонию с тяжелым течением - особую форму заболевания, проявляется тяжелым интоксикационным синдромом, изменением гемодинамики, выраженной дыхательной недостаточностью и /или признаками тяжелого сепсиса или септического шока. В случае этого заболевания прогноз неблагоприятный, требуется интенсивная терапия. О тяжелом течении пневмонии свидетельствует наличие у больных не менее двух "малых" или одного "большого" критерия, каждый из которых достоверно повышает риск развития летального исхода. В таких случаях рекомендуют срочно госпитализировать больных в отделение реанимации и интенсивной терапии.
"Малые" критерии:
• частота дыхания> 30 в 1 мин
• нарушение сознания
• Sa0 2 <90%, Ра0 2 <60 мм рт. ст.
• систолическое AT <90 мм рт. ст.
• двустороннее или багаточасточкове поражения легких, наличие полостей распада, плеврального выпота.
"Большие" критерии:
• потребность в проведении ИВЛ
• быстрое прогрессирование очагово-инфильтративных изменений в легких - увеличение размеров инфильтрации более 50% в течение ближайших 2 суток
• септический шок или необходимость введения вазопресивних препаратов в течение> 4 ч
• ОПН.
Негоспитальная и нозокомиальная пневмонии имеют особенности относительно спектра потенциальных патогенов, клинического течения, терапевтических подходов.
Клиническая картина
Клинические проявления пневмонии разнообразны, однако есть признаки, присущие всем формам острого воспаления дыхательных путей: инфекционная интоксикация, субъективные и физикальные симптомы, осложнения. В случае интоксикации повышается температура тела, появляются головная боль, астеновегетативный синдром, слабость, адинамия, снижение аппетита (общие симптомы). К местным респираторных симптомов принадлежит кашель, иногда сухой, чаще - влажный. При вовлечении в воспалительный процесс плевры появляются боли в грудной клетке, усиливающаяся во время глубокого дыхания и резких движений, одышка, которая более выражена в случае тяжелого течения. При перкуссии может определяться притупление или тупость над пораженным участком, аускультативно - бронхов дыхания, влажные разнокалиберные хрипы, крепитация над очагом воспаления. Лабораторное исследование выявляет лейкоцитоз, другие признаки воспалительного процесса. Выраженность этих признаков зависит от состояния пациента в начале заболевания, тяжести течения заболевания, объема и локализации поражения легких, возраста больного, наличия и тяжести сопутствующих заболеваний. Такой симптомокомплекс неспецифический для негоспитальной пневмонии, но достаточный для установления предварительного клинического диагноза. Однако примерно у 20% больных объективные признаки негоспитальной пневмонии могут отличаться от типичных или их может не быть. У лиц старших возрастных групп, а также у пациентов с ослабленным иммунитетом иногда отмечают спутанность сознания, обострение или декомпенсацию сопутствующих хронических заболеваний, вероятно без лихорадки.
зависимости от возбудителя клинические проявления пневмонии также имеют свои особенности. Так, для пневмококковой пневмонии характерны острое начало, высокая лихорадка, боль в груди, для легионельознои - диарея, наличие неврологической симптоматики, нередко тяжелое течение заболевания, нарушения функции печени, для микоплазменной - головная боль, боль в мышцах, симптомы инфекции верхних дыхательных путей. Конкурентные клинические признаки часто обусловлены не особенностями возбудителя, а факторами макроорганизма - возрастом и наличием сопутствующих заболеваний. Острого начала, лихорадки, боли в груди и т.д. может не быть, особенно у ослабленных больных и пожилых людей - примерно у 25% больных негоспитальной пневмонией старше 65 лет нет лихорадки, а лейкоцитоз определяют в 50-70% из них. При этом нередко главными клиническими симптомами являются быстрая утомляемость, слабость, тошнота, анорексия, боль в животе, нарушение сознания. Плевральный выпот, который появляется обычно в небольшом количестве, не зависит от вида этиопатогенеза негоспитальной пневмонии, однако в 10-25% случаев усугубляет течение заболевания. Образование полостей распада в легких основном свидетельствует о стафилококковой инфекцией, аэробные грамотрицательные возбудители кишечной группы и анаэробы. Ретикулонодулярна инфильтрация в базальных отделах легких характерна для микоплазменной пневмонии (однако в 20% случаев микоплазменная пневмония может сопровождаться вогнищевозлитою инфильтрацией в проекции нескольких сегментов или доли легкого).
Осложнения негоспитальной пнев?? Онии:
• плевральный выпот
• эмпиема плевры
• деструкция /абсцесс ткани легкого
• острый респираторный дистресс-синдром
• острая дыхательная недостаточность
• инфекционно-токсический шок
• вторичная бактериемия, сепсис, гематогенные очага отсева
• перикардит, миокардит и др..
Важнейшими том числе и с точки зрения планирования антибактериальной терапии, является гнойно-деструктивные осложнения заболевания.
Абсцесс легких - это ограниченная полость в легочной ткани, которая сформировалась в результате некроза и гнойного расплавления. Возникновение абсцесса легких связывают прежде всего с анаэробными возбудителями (Bacteroides sp., Fusobacterium nucleatum, Peptostreptococcus sp. И др.)., Часто - с энтеро-бактериями (вследствие аспирации содержимого ротовой части глотки) или S. aureus.
Эмпиема плевры (гнойный плеврит) - накопление гноя в плевральной полости. Главными возбудителями эмпиемы плевры, связанная с пневмонией (с абсцессом легких или без него), являются анаэробы (довольно часто в комплексе с аэробными грамотрицательными бактериями), при подостром /хроническом течении эмпиемы плевры нередко этиологического значение приобретают анаэробные стрептококки, бактероиды и грамотрицательные энтеробактерии.
Затяжной течение негоспитальной пневмонии. У большинства больных после З-5 суток эффективной антибактериальной терапии отмечают положительную динамику - нормализуется температура тела и регрессируют другие клинические признаки заболевания. Рентгенологическая динамика обычно запаздывает, однако если на фоне улучшения клинической картины к концу 4-й недели от начала заболевания не удается достичь полного рентгенологического рассасывания очагово-инфильтративных изменений в легких, следует заподозрить пневмонию, не рассасывается (медленно рассасывается) или пневмонию с затяжным течением .
Факторы затяжного течения негоспитальной пневмонии: возраст свыше 50 лет, алкоголизм, сопутствующие заболевания (X03JI, застойная сердечная недостаточность, почечная недостаточность, злокачественная опухоль, сахарный диабет и др.)., тяжелое течение пневмонии, мультичасточкова распространенность пневмонийнои инфильтрации, такие возбудители пневмонии, как L. pneumophila, S. aureus, грамотрицательные энтеробактерии, курение, клиническая неэффективность назначенной терапии (сохраняются лейкоцитоз и лихорадка), вторичная бактериемия, приобретенная антибиотикорезистентность возбудителя заболевания.
внебольничной пневмонии с затяжным течением нужно дифференцировать с очагово-инфильтративным туберкулезом легких, онкопатологией, тромбоэмболией легочной артерии, инфарктом легкого, иммунопатологическими заболеваниями, заболеваниями сердечно-сосудистой системы (застойная сердечная недостаточность), медикаментозной токсическим пневмопатия, аспирацией инородного тела, саркоидозом, липощною пневмонией, ателектазом.
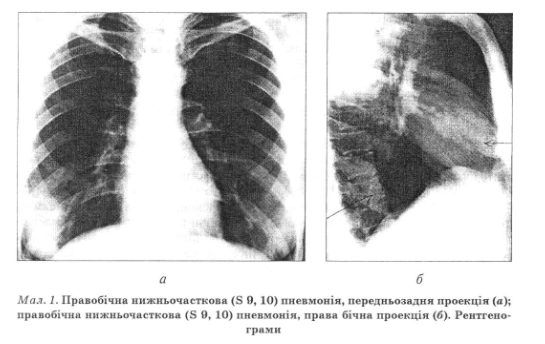
Диагностика
Диагноз пневмонии не является окончательным без рентгенологического подтверждения. Рентгенография органов грудной клетки позволяет визуализировать пневмонийну инфильтрацию, т.е. верифицировать диагноз пневмонии (как правило, при наличии соответствующих клинических признаков), оценить динамику патологического процесса и полноту выздоровления, а также провести дифференциальную диагностику с другими заболеваниями. Ее рекомендуют выполнять в задньопередний и боковой проекциях. Степень выраженности рентгенологических изменений (распространенность инфильтрации, наличие или отсутствие плеврального выпота, полостей распада) соответствует тяжести заболевания и может быть критерием для выбора антибактериальной терапии (рис. 1). В случае возникновения дифференциально-диагностических затруднений (например, при поражениях верхних долей легких, лимфатических узлов, средостения, при уменьшении объема доли легкого, в случае подозрения на абсцедирования, а также при неэффективности предшествующей антибактериальной терапии) рекомендуется провести дополнительные рентгенологические исследования (рентгенотомография , компьютерную томографию - КТ).
Микробиологическое исследование в случае негоспитальной пневмонии проводят с целью выявить возбудителя в материале, который получен из очага инфекции. Материал для исследования нужно собирать до проведения антибактериальной терапии. Однако микробиологическое исследование требует достаточно длительного времени, поэтому назначение антибиотика не следует откладывать.
Стандартные методы исследования - бактериоскопия окрашенных по Граму мазков мокроты и посев мокроты, полученный во время глубокого отхаркивание. Эти исследования обязательны при лечении больных с тяжелым течением негоспитальной пневмонии и необязательные в случае нетяжелым течением заболевания.
Материал, полученный при проведении бронхоальвеолярного лаважа и бронхоскопии, имеет высокую диагностическую ценность только при использовании так называемых защищенных щеток. Материал транстрахеального аспирата, мазки из интубационных трубок, зева и трахеостомы имеют низкую диагностическую ценность.
Перед началом микробиологического исследования мокроты проводят бактериоскопию мазков, ПОФарбованих по Граму. О гнойный характер мокроты свидетельствует наличие в мазках более 25 лейкоцитов и менее 10 эпителиальных клеток в поле зрения. Определение в мазках большого количества грамотрицательных или грамположительных микроорганизмов с типичной морфологией (грампозы-ные ланцетовидные диплококки - S. pneumoniae; сосредоточения грамположительных кокков в виде гроздьев - S. aureus, грамотрицательные кокобацилы - Н. influenzae) может быть ориентиром в выборе препаратов для назначения эмпирической антибиотикотерапии. Интерпретацию результатов бактериоскопии и посева мокроты следует проводить с учетом клинических данных.
При тяжелом течении негоспитальной пневмонии следует обязательно провести микробиологическое исследование крови (нужно взять 2 образца венозной крови из разных вен с интервалом более 10 мин).
Если невозможно получить пригодные для исследования образцы мокроты - при отсутствии продуктивного кашля, при наличии "обструктивной пневмонии" на фоне бронхогенной карциномы, при аспирации инородного тела в бронхи и т.д. - следует применять инвазивные методы диагностики: фибробронхоскопии с "защищенной" брашбиопсиею слизистой оболочки бронха, транстра-хеальну всасывании трансторакальную биопсию т.д.. Применение инвазивных методов исследования целесообразно у больных, находящихся на ИВЛ.
фибробронхоскопии проводят при наличии четких показаний - для исключения локальной бронхиальной обструкции и получения материала из нижних дыхательных путей.
Клинический анализ крови, лейкоцитоз свыше 10-12 - 10 9 /л свидетельствует о высокой вероятности бактериальной инфекции, а лейкопения ниже 3-10 9 /л или лейкоцитоз более 25 * 10 9 /л являются неблагоприятными прогностическими признаками.
Биохимические анализы крови (функциональные тесты печени, почек, гликемия и др.). при наличии отклонений от нормальных значений свидетельствуют о поражении органов /систем, имеет клиническое и прогностическое значение.
При наличии признаков дыхательной недостаточности нужно определить насыщенность крови кислородом или газы артериальной крови. Гипоксемия при Sa0 2 ниже 90% или Ра0 2 ниже 60 мм рт. ст. (Во время дыхания комнатным воздухом) является прогностически неблагоприятным признаком и показанием к лечению больного в условиях стационара.
При наличии у больного плеврального выпота и условий для безопасного проведения плевральной пункции (визуализация на латерограми свободной жидкости слоем толщиной более 1 см) следует проводить исследование плеврального выпота с клиническим, биохимическим анализом (содержимое лейкоцитов и лейкоцитна формула, рН, активность лактатдегидрогеназы, содержание белка), красить мазки по Граму и на кислотоустойчивые бактерии, провести посев для выявления аэробных, анаэробов и микобактерий.
Критерии диагноза негоспитальной пневмонии. Диагноз негоспитальной пневмонии считают установленным при наличии у больного рентгенологически подтвержденной очаговой инфильтрации легочной ткани и не менее 2 клинических признаков, перечисленных ниже:
• острое начало заболевания с температурой тела выше 38 ° С
• кашель с выделением мокроты
• физикальные признаки (притупление или тупой перкуторный звук, ослабленное или жесткое бронхов дыхание, фокус звонких мелкопузырчатые хрипы и /или крепитации)
• лейкоцитоз (свыше 10Т0 9 /л) и /или палочкоядерных сдвиги (более 10%).
В случае невозможности получить рентгенологическое подтверждение пневмонии диагноз негоспитальной пневмонии считают неточным /неустановленным. В таком случае диагноз заболевания устанавливают с учетом результатов эпидемиологического анамнеза, жалоб больного и выявленных у пациента соответствующих физикальных признаков. В такой ситуации диагноз негоспитальной пневмонии рентгенологически подтверждается лишь в 22% случаев.
Наличие негоспитальной пневмонии маловероятна у больных с лихорадкой, жалобами на кашель, одышку, выделение мокроты и /или боли в груди при отсутствии физикальных признаков и невозможности проведения рентгенологического исследования органов грудной клетки.
Следующим этапом ведения больного негоспитальную пневмонию является решение, в каких условиях (амбулаторно или в стационаре) лечиться конкретный пациент, оно должно основываться на точном определении тяжести заболевания при обращении больного за медицинской помощью и на прогнозе вероятного неблагоприятного (летального) исхода заболевания.
Для объективной оценки тяжести и прогноза негоспитальной пневмонии целесообразно применять балльную оценку факторов риска летального исхода (по исследованиям the Pneumonia Patient Outcomes Research Team (PORT)), распространенную и апробированную. По этой шкале возраст, наличие сопутствующих заболеваний, отягощающих симптомов, клинически значимых лабораторных показателей оценивают в баллах, суммируют и по сумме баллов определяют класс риска летального исхода при внебольничной пневмонии. С учетом класса определяют место лечения больных и производят соответствующую тактику.
Больные с низким риском вероятности летальных исходов (I-II класс, 70 баллов, летальность 0,1%) могут лечиться амбулаторно. Те, набравшие 71-90 баллов, относятся к III классу с летальностью 0,6% и могут счетаваться амбулаторно или до 4 суток находиться в стационаре, затем продолжить лечение в амбулаторных условиях. Пациенты с высоким риском (> 91 балл, IV и V классы риска) подлежат госпитализации.
Выделяют особые категории больных, которые могут лечиться в условиях стационара независимо от степени тяжести пневмонии - при наличии социальных показаний (например, невозможность ухода в домашних условиях, социально незащищенные субъекты т.п.) , в случае обострения сопутствующей патологии (25-50% от числа всех госпитализированных).
Есть более упрощенная схема, которая предусматривает выделение 3 групп неблагоприятных прогностических факторов риска летальных исходов у больных негоспитальной пневмонией. Главные из них: нарушение сознания, частота дыхания более 30 в 1 мин; артериальная гипотензия (систолическое АД ниже 90 мм рт. Ст. И /или диастолическое АД 60 мм рт. Ст. И ниже); азот мочевины более 7 ммоль /л; дополнительные - двустороннее или многочастичных поражения легких, полости распада, плевральный выпот (по данным рентгенологического обследования); гипоксемия (Sa0 2 менее 90% или Ра0 2 ниже чем 60 мм рт. ст.) и факторы, которые были у больного до начала заболевания негоспитальную пневмонию: возраст свыше 50 лет; сопутствующие заболевания (X03JI, бронхоэктатическая болезнь, злокачественные новообразования, сахарный диабет, хроническая почечная недостаточность, застойная сердечная недостаточность, хронические заболевания печени, заболевания головного мозга, алкоголизм, наркомания).
При отсутствии каких-либо неблагоприятных прогностических факторов из трех приведенных групп риск летальных исходов является низким (0,1-0,4%). Таких больных лечат в амбулаторных условиях. Но они могут быть госпитализированы учитывая обстоятельств.
При наличии одного из основных неблагоприятных прогностических факторов больного следует госпитализировать. Для пациентов с прогностические факторы других групп (дополнительные факторы и /или те, которые были у больного до начала заболевания), при решении вопроса о месте (амбулаторно или в условиях стационара) и объем (как больных с нетяжелым или тяжелым течением негоспитальной пневмонии ) лечение следует исходить из конкретной клинической ситуации.
Наличие у пациентов двух или более основных неблагоприятных прогностических факторов свидетельствует о тяжелом течении заболевания и высокий риск летальных исходов (23% - в случае 2 факторов, 33% - 3), поэтому их нужно срочно госпитализировать в отделение реанимации и интенсивной терапии.
Больных негоспитальную пневмонию с тяжелым течением выделяют в отдельную группу, поскольку они требуют проведения неотложной интенсивной терапии. Во всех госпитализированных больных регулярно оценивают степень тяжести заболевания для решения вопроса об уменьшении или увеличении объема антибактериальной терапии, а у больных, у которых во время госпитализации было выявлен один или более основных неблагоприятных прогностических факторов, переоценивают состояние не реже чем каждые 12 ч до появления признаков улучшения.
Поскольку микробиологическая диагностика пневмонии отсрочена во времени, а антибактериальную терапию нужно начинать как можно раньше, больных негоспитальной пневмонией условно разделяют на группы, в каждой из которых можно предположить наличие вероятных возбудителей и их чувствительность к антибактериальным препаратам.
При делении на группы для проведения терапии учитывают избранное на основе оценки неблагоприятных прогностических факторов место лечения больного (в амбулаторных условиях, в стационаре, в отделении реанимации и интенсивной терапии), наличие сопутствующих хронических заболеваний и других модификувальних факторов, определяющих возможную наличие определенных проблемных возбудителей негоспитальной пневмонии у взрослых.
Модификувальни факторы, влияющие на риск появления отдельных возбудителей негоспитальной пневмонии у взрослых, в некоторой степени специфические для того или иного микроорганизма. Так, для антибиотикорезистентных штаммов S. pneumoniae это возраст более 65 лет; терапия р-лактамами, которую проводили в течение последних 3 мес.; алкоголизм, иммунодефиците заболевания /состояния (в частности лечение системными ГКС) множественные сопутствующие заболевания внутренних органов.
грамотрицательные энтеробактерии ассоциируются с сопутствующими сердечно-сосудистыми и бронхолегочными заболеваниями множественными сопутствующими заболеваниями внутренних органов; антибактериальной терапией по поводу других заболеваний; пребыванием в доме престарелых.
Роль P. aeruginosa значительно возрастает в случае структурных заболеваний легких (например бронхоэктазы, муковисцидоз), длительного лечения системными ГКС (употребление преднизолона в дозе 10 мг в сутки) терапии антибиотиками широкого спектра действия более 7 суток в течение последнего месяца, при истощении. С учетом этого всех взрослых пациентов с негоспитальной пневмонией делят на четыре группы.
I группа: больные негоспитальную пневмонию с нетяжелым течением, не требующие госпитализации, без сопутствующей патологии и других модификувальних факторов. Частые возбудители - S. pneumoniae, М. pneumoniae, С. pneumoniae, Н. influenzae (как правило, у курильщиков) и респираторные вирусы. У 30-50% пациентов возбудителя не определяют вообще, поэтому проводить рутинную микробиологическую диагностику нецелесообразно. Пе?? Ну ценность могут иметь результаты эпидемиологических исследований (групповая заболеваемость лиц молодого возраста в организованных коллективах характерна для инфекции, вызванной S. pneumoniae или М. pneumoniae).
II группа: больные негоспитальную пневмонию с нетяжелым течением, не требующие госпитализации, при наличии сопутствующей патологии (ХОБЛ, почечная и сердечная недостаточность, заболевания головного мозга, опухоли, сахарный диабет, хронические заболевания печени различной этиологии, психические расстройства, алкоголизм) и /или других модификувальних факторов. Возбудители: S. pneumoniae (в том числе антибиотикорезистентные штаммы), Н. influenzae, S. aureus, М. catarrhal, возможна грамотрицательная инфекция: семейство Enterobacteriaceae (Е. coli, Klebsiella sp.), особенно у пожилых людей. Возрастает вероятность анаэробной инфекции - у лиц с несанованою полостью рта, наличием в анамнезе неврологических заболеваний и /или нарушение акта глотания. Рутинная микробиологическая диагностика у этих больных также малоинформативна и практически не влияет на выбор антибиотиков. Однако примерно у 20% больных этой группы может возникнуть потребность в госпитализации из-за неэффективности амбулаторного лечения и /или обострение /декомпенсацию сопутствующих заболеваний.
III группа: больные негоспитальную пневмонию с нетяжелым течением, которые нуждаются в госпитализации в терапевтическое отделение по медицинским (наличие неблагоприятных прогностических факторов) показаниям. Типичные патогены: S. pneumoniae, Н. influenzae, атипичные возбудители, грамотрицательные энтеробактерии. В 10-40% больных III группы часто обнаруживают "смешанную" инфекцию (то есть объединение типичных бактериальных и атипичных возбудителей).
IV группа: больные негоспитальную пневмонию с тяжелым течением, которые нуждаются в госпитализации в отделение реанимации и интенсивной терапии. Спектр мик-робно флоры: S. pneumoniae, Legionella sp., Н. influenzae, грамотрицательные энтеробактерии, S. aureus и М. pneumoniae (достаточно редко). При наличии модулировали-ных факторов возбудителем негоспитальной пневмонии может быть P. aeruginosa.
Антибактериальная терапия негоспитальной пневмонии. Основным в лечении негоспитальной пневмонии является антибактериальная терапия. Антибактериальное лечение нужно начинать сразу после установления диагноза, особенно у тех пациентов, которые нуждаются в госпитализации, а у больных с тяжелым течением заболевания задержания с введением первой дозы антибиотика на 4 часа и более значительно повышает риск смерти.
Если этиология заболевания неизвестна, назначают эмпирическую терапию (с учетом вероятных возбудителей). В реальных условиях начальная этиотропная антибиотикотерапия практически всегда является эмпирической.
Для проведения эмпирической антибактериальной терапии следует использовать антибиотики широкого спектра действия, высокоактивные относительно основных возможных возбудителей негоспитальной пневмонии, с оптимальным профилем безопасности (низкая частота развития побочных эффектов), те, что создают высокие концентрации в тканях и биологических жидкостях органов дыхания; имеющие оптимальное соотношение стоимость /эффективность; удобны в применении, что способствует склонности больного к соответствующему режима лечения (комплаенс). Это особенно важно в случае амбулаторного лечения больных, которые нарушают режим употребления лекарств.
Эмпирическая антибактериальная терапия больных негоспитальной пневмонией в амбулаторных условиях. Больным негоспитальную пневмонию I группы рекомендуют амоксициллин или макролид (азитромицин, кларитромицин, мидекамицин, спирамицин) в качестве монотерапии перорально. Если больным нельзя употреблять эти препараты назначают альтернативный препарат - респираторный фторхинолон III-IV поколения.
V пациента, относится к группе низкого риска летальных исходов, при условии назначения адекватного лечения состояние должно улучшиться в течение 48 ч (см. далее "Критерии эффективности антибактериальной терапии"). По больного, состояние которого не улучшилось в течение 48 ч, решают вопрос о целесообразности госпитализации (с учетом основных и дополнительных неблагоприятных прогностических критериев) или проведение рентгенографии легких. Пациента, который не относится к группе с низким риском летальных исходов, но которого лечат амбулаторно, необходимо наблюдать ежедневно в течение первых 3 суток лечения.
У больных II группы можно назначать пероральное применение антибиотика. Однако поскольку увеличивается вероятность этиологической роли грамотрицательных микроорганизмов (в частности, имеющие некоторые механизмы развития резистентности к антибиотикам) как средство выбора рекомендуют защищен аминопенициллины (амоксициллин /клавулановая кислота) или цефалоспорин II поколения (цефуроксим аксетил). Как альтернативу можно применять фторхинолон III-IV поколения. При невозможности перорального приема препарата или низкого комплаенса назначают парентерально антибиотик III поколения (лучше цефтриаксон внутримышечно, который можно применять 1 раз в сутки).
Через 48 ч от начала антибактериальной терапии обязательно следует оценивать эффективность терапии. Основные критерии эффективности в эти сроки - уменьшение выраженности интоксикации и снижение температуры тела больного, отсутствие признаков дыхательной недостаточности. Если в начале лечения у пациента отсутствовали эти симптомы, следует ориентироваться на его общее состояние и показатели общего клинического анализа крове (количество лейкоцитов, СОЭ). При наличии положительной динамики предназначенную терапию продолжают. Если у пациента сохраняются высокая лихорадка и интоксикация или прогрессирует симптоматика, лечение следует считать неэффективным, антибактериальное средство заменить на другой и повторно оценить целесообразность госпитализации.
Так, в I группе, если первым назначенным препаратом был амоксициллин и лечение оказалось неэффективным, возможной причиной клинической неудачи может быть наличие атипичных возбудителей и на втором этапе лечения следует назначить макролид. Если начальная терапия макролидом была неэффективной, то вероятно, что негоспитальная пневмония у больного вызвана макролидорезистентним S. pneumoniae и на втором этапе следует назначить амоксициллин. Во II группе в случае неэффективности начальной терапии защищенным аминопенициллины или цефалоспорины II поколения, возможно, через атипичные возбудители, в р-лактаму добавляют макролид или проводят монотерапию фторхинолоном III-IV поколения.
У пациентов с нетяжелым течением негоспитальной пневмонии антибактериальная терапия может быть завершена после достижения нормализации температуры тела в течение 3-5 суток. В таких случаях продолжительность лечения обычно составляет 7-10 суток. В случае получения клинических или эпидемиологических данных, подтверждающих микоплазменную или хламидийной этиологии негоспитальной пневмонии, длительность антибактериальной терапии в среднем составляет 10 - 14 суток. Если в эти сроки положительного эффекта лечения достигнуто, заменять антибиотик нецелесообразно.
Критерии достаточности антибактериальной терапии больных негоспитальной пневмонией
• Температура тела ниже 37,5 ° С.
• Отсутствие симптомов интоксикации.
• Отсутствие признаков дыхательной недостаточности (частота дыхания до 20 в 1 мин).
• Отсутствие гнойной мокроты.
• Количество лейкоцитов в крови менее 10Т0 9 /л, нейтрофилов - менее 80%, юных форм - менее 6%.
• Отсутствие отрицательной динамики по результатам рентгенологического исследования.
Удлинение антибактериальной терапии или ее коррекция при сохранении отдельных клинико-рентгенологических или лабораторных признаков заболевания не всегда являются целесообразными. Так, стойкий субфебрилитет (температура тела в пределах 37,0-37,5 ° С) при отсутствии других признаков бактериальной инфекции может быть проявлением неинфекционного воспаления, постинфекционной астении (вегетативной дисфункции), медикаментозной лихорадки, остаточные изменения на рентгенограмме (инфильтрация, усиление легочного рисунка) могут храниться более 1-2 мес. после перенесенной пневмонии, сухой кашель может продолжаться 1-2 мес. после перенесенной пневмонии, особенно у курильщиков и пациентов с X03J1; сухие хрипы могут сохраняться в течение более 3-4 недель. после перенесенной пневмонии и свидетельствуют о естественное течение заболевания (локальный эндобронхит или пневмосклероз на месте фокуса воспаления) слабость, потливость могут храниться как проявление постинфекционной астении. В основном эти симптомы исчезают - самостоятельно или под влиянием симптоматического лечения.
Эмпирическая антибактериальная терапия больных негоспитальной пневмонией в условиях стационара. Больным I и II групп, которые госпитализированы по социальным показаниям, назначают пероральную антибактериальную терапию, как и в случае амбулаторного лечения этих групп пациентов.
Если больные были госпитализированы по медицинским показаниям (тяжесть), терапию целесообразно начинать с парентерального (внутримышечного, внутривенного) введения антибиотиков. Через 3-4 суток при достижении положительного клинического эффекта (нормализация температуры тела, уменьшение выраженности интоксикации и других симптомов заболевания) можно переходить к перорального приема антибиотика до завершения полного курса антибактериальной терапии (ступенчатая терапия).
Госпитализированным в терапевтическое отделение больным III группы проводят комбинированную парентеральную антибиотикотерапию с использованием защищенного аминопенициллины (амоксициллин /клавулановая кислота, ампициллин /сульбактам) или цефалоспорины II-III поколения (цефуроксим, цефотаксим, цефтриаксон ) вместе с макролидом. В случае отсутствия нарушений всасывания в ЖКТ макролид употребляют перорально. При невозможности употребления больным препарата выбора или в случае его неэффективности через 48 ч следует назначить фторхинолон III-IV поколения (монотерапия).
Больным IV группы с тяжелым течением негоспитальной пневмонии, которые госпитализированы в отделение реанимации и интенсивной терапии, следует безотлагательно назначить антибактериальную терапию, поскольку отсрочка назначения антибиотика даже на 4 ч достоверно повышает риск смерти пациентов .
Для лечения больных этой группы, не имеющих факторов риска инфицирования P. aeruginosa, рекомендуют внутривенно вводить защищен аминопенициллины (амоксициллин /клавулановая кислота, ампициллин /сульбактам) или цефалоспорин III поколения (цефотаксим, цефтриаксон) вместе с макролидом. Как альтернативную терапию предлагают комбинацию фторхинолона III-IV поколения с (3-лактамным антибиотиком. При легионельознои пневмонии целесообразно комбинировать макролид с рифампицином, а как альтернативну терапию рекомендуют назначать фторхинолон III-IV поколения.
Для лечения больных IV группы при наличии факторов риска инфицирования P. aeruginosa нужно назначать в: р-лактам, активен в отношении синегнойной палочки (цефтазидим, цефоперазон, цефепим, меропенем), в сочетании с аминогликозидом и макролидом. Как альтернативную терапию предлагают антипсевдомонадний р-лактам (меропенем) в сочетании с аминогликозидом и ципрофлоксацином или левофлоксацином.
Критерии эффективности антибактериальной терапии. Оценивать эффективность антибактериальной терапии нужно через 48-72 ч от начала лечения. Основными критериями эффективности в эти сроки является уменьшение проявлений интоксикации и снижение температуры тела больного, отсутствие признаков дыхательной недостаточности. При наличии положительной динамики курс назначенной антибактериальной терапии удлиняют. Если у пациента сохраняются высокая лихорадка и интоксикация или симптоматика прогрессирует, лечение следует считать неэффективным и провести соответствующую коррекцию терапии.
В случае неэффективности антибактериальной терапии необходимо дополнительно обследовать больного для уточнения диагноза или выявления возможных осложнений пневмонии.
Для оценки состояния больного и эффективности терапии целесообразно провести следующие исследования:
• клинический анализ крови - на 2-й день и до окончания антибактериальной терапии
• биохимический анализ крови - при наличии изменений в первую исследования - контрольный анализ через 1 нед.
• исследование газов крови или Sa0 2 у больных с тяжелым течением негоспитальной пневмонии - ежедневно до нормализации показателей
• рентгенография органов грудной клетки - через 2-3 нед. от начала лечения (перед выпиской из стационара), в случае ухудшения состояния пациента - в более ранние сроки.
У пациентов с нетяжелым течением негоспитальной пневмонии антибактериальная терапия может быть завершена по достижении стойкой нормализации температуры тела в течение 3-5 суток. В таких случаях продолжительность лечения составляет, как правило, 7-10 дней.
У больных негоспитальной пневмонией с тяжелым течением и невстанов-лено этиологии длительность антибиотикотерапии составляет 10 суток.
В случае микоплазменной или хламидийной этиологии заболевания длительность антибактериальной терапии составляет в среднем 10-14 суток.
Во время лечения больных с негоспитальной терапией стафилококковой этиологии или обусловленной грамотрицательными энтеробактериями рекомендуют проведение более длительной антибактериальной терапии - от 14 до 21 суток, а при наличии результатов о легионельозну этиологию заболевания - 21 день .
У пациентов с ранней клинической эффективностью назначенной антибактериальной терапии можно заменить парентеральное введение антибиотиков на пероральный применения с последующим выписыванием из стационара.
Пациентам при отсутствии адекватной клинической "ответы" на лечение в течение первых 3 суток после госпитализации или в случае ухудшения клинического течения заболевания через 24-48 ч от начала лечения необходимо откорректировать лечение и дополнительные обследования .
Если клиническая, лабораторная и рентгенологическая симптоматика негоспитальной пневмонии сохраняется длительное время, нужно проводить дифференциальную диагностику с такими заболеваниями, как рак легких, туберкулез, застойная сердечная недостаточность и др..
Ступенчатая антибактериальная терапия негоспитальной пневмонии. Ступенчатая терапия предполагает двухэтапное назначение антибиотиков для лечения госпитализированных больных: переход от парентерального введения на пероральное применение в кратчайшие сроки с учетом клинического состояния пациента.
Такая тактика имеет ряд преимуществ - уменьшается продолжительность парентерального введения антибиотика, что способствует существенному снижению стоимости лечения, сокращению длительности госпитализации при сохранении высокой клинической эффективности лечения. Раннее, без необоснованного задержания, выписки больного из стационара не только сокращает прямые и косвенные расходы, но и уменьшает риск присоединения нозокомиальной инфекции.
Основные критерии для перевода больного на пероральный приема антибиотика: нормальная температура тела в течение двух последующих измерений с интервалом 8 ч, уменьшение выраженности одышки, нарушена сознание, положительная динамика других симптомов заболевания, отсутствие нарушений всасывания в ЖКТ, согласие пациента на пероральный прием препаратов. Обычно возможность перехода на пероральное применение антибиотика возникает через 2-4 суток от начала лечения.
Во время проведения ступенчатой терапии предпочтение отдается препаратам, которые имеют две лечебные формы - как для парентерального введения, так и для применения внутрь. Если антибиотик существует лишь в форме для парентерального введения или оральная форма недоступна, возможен переход на пероральные антибиотики других групп, имеющих сходные антимикробные свойства и одинаковый уровень приобретенной резистентности. Выбранный препарат должен иметь также высокую биодоступность, не взаимодействия?? Модияты с другими лекарственными средствами, хорошо переноситься, иметь длительный период полувыведения и доступную стоимость курса лечения.
Во время лечения негоспитальной пневмонии установленной этиологии назначают препараты, к которым имеет чувствительность выделена флора.
Прогноз. Прогноз при пневмонии значительно улучшилось после начала применения антибактериальных средств. В случае первичных очаговых пневмоний прогноз обычно благоприятный. Выздоровление наступает, как правило, на 15-25-е сутки от начала заболевания.
Однако при стафилококковых пневмониях, распространенных пневмониях, осложненных дыхательной и сердечной недостаточностью, а также в случае возникновения пневмонии у больных с тяжелыми болезнями сердечно-сосудистой и других систем прогноз остается серьезным. Крупозная пневмония, очаговые пневмонии средней тяжести или тяжелого течения наблюдают чаще у лиц с серьезной сопутствующей патологией, они сопровождаются, как правило, различными легочными и нелегеневимы осложнениями, нередко приводят к летальному исходу. При этом риск смерти больного определяется возрастом (дети до 12 лет и взрослые - старше 50 лет), тяжестью интеркуррентных заболеваний и характером осложнений (при развитии бактериемии летальность составляет 18% и выше).
Профилактика. Различают первичную и вторичную профилактику пневмонии. Вторичная профилактика направлена на предотвращение повторных заболеваний и осложнений во время лечения.
Первичная профилактика предусматривает повышение резистентности организма, устранение факторов, ослабляющих организм. Важнейшим средством профилактики первичных пневмоний является тщательное и своевременное лечение ОРЗ, занятия спортом, отказ от курения и злоупотребления алкоголем, правильное питание, регулярное употребление поливитаминов. Избежать развития пневмонии после травм, отравлений, оперативных вмешательств можно благодаря применению дыхательной гимнастики, нормализации дренажа бронхов, а иногда и превентивному назначению антибиотиков. Сейчас большое значение придают профилактике пневмоний у больных, относящихся к группе риска (наличие гематологической, онкологической патологии и других состояний, требующих цитостатической и иммуносупрессивной терапии). Сюда же можно отнести BIJI-инфицированных и больных с тяжелыми хроническими заболеваниями сердца, легких, печени, сахарным диабетом, почечной недостаточностью и др.. Для профилактики пневмококковой инфекции в перечисленных групп больных все чаще применяют 23-валентную вакцину, созданную с капсульных полицукридив пневмококка. У лиц с интактной иммунной системой эффективность вакцинации достигает 80-90%, а потребность ревакцинации возникает не чаще чем 1 раз в 5 лет. Вакцинация защищает не только от пневмонии, но и от других форм пневмококковой инфекции. Например, у лиц с резекцией селезенки нередко развивается очень тяжелое пневмококковый сепсис. Эти лица также следует иммунизировать.
Вторичная профилактика заключается в поэтапной реабилитации и оздоровлении больных, перенесших пневмонию. На период нормализации общего состояния выздоровления полностью еще не наступило и очень важно в это время не допустить повторного заражения, исключить влияние неблагоприятных факторов окружающей среды. Рекомендуется комплекс лечебной гимнастики, водных процедур, массаж, физиотерапевтические процедуры. Лицам, перенесшим пневмонию, рекомендуют посещать врача не реже 2 раз в месяц в течение 3 мес.
Эпидемиология госпитальной пневмонии
Госпитальная пневмония развивается у 0,5-1% госпитализированных больных. Уровень заболеваемости госпитальную пневмонию зависит от многих факторов - возраста пациентов, тяжести основного и сопутствующего заболеваний, объема инвазивных вмешательств и др.. Заболеваемость госпитальную пневмонию среди госпитализированных пациентов в возрасте до 35 лет составляет около 5%, а среди лиц старше 65 лет - 15% и более. Среди пациентов хирургических отделений, отделения реанимации и интенсивной терапии этот показатель возрастает до 15-20%, а среди больных, находящихся на ШВЫ, - до 18-60%. Ежедневное пребывание пациента в реанимационном отделении или блоке интенсивной терапии по поводу проведения ИВЛ увеличивает риск развития госпитальной пневмонии на 1-3%. В 9-27% пациентов, находящихся на ИВЛ, развивается так называемая вентилятор-ассоциированная пневмония (ВАП). Срок между госпитализацией, поступлением пациента в отделение реанимации и интенсивной терапии, интубацией и развитием ВАП в среднем составляет соответственно 3,3, 4,5 и 5,4 суток.
Летальность при госпитальной пневмонии колеблется от 10 до 30%, а среди больных, находящихся на ИВЛ, может достигать 70%. Несмотря на столь высокий уровень смертности больных госпитальную пневмонию, летальный исход не всегда является прямым следствием этого заболевания. Смертность, связанная с пневмонией, определяется как часть смертельных случаев при госпитальной пневмонии, которые не произошли при отсутствии этой инфекции. Проведенные исследования показали, что от 30 до 50% общего количества смертельных случаев пациентов с госпитальной пневмонией является непосредственным следствием этой болезни, однако показатель может быть и выше, если есть бактериемия или этиологическим агентом госпитальной пневмонии является P. aeruginosa или Acinetobacter sp.
Распространенность госпитальной пневмонии различается не только в разных странинах или регионах, но и в лечебных учреждениях и даже в отдельных отделениях. Поэтому очень важно контролировать эпидемическую ситуацию в конкретном стационаре и соответствующим образом корректировать лечение больных госпитальную пневмонию. Особенно актуальной проблемой является госпитальная пневмония у больных, находящихся в отделениях реанимации и интенсивной терапии, хирургических, ожоговых и т.п..
Этиология госпитальной пневмонии. Определение этиологии госпитальной пневмонии является сложным вопросом из-за разнообразия возбудителей заболевания, а также объективных трудностей микробиологической диагностики. Даже при тщательном бактериологического исследования почти у половины больных госпитальную пневмонию не удается определить инфекционный агент, а у большинства пациентов обнаруживают полимикробные ассоциации.
Наибольшее значение в этиологии госпитальной пневмонии имеют грамотрицательные бактерии (в 50-70% случаев). Среди них ведущими возбудителями являются P. aeruginosa и представители семейства Enterobacteriaceae (прежде Klebsiella sp. и Enterobacter sp., а также E. coli, Serratia sp., Proteus sp.).
S. aureus занимает второе место среди возбудителей госпитальной пневмонии и в 15-30% случаев вызывает ее возникновения. В секрете дыхательных путей больных, находящихся в стационаре, достаточно часто обнаруживают S. epidermidis. Однако его патогенные свойства по легких не установлено и эту микробиологическую находку, по данным большинства исследований, можно не учитывать.
P. aeruginosa, представитель семейства Enterobacteriaceae, S. aureus в большинстве случаев устойчивы к антибактериальным препаратам разных классов. Они имеют сложные и разнообразные механизмы резистентности, из которых важнейшими являются продуцирование (3-лактамаз широкого спектра действия (extended spectrum P-lactamase - ESBL), модификация мишени действия антибиотиков и т.п., что и определяет высокую устойчивость их к р-лактамным антибиотикам. Часто возбудителями госпитальной пневмонии, особенно у больных в отделениях реанимации и интенсивной терапии, является неферментативные микроорганизмы, такие как Acinetobacter sp., С. meningosepticum, S. maltophilia, B. cepacia, которые имеют своеобразный спектр естественной устойчивости к антибактериальным средствам.
Анаэробные бактерии (неклостридийни облигатные анаэробы) - В. fragilis, В. melaninogenicus, F. nucleatum - выделяют в 10-30% случаев госпитальной пневмонии. Эти микроорганизмы вызывают обычно тяжелую и раннюю деструкцию легочной ткани (абсцесс, гангрена). Как правило, вместе с анаэробной микрофлорой в лабораторном материале обнаруживают и конкурентные аэробные бактерии.
В 5-10% случаев госпитальную пневмонию вызывают другие микроорганизмы, в том числе S. pneumoniae, Н. influenzae, С. pneumoniae, зачастую приводят к развитию "ранних" (до 6 дней) госпитальных пневмоний у больных без факторов риска.
В 4% случаев госпитальные пневмонии связывают с легионельозною инфекцией. Массовые вспышки болезни легионеров в госпиталях обычно обусловлены контаминацией систем водоснабжения и кондиционирования. Кроме того, эпидемические вспышки могут вызвать Acinetobacter sp., S. aureus, P. aeruginosa, Serratia sp., представители семейства Enterobacteriaceae, Aspergillus sp., вирусы и тому подобное.
Аспергиллез наблюдают, как правило, у ослабленных больных, в основном у лиц с подавленным клеточным иммунитетом и /или нейтропенией. Его можно заподозрить, если при наличии соответствующих факторов риска на компьютерных томограммах появляется характерная картина - очаговое поражение легких с распадом. Другие грибковые инфекции в происхождении госпитальной пневмонии важное значение не имеют. Часто из материала, взятого у больных, находящихся в стационаре, выделяют Candida sp., Но в таких случаях чаще всего речь идет не о инфицирования, а о контаминацию.
У больных госпитальную пневмонию вирусы выделяют в 10-20% случаев. У взрослых иммунокомпетентных больных, как правило, это вирусы гриппа А и В, респираторно-синцитийний вирус. У лиц с нарушениями клеточного иммунитета возбудителем госпитальной пневмонии может быть цитомегаловирусная инфекция, а при наличии тяжелых иммунологических нарушений - P. carinii и патогенные грибы.
По данным современных эпидемиологических исследований, существует определенная зависимость между условиями возникновения госпитальной пневмонии и ее этиологическими агентами, следует учитывать, выбирая эмпирической антибиотикогерапию.
Например, модификувальнимы факторами, которые ассоциируются с большой вероятностью участия антибиотикорезистентных штаммов S. pneumoniae в возникновении госпитальной пневмонии, являются:
• возраст старше 65 лет
• терапия р-лактамами, которую проводили в течение последних 3 мес.
• алкоголизм
• иммунодефицитные состояния (в том числе лечение системными глюкокор-тикостероидамы)
• сопутствующие заболевания внутренних органов.
S. aureus чаще обнаруживают у больных с
• черепно-мозговой травмой
• сахарным диабетом
• ХПН
• при длительной катетеризации сосудов
• после вирусной инфекции (гриппа).
Возникновение грамотрицательных энтеробактерий могут обусловить:
• сопутствующие сердечно-сосудистые и бронхолегочные заболевания
• Антиб?? Материально терапия, которую проводили по поводу других заболеваний
• пребывания в стационаре или дома престарелых.
Анаэробные возбудители характерные для больных в случае:
• аспирации желудочного содержимого (кома, черепно-мозговая травма, алкоголизм)
• проведения оперативных вмешательств на органах брюшной полости.
Этиологическая значимость P. aeruginosa значительно возрастает в случае:
• пребывания больного на ИВЛ
• длительного лечения системными ГКС (употребление преднизолона в дозе 10 мг в сутки)
• терапии антибиотиками широкого спектра действия более 7 суток за последний месяц
• истощения
• "структурных" заболеваний легких (например, бронхоэктазы, муковисцидоз).
Спектр возбудителей госпитальной пневмонии в значительной степени зависит от типа лечебного учреждения, контингента больных, времени возникновения и тяжести течения заболевания, наличия факторов риска госпитальной пневмонии и модификувальних факторов.
Патогенез госпитальной пневмонии . Патогенез госпитальной пневмонии связывают со многими факторами, причем они нередко взаимодействуют друг с другом.
Обязательным условием развития госпитальной пневмонии являются:
• снижение эффективности защитных механизмов организма человека, что обусловлено основным заболеванием, оперативным вмешательством, ИВЛ и др..
• массивная доза микроорганизмов и /или их повышенная вирулентность. Проникновение в дыхательные пути даже единичных высоковирулентных микроорганизмов, устойчивых к действию защитных механизмов макроорганизма, также приводит к развитию госпитальной пневмонии.
Основные пути проникновения инфекции в нижние отделы дыхательных путей:
• аспирация секрета ротовой части глотки, содержит потенциальные возбудители госпитальной пневмонии
• аспирация нестерильного содержимого пищевода /желудка
• вдыхание микробного аэрозоля
• гематогенное распространение микроорганизмов из отдаленного очага инфекции
• непосредственное проникновение возбудителей в дыхательные пути.
Аспирация содержимого ротовой части глотки является основным путем инфицирования при госпитальной пневмонии. Частота аспирации существенно возрастает при потери сознания, нарушении глотания, снижении рвотного рефлекса, угнетении двигательной активности пищеварительного тракта и замедлении опорожнения желудка.
Из многочисленных микроорганизмов "нормальной" микрофлоры верхних дыхательных путей (ротовой и носовой частей глотки) лишь некоторые виды с повышенной вирулентностью способны привести к развитию госпитальной пневмонии. Наиболее чаще это S. pneumoniae, Н. influenzae, М. catarrhalis. Два последних возбудители характерные для курильщиков, больных ХОБЛ. Другая грамотрицательная флора встречается крайне редко, только в 2-3% здоровых лиц выявлено бессимптомное носительство. Частота выявления грамотрицательной флоры растет у лиц пожилого возраста, у больных с сопутствующими заболеваниями - сахарным диабетом, сердечной, почечной и печеночной недостаточностью и др.. S. aureus также проявляют чрезвычайно редко, обычно у больных с факторами риска - пожилой возраст, наркомания, хронический гемодиализ, грипп.
В условиях стационара у пациентов происходит существенное изменение микрофлоры. Практически сразу после госпитализации начинается колонизация кожи и слизистых оболочек верхних дыхательных путей микроорганизмами, циркулирующих в стационаре, прежде грамотрицательной микрофлорой, а также S. aureus.
Вероятность колонизации верхних дыхательных путей грамотрицательной микрофлорой непосредственно связана со степенью тяжести течения основного заболевания (причины госпитализации): в случае заболевания средней степени тяжести количество бессимптомных носителей составляет 30-40%, в случае тяжелого течения и у больных отделения реанимации и интенсивной терапии - 60-70%. Колонизация чаще происходит у больных в коматозном состоянии, с уремией и полиорганной недостаточностью, несколько реже - у больных сахарным диабетом, алкоголизмом, с инфекциями верхних дыхательных путей и с наличием функциональных расстройств.
В отдельных случаях самостоятельным патогенетическим фактором госпитальной пневмонии может быть массивная аспирация нестерильного содержимого пищевода или желудка, колонизация желудка возможна в случае проглатывания бактерий, а также низкого содержания соляной кислоты. Риск аспирации значительно возрастает в бессознательном больных, в находящихся на постельном режиме, после проведения анестезии, интубации трахеи, зондирование желудка, употребление антацидов и блокаторов Н-рецепторов.
Ингаляция аэрозоля, содержащего микроорганизмы - менее распространенный механизм развития госпитальной пневмонии, который имеет основное значение при инфицировании облигатными микроорганизмами, например Legionella sp. Еще меньшее значение (по частоте выявления) имеет гематогенное распространение микроорганизмов с внелегочного очага инфекции (например, эндокардит с поражением трехстворчатого клапана, септический тромбофлебит вен таза)и непосредственное распространение возбудителя из очага инфекции (например, абсцесс печени) или в результате инфицирования при проникающих ранений грудной клетки.
Классификация госпитальных пневмоний. В мире чаще пользуются классификацией госпитальных пневмоний, критерием которой является срок развития заболевания, наличие или отсутствие факторов риска ее развития.
Согласно этой классификации выделяют следующие виды госпитальных пневмоний:
• ранняя госпитальная пневмония - возникает в течение первых 5 суток пребывания в стационаре и обусловлена возбудителями, которые были у больного еще до госпитализации, - S. pneumoniae, Н. influenzae, метицилинчутливий S. aureus (MSSA) и другие представители нормальной микрофлоры ротовой части глотки. Чаще всего эти возбудители чувствительны к традиционно применяемых антимикробных препаратов, а собственно пневмония имеет благоприятный прогноз
• поздняя госпитальная пневмония - развивается не ранее чем после 6-го дня госпитализации и вызвана собственно госпитальной микрофлорой с высоким риском наличия высоковирулентных и полирезистентных возбудителей - P. aeruginosa, Acinetobacter sp., представители семейства Enterobacteriaceae, метициллин S. aureus (MRSA). Такая госпитальная пневмония характеризуется менее благоприятным прогнозом.
Учитывая тяжесть течения заболевания, серьезность прогноза и особенности ведения реанимационных больных выделяют как особую форму так называемую вентилятор-ассоциированной пневмонией (ВАП) - пневмонию, возникшую через 48 ч от начала проведения IIIBJI при отсутствии признаков легочной инфекции на момент интубации.
Этиология ВАП зависит от длительности пребывания на ИВЛ, поэтому ВАП также разделяют на:
• раннюю (ее развитие приходится на первые 5 суток пребывания на ИВЛ)
• поздний (развивается после 5 суток пребывания на ИВЛ).
В случае ранней ВАП вероятными возбудителями являются S. pneumoniae, Н. influenzae, S. aureus (MSSA) и другие представители нормальной микрофлоры полости рта. Развитие поздней ВАП обусловлен P. aeruginosa, Acinetobacter sp., представителями семейства Enterobacteriaceae и MRSA (реже). Части ВАП имеет полимикробной этиологии.
Факторы риска развития госпитальной пневмонии. Учитывая сложность патогенеза госпитальной пневмонии, выделяют значительное количество факторов риска ее развития. Условно их можно разделить на:
• факторы, связанные с состоянием макроорганизма (возраст, тяжесть течения основного заболевания, наличие сопутствующей патологии и др.).
• факторы, повышающие риск колонизации ротовой части глотки и желудка возбудителями госпитальной пневмонии (пребывания в отделении реанимации и интенсивной терапии, применение антибиотиков, антацидов, неадекватная техника выполнения лечебных и диагностических манипуляций, неадекватное обработки рук персонала и дыхательной аппаратуры и т.п.)
• факторы, способствующие рефлюкса и аспирации (проведения ИВЛ, трахеостомия, применение назогастрального зонда, неизменное положение больного на спине)
• факторы, препятствующие нормальному выделению мокроты (интубация, применение морфиноподобных препаратов, иммобилизация).
Для профилактики госпитальной пневмонии наибольшее практическое значение имеет определение эндогенных (связанных с пациентом) и экзогенных (связанных с пребыванием пациента в стационаре) факторов риска развития госпитальной пневмонии. Среди последних наибольшую роль играют длительность госпитализации, проведения лечебных и диагностических манипуляций - эндотрахеальная интубация, фибробронхоскопия, трахеостомия, назогастрального зондирования, ИВЛ, длительность и сложность оперативного вмешательства, медикаментозная терапия.
Риск развития госпитальной пневмонии возрастает после перенесенного оперативного вмешательства. Особенно это актуально для пациентов после операций на органах грудной или брюшной полости, для которых характерны послеоперационная боль, развитие ателектазов, нарушение мукоцилиарного клиренса. При этом относительно простые манипуляции /подходы существенно уменьшают риск развития госпитальной пневмонии:
• адекватное обезболивание
• регулярная физиотерапия (массаж, постуральный дренаж, дыхательная гимнастика)
• стимулирование кашля у пациентов без ИИИВЛ
• ранняя (по возможности) активизация пациентов
• потребление пищи в положении полусидя.
Фибробронхоскопия является самостоятельным фактором риска развития госпитальной пневмонии у пациентов, находящихся на ИВЛ. Во многом это может быть связано с тем, что продвижение через ротовую часть глотки бронхоскопа способствует колонизации нижних отделов дыхательных путей потенциально патогенными бактериями. Кроме этого, нередко большой объем жидкости, которую вводят через бронхоскоп, затрудняет клиренс бактерий из нижних отделов дыхательных путей. И хотя связь между этой врачебной манипуляцией и колонизацией дыхательных путей не является безусловным, рекомендуют четко определить показания к проведению фибробронхоскопии у пациентов, находящихся на ИВЛ.
Искусственная вентиляция легких. Имеющиеся многочисленные докази 6-21-кратного увеличения риска развития госпитальной пневмонии у пациентов, находящихся на ИВЛ, равно как и связи между частотой госпитальной пневмонии и длительностью механической вентиляции. Пребывание эндотрахеальной трубки в дыхательных путях пациента нарушает местные защитные механизмы, а именно целостность эпителия трахеи; затрудняет или полностью исключает выделение бронхиального секрета с помощью мукоцилиарного клиренса и кашля. Эндотрахеальная трубка является своеобразной ловушкой для секрета трахеи, локализуется выше манжеты. Это может привести к колонизации ротовой части глотки нозоко-миальнимы бактериями и контаминировать секрет, который просачивается между раздутой манжетой и стенкой трахеи и проникает в нижние отделы дыхательных путей.
На поверхности интубационной трубки часто образуются биопленки, которые усиливают аккумуляцию бактерий и производящие факторы, снижающие эффективность антибактериальной терапии. Это происходит вследствие того, что в биопленках ниже напряжения кислорода и уменьшенный содержимое железа - это допускает анаэробный рост бактерий и меньшую скорость деления клеток. Вследствие этого снижается активность р-лактамов, поскольку эти антибиотики активны в отношении аэробных бактерий.
Вводить эндотрахеальные трубки и желудочные зонды лучше через рот, чем через нос (снижается риск развития нозокомиального синусита и, возможно, госпитальной пневмонии).
Ограничения в использовании седативных препаратов, которые подавляют кашлевой рефлекс, а также поддержания давления в манжете эндотрахеальной трубки более 20 мм вод. ст. снижают вероятность аспирации бактерий из ротовой части глотки.
Стоит учитывать и вероятность загрязнения увлажнителя в контуре аппарата для ИВЛ, вследствие чего пациент вдыхает аэрозоль, содержащий микробы. Источниками бактерий является поверхность кожи самого пациента, руки врача и медицинской сестры, медицинское оборудование и т.д..
Аспирация, положение пациента и энтеральное питание. Положение пациента на спине также может способствовать аспирации, вероятность которой в значительной степени можно уменьшить, положив больного в положение полулежа. Результаты рандомизированного исследования продемонстрировали 3-разовое снижение частоты госпитальной пневмонии у пациентов отделения реанимации и интенсивной терапии, принимали лекарства в положении полулежа (под углом 45 °). Существует прямая взаимосвязь частоты развития инфекций у пациентов в положении лежа на спине с началом энтерального питания. Скорее всего, это связано с увеличением риска аспирации желудочного содержимого.
Применение отдельных классов лекарственных средств сопровождается увеличением риска развития госпитальной пневмонии. Например, седативные препараты увеличивают риск аспирации, снижают кашльовой рефлекс, что приводит к "застою" бронхиального секрета. В наибольшей степени это выражено у пожилых людей и у пациентов с дисфагией. Применение антацидов и блокаторов Н 2 -рецепторов, которые назначают для профилактики стрессовых язв и желудочно-кишечных кровотечений, за счет повышения рН содержимого желудка способствует бактериальной колонизации его слизистой оболочки.
Клиника и осложнения госпитальной пневмонии подобные таковым при внебольничной пневмонии.
Диагностика и критерии диагноза госпитальной пневмонии
Клиническое обследование остается "отправной точкой" диагностики госпитальной пневмонии. Результаты других методов исследования (в том числе и инвазивных) интерпретируют только с учетом клинической картины госпитальной пневмонии.
Для клинической картины госпитальной пневмонии характерно появление новых инфильтративных изменений на. рентгенограмме органов грудной клетки в комплексе с такими признаками инфекционного заболевания, как лихорадка, выделение гнойной мокроты и /или лейкоцитоз.
В связи с этим к числу формализованных диагностических критериев госпитальной пневмонии относят:
• появление на рентгенограмме новых очагово-инфильтративных изменений в легких
• две из следующих характеристик:
1) температура тела> 39,3 ° С
2) бронхиальная гиперсекреция
3) Pa0 2 /Fi0 2 менее 240 (Ра0 2 - парциальное напряжение кислорода в артериальной крови, мм рт. ст.; FiO z - фракция кислорода во вдыхаемом воздухе,%)
4) кашель, тахипноэ, локальная крепитация, влажные хрипы, бронхиальное дыхание
5) количество лейкоцитов в крови менее 4 • 10 9 /л или более 12 • 10 9 /л , палочкоядерные сдвиги более 10%
6) гнойная мокрота /бронхиальный секрет (более 25 полиморфноядерных лейкоцитов в поле зрения при микроскопии с малым увеличением).
Однако на практике приведены клинические, лабораторные и рентгенологические критерии диагностики госпитальной пневмонии выявляются не всегда бесспорными, особенно у пациентов, находящихся на ИВЛ. Подобные проявления имеют тромбоэмболия ветвей легочной артерии с развитием инфаркта легкого, ателектаз легкого, медикаментозная реакция, легочное кровотечение, острый респираторный дистресс-синдром и др.. Указанные критерии могут быть слишком "расплывчатыми" у пациентов с сопутствующими сердечно-сосудистыми или бронхолегочногоими заболеваниями. Поэтому клинический диагноз госпитальной пневмонии в 10-29% случаев не находит подтверждения аутопсии, а с другой стороны, в 20-40% случаев выявлена на аутопсии госпитальная пневмония не была распознана по данным прижизненного клинико-рентгенологического обследования.
Учитывая вышесказанное, независимо от клинической ситуации, наличия данных соответствующих инвазивных методов исследования, в случае подозрения на госпитальную пневмонию всем пациентам нужно проводить обследование по такой схеме:
• Изучение анамнеза заболевания с целью выявить специфические клинические ситуации, которые определяют возможную этиологическую роль соответствующих возбудителей госпитальной пневмонии с учетом результатов местного микробиологического мониторинга и исследования уровня антибиотикорезистентности возбудителей нозокомиальной инфекции.
• Клиническое обследование.
Клиническая диагностика госпитальной пневмонии направлена на выявление общих (слабость, адинамия, снижение аппетита, лихорадка) и локальных (кашель, выделение мокроты, одышка, боль в груди) респираторных симптомов, а также физических данных (притупленный или тупой перкуторный звук, ослабленное или жесткое бронхиальное дыхание, фокус звонких мелкопузырчатые хрипы и /или крепитации). Выраженность этих признаков зависит от состояния пациента в начале заболевания, тяжести течения основного заболевания, объема и локализации поражения легочной паренхимы, возраста, наличия сопутствующих заболеваний. Все это симптомокомплекс неспецифический для госпитальной пневмонии, но его достаточно для установления предварительного клинического диагноза. Однако у части больных объективные признаки госпитальной пневмонии могут отличаться от типичных или отсутствовать.
У лиц старших возрастных групп, больных с острым нарушением мозгового кровообращения и /или при неадекватной иммунном ответе в клинике заболевания на передний план могут выходить потери сознания, обострение /декомпенсация сопутствующих заболеваний, отсутствие лихорадки .
Скудность симптоматики госпитальной пневмонии наблюдается в послеоперационный период. Основными клиническими проявлениями легочного осложнения нередко бывают лихорадка, не связана с местным процессом в послеоперационной ране, общая интоксикация, одышка, тахикардия.
• Рентгенологическое обследование.
Всем пациентам с подозрением на госпитальную пневмонию нужно сделать рентгенографию органов грудной клетки в двух проекциях (задньопередний и боковой). Ценность этого исследования заключается не только в самом факте визуализации пневмонийнои инфильтрации, т.е. в верификации диагноза пневмонии (как правило, при наличии соответствующих клинических признаков), оценке динамики патологического процесса и полноты выздоровления, а также в возможности провести дифференциальную диагностику с другими заболеваниями. Степень выраженности рентгенологических изменений (распространенность инфильтрации, наличие или отсутствие плеврального выпота, полостей распада) соответствует тяжести заболевания и может быть критерием при выборе антибактериальной терапии.
Проведение дополнительных рентгенологических исследований (рентгенотомография, компьютерной томографии) целесообразно для дифференциальной диагностики при поражениях верхних долей легких, лимфатических узлов, средостения, при уменьшении объема доли легкого, в случае возможного абсцедирования, а также неэффективности предшествующей антибактериальной терапии.
• Лабораторное обследование.
Результаты клинического анализа крови не позволяют определить потенциального возбудителя пневмонии. Однако лейкоцитоз более 10-12Т0 9 /л и сдвиг лейкоцитнои формулы влево (палочкоядерных нейтрофилов более 6%) свидетельствует высокую вероятность бактериальной инфекции, а лейкопения ниже ЗТ0 9 /л или лейкоцитоз выше 25Т0 9 /л являются неблагоприятными прогностическими признаками госпитальной пневмонии.
Биохимические анализы крови (функциональные печеночные, почечные тесты, гликемия и др.). не несут специфической информации, однако при наличии отклонений от нормальных величин свидетельствуют о поражении некоторых органов /систем, имеющая несомненное клиническое и прогностическое значение.
У больных с признаками дыхательной недостаточности, обусловленной распространенной пневмонийною инфильтрацией, массивным плевральным выпотом, развитием пневмонии на фоне хронического обструктивного заболевания легких следует определять насыщенность крови кислородом или газы артериальной крови. Гипоксемия - Sa0 2 менее 90% или Ра0 2 ниже 60 мм рт. ст. (При дыхании комнатным воздухом) - прогностически неблагоприятный признак и свидетельствует о необходимости лечения больного в условиях отделения реанимации и интенсивной терапии. Распространена практика исследования газов в капиллярной крови имеет относительную диагностическую ценность, недостаточную воспроизводимость и часто не соответствует изменениям газов артериальной крови.
При наличии на латерограми плеврального выпота (с толщиной слоя свободной жидкости более 1 см) для исключения эмпиемы плевры следует проводить диагностический торакоцентез. Исследование плевральной жидкости должно включать определение количества лейкоцитов и лейкоцитнои формулы, рН, содержания белка, глюкозы, активности лактатдегидрогеназы, окраски мазков по Граму и на кислотоустойчивыебактерии, проведения посевов на выявление аэробных, анаэробов и М. tuberculosis.
Серологические исследования крови имеют ограниченную диагностическую ценность, как правило, их не применяют при обследовании пациентов с подозрением на госпитальную пневмонию.
Сейчас есть коммерческие тест-системы для определения антигенов S. pneumoniae и L. pneumophila в моче. Эти тесты благодаря скорости их выполнения позволяют в ряде случаев выбрать адекватную стартовую антимикробную терапию или объяснить эпидемиологические взаимосвязи. Тесты имеют высокую специфичность, однако из-за их относительно низкую чувствительность даже в случае отрицательного результата и невозможности клинически исключить легионельозну этиологии госпитальной пневмонии следует дополнительно проводить культуральное, а в случае необходимости - молекулярно-генетическое исследование.
Микробиологическая диагностика . Микробиологическую диагностику госпитальной пневмонии целесообразно проводить как можно быстрее после установления клинического диагноза. Материал для исследования желательно забирать до начала антибактериальной терапии. Однако, несмотря на трудности проведения микробиологического исследования в полном объеме, не следует откладывать назначения антибиотикотерапии.
Если антимикробную терапию уже проводят, ее не стоит менять в течение 72 ч перед забором материала. Также нецелесообразно временно прекращать терапию для проведения диагностических исследований.
микробиологическое исследование обязательно подлежат кровь больного (для получения гемокультуры), а также патологический материал, полученный из очага инфекции, то есть с дистальных отделов бронхиального дерева и альвеол.
По мнению большинства авторов, диагностическая ценность материала зависит от способа его получения. Наименьшее диагностическую значимость имеют результаты исследования транстрахеального аспирата, мазков, полученных из интубационных трубок, зева, трахеостомы. Далее, в порядке возрастания диагностической ценности, нужно мокроты, полученное во время глубокого отхаркивание, жидкость бронхоальвеолярного лаважа и содержание, полученный при бронхоскопии с использованием "защищенных" щеток.
Исследование гемокультуры имеет обязательный характер при обследовании пациента с подозрением на госпитальную пневмонию. До начала антибактериальной терапии следует сделать посевы венозной крови (проводят забор 2 образцов крови из 2 разных вен). Во время забора крови следует придерживаться классических правил асептики и обрабатывать место забора 70% этиловым спиртом, затем 1-2% раствором йода. У пациентов осуществляют забор не менее 20 мл крови для каждого образца, поскольку это существенно повышает частоту выявления возбудителей инфекции. Исследование гемокультуры имеет важное диагностическое и прогностическое значение. У пациентов с положительной гемокультурой возрастает вероятность осложненного течения госпитальной пневмонии. К сожалению, чувствительность этого метода не превышает 10-25%, а специфичность ограничивается большой вероятностью того, что в госпитализированных пациентов (особенно тяжелобольных) могут быть многочисленные источники бактериемии. Соответственно микроорганизмы, выделенные из крови, можно рассматривать как возбудителей госпитальной пневмонии лишь в тех случаях, если их находят и при исследовании образцов из нижних отделов дыхательных путей.
Микробиологическое исследование мокроты (бактериоскопия окрашенных по Граму мазков, посев) продолжает оставаться методом, его чаще применяют для диагностики госпитальной пневмонии, однако диагностическая ценность этого метода в аспекте выявления возможной этиологии заболевания в пациентов с подозрением на госпитальную пневмонию существенно ограничена. Это связано с очень низкой (0-30%) специфичностью метода, объясняют контаминацией образцов мокроты микрофлорой, которая обычно колонизирует ротовую часть глотки /верхние дыхательные пути у госпитализированных пациентов.
Сейчас основное назначение культурального исследования мокроты - выявление устойчивых к антибиотикам штаммов вероятных возбудителей госпитальной пневмонии.
Повысить информативность этого исследования и избежать ряда ошибок можно в случае строгого соблюдения правил сбора мокроты и проведения его макро-и микроскопического оценки перед посевом на питательные среды.
Бактериологическое исследование проводят после оценки окрашенного по Граму мазка при условии наличия в нем более 25 лейкоцитов и менее 10 эпителиальных клеток при малом увеличении (хЮО). Обнаружение в мазке значительного количества грамположительных или грамотрицательных микроорганизмов с типичной морфологией может быть ориентиром для эмпирической терапии.
В интубированных пациентов с подозрением на госпитальную пневмонию доступным методом получения материала для микробиологического исследования является эндотрахеальная аспирация. Подобно исследование мокроты в неинтубованих пациентов исследования материала эндотрахеальной аспирации имеет ограниченную диагностическую ценность - при чувствительности, достигает 82-88%, специфичность не превышает 27-33%. В этой связи основное значение микробиологического исследования эндотрахеальных аспирантов заключается в исключении неопределенных микроорганизмов (в случае отрицательных результатов исследования) из перечня вероятных возбудителей госпитальной пневмонии. Так, отсутствие в материале Pseudomonas sp. свидетельствует крайне низкую ймовирнис?? Ь синегнойной этиологии заболевания. При количественной оценки диагностически значимыми являются титры микробных тел 10 5 КОЕ /мл и выше. В случае превышения указанных предельных значений микробной обсемененности значительно возрастает специфичность исследования (до 95%), но одновременно существенно снижается его чувствительность - до 43%.
Роль инвазивных диагностических методов при обследовании пациентов с клинически предполагаемой госпитальной пневмонией является противоречивой. Наиболее информативным из них является "защищена" браш-биопсия слизистой оболочки бронхов. Однако воспроизводимость этого метода в того же больного невысока. Еще одно обстоятельство, которое ограничивает диагностическую ценность "защищенной" браш-биопсии, - снижение количества микробных тел в случае предварительного проведения антибактериальной терапии.
В отличие от "защищенной" браш-биопсии при исследовании образца, полученного при проведении бронхоальвеолярного лаважа, можно судить о микробное обсеменение огромного количества альвеол (10 6 ). Чувствительность и специфичность исследования образца бронхоальвеолярного лаважа при титре микробных тел более 10 4 КОЕ /мл достигают 91% и 100% соответственно.
Роль и место неинвазивных и инвазивных ("защищена" браш-биопсия, бронхоальвеолярный лаваж) диагностических методов при обследовании пациентов с подозрением на госпитальную пневмонию должны определяться с учетом клинической целесообразности и возможности их применения. При этом следует знать, что внедрение микробиологической диагностики с целью минимизировать частоту ложноположительных случаев госпитальной пневмонии не дает ожидаемого результата в случае высокой вероятности диагноза заболевания с клинико-рентгенолог-ческих позиций. "Конечная границей", определяющий диагностическую ценность неин-вазивних и инвазивных методов исследования, результаты лечения. Однако до сих пор не получено доказательств, которые бы свидетельствовали улучшения конечного результата у больных госпитальную пневмонию в случае применения "агрессивной" диагностической тактики.
Антибактериальная терапия госпитальной пневмонии . Диагноз госпитальной пневмонии - безусловное показание к применению антибиотиков, является основой лечения таких больных. Антибактериальное лечение нужно начинать сразу после установления диагноза. Совершенно неприемлемо промедления со срочным назначением антибиотиков пациентам с тяжелым течением заболевания из-за отсутствия результатов бактериоскопии и посева мокроты, поскольку задержание введения первой дозы антибиотика значительно повышает риск смерти таких больных.
Важнейший фактор повышения выживаемости больных госпитальную пневмонию - своевременное назначение адекватной антибиотикотерапии.
Критерием адекватности антибиотикотерапии является активность приме-ного (ых) антибиотика (ов) по всех возможных и /или выявленных микроорганизмов (за исключением P. aeruginosa, в отношении которого активными должны быть не менее двух антибиотики).
Основные антимикробные средства, используемые для лечения больных госпитальную пневмонию, приведены в табл. 1.

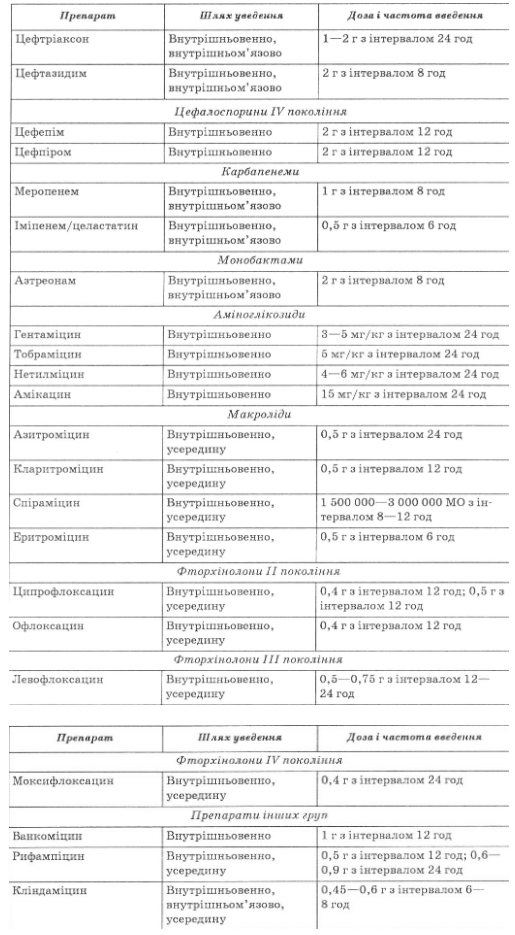
Принципы антибиотикотерапии больных госпитальную пневмонию
При выборе и проведении антибиотикотерапии согласно действующих рекомендаций, в частности Американского торакального общества (ATS), нужно учитывать следующие моменты:
• что тяжелое течение госпитальной пневмонии, то широкий и более тяжело прогнозируемый спектр патогенов
• чем длиннее период пребывания больного в больнице и в отделении реанимации и интенсивной терапии, то чаще случается полимикробная инфекция и большая вероятность наличия мультирезистентных штаммов патогенов.
настоящее время при проведении антибиотикотерапии больных госпитальную пневмонию пользуются двумя основными принципами - эскалации и деэскалации.
Принцип эскалации ("увеличение") предусматривает выбор для начальной терапии антибактериальных препаратов с узким спектром действия, с последующим расширением спектра охвата микрофлоры в случае неэффективности проводимой терапии. Режим эскалации, вероятно, эффективен в случае инфекций, не угрожающих жизни больного, когда можно дождаться результатов посева и производить "целенаправленную" терапию.
Принцип деэскалации ("меншення") применяют при наличии инфекции, угрожающее жизни больного, когда начинают лечение ("стартовая терапия") из одного или более антибиотиков широкого спектра, а после идентификации возбудителя и определение чувствительности решают вопрос о возможном переходе на препарат с более узким спектром действия. Режим деэскалации комбинирует в себе сильное антибактериальное действие и высокую стоимость, поэтому при выборе этого режима нужно быть уверенным в правильности установления диагноза госпитальной пневмонии. Если антибиотик (и) широкого спектра применяют, когда у больных еще не развилась госпитальная пневмония, то это может приводить к селекции полирезистентных штаммов микроорганизмов, а в дальнейшем - к увеличению ризику развития крайне тяжелой нозокомиальной инфекции, в том числе госпитальной пневмонии или ВАП.
Из практических соображений различают эмпирическую антибиотикотерапию (если не определено этиологию заболевания) и антибиотикотерапию больных госпитальную пневмонию с установленной этиологией. Поскольку сейчас не существует эффективных методов этиологической экспресс-диагностики госпитальной пневмонии, в реальных условиях начальная этиотропная терапия практически всегда эмпирическая.
Эмпирическая антибиотикотерапия больных госпитальную пневмонию
Найвиправданиший подход к эмпирической антибиотикотерапии больных госпитальную пневмонию - лечение зависимости от сроков возникновения пневмонии ("ранняя", "поздняя") и наличия модификувальних факторов, риска инфицирования полирезистентными штаммами микроорганизмов (табл. . 2, 3).

Антибактериальная терапия больных госпитальную пневмонию установленной этиологии
Антибактериальные препараты для лечения больных госпитальную пневмонию установленной этиологии приведены в табл. 4. Перечень препаратов, которые имеют подтвержденную клиническую эффективность при лечении больных госпитальную пневмонию установленной этиологии, не следует ограничивать приведенными в этой таблице. Отбор новых препаратов для использования как средств выбора должно основываться на экспертном оценивании опубликованных результатов клинических испытаний, а также учитывать национальные и международные рекомендации.
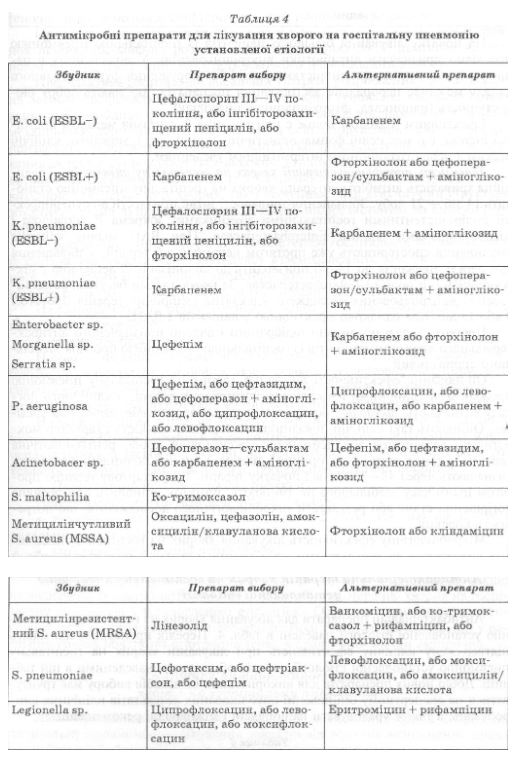
В начале лечения большинства пациентов с госпитальной пневмонией необходимо назначать антибиотики внутривенно. В дальнейшем у пациентов с клинической эффективностью терапии и без нарушения функции ЖКТ возможно пероральное применение препаратов, которые имеют хорошую биодоступность (например, фторхинолонов и линезолида).
Эффективным подходом также назначения (3-лактамов методом постоянной инфузии, имеющий определенные фармакокинетические, экономические и, возможно, клинические преимущества перед традиционным интермитивним вводом.
Длительность антибиотикотерапии больных госпитальную пневмонию. Традиционная длительность антибиотикотерапии больных госпитальную пневмонию составляет 14 суток - 21 сутки. Увеличение продолжительности может привести к суперинфекции полирезистентными госпитальными возбудителями, в частности P. aeruginosa и микроорганизмами семейства Enterobacteriaceae. При ВАП значительное клиническое улучшение наблюдается уже в течение первых 6 суток терапии, а увеличение длительности лечения до 14 суток приводит к колонизации P. aeruginosa и микроорганизмами семейства Enterobacteriaceae. По результатам многих рандомизированных контролируемых исследований адекватная эмпирическая терапия в течение 8 или 15 суток была одинаково эффективной у пациентов с весов.
Прогноз
При правильно подобранной и вовремя назначенного антибактериального лечения пациентов с госпитальной пневмонией прогноз в большинстве случаев благоприятный.
Оценка эффективности лечения больных госпитальную пневмонию проводят по клиническим и микробиологическим критериям. С клинической точки зрения определяют: лечение, улучшения, ухудшения, рецидив, летальный исход. Оценивают такие клинические показатели, как лихорадка, количество и характер мокроты, лейкоцитоз или лейкопения, оксигенация крови, рентгенологическая картина, а также состояние других органов и систем. Клиническое улучшение обычно определяют через 48-72 ч от начала терапии, так стартовую терапию в течение этого времени в основном не меняют. Исключение составляет прогрессивное ухудшение состояния или результаты микробиологического исследования, требующие коррекции.
Микробиологическую эффективность лечения больных госпитальную пневмонию определяют по результатам исследования секрета дыхательных путей и оценивают как эрадикацию, суперинфекции (появление нового возбудителя), рецидив (элиминация с последующей появлением первичного возбудителя) или персистенцию. Однако микробиологические параметры, которые указывают на необходимость изменить терапию, недостаточно изучены.
Результаты рентгенографического исследования органов грудной клетки имеют ограниченную ценность при определении динамики госпитальной пневмонии с тяжелым течением, поскольку часто отмечают первичное рентгенологическое ухудшение, особенно у пациентов с бактериемии или инфекцией, вызванной высоковирулентные микроорганизмами. Кроме того, у лиц пожилого возраста или с сопутствующими заболеваниями (например, X03J1) положительную динамику рентгенологических симптомов наблюдают медленнее, чем клинических.
Прогностически неблагоприятными являются следующие показатели: поражения новых участков легких, увеличение размера инфильтрата более 50% в течение 48 ч, появление очагов деструкции, наличие большого плеврального выпота.
Профилактика госпитальной пневмонии . Потребность разработки и внедрения средств профилактики госпитальной пневмонии обусловлена высокой распространенностью ее, особенно среди больных хирургических отделений, пациентов с тяжелой механической и термической травмой и среди лиц с нарушением сознания, что приводит к сбольшення срока госпитализации, повышение расходов на лечение, а также сопровождается высокой атрибутивной летальностью. Высокие затраты на лечение пациентов с госпитальной пневмонией обусловлены как исходной тяжестью состояния больных, так и особенностями этиологической структуры возбудителей, среди которых преобладают бактерии, полирезистентные к антимикробным средствам.
С учетом факторов риска и патогенеза госпитальной пневмонии профилактика должна состоять из комплекса взаимосвязанных мероприятий организационного, технического и медицинского характера, которые снижают вероятность контаминации и инфицирования и усиливают антиинфекционной защиты самого пациента.
Наивысшая степень обоснованности имеют такие направления профилактики госпитальной пневмонии:
1. Обучение персонала.
Обучение персонала правилам ухода за больными с нарушенным сознанием и бульбарными расстройствами; пациентов, которым оказывают респираторную поддержку, осуществляют небулайзерную терапию или энтеральное питание, с позиции предотвращения воздействия факторов, которые провоцируют развитие госпитальной пневмонии.
Важнейшими из правил ухода является соблюдение угла наклона головного конца кровати (30-40 °), периодический контроль положения желудочного зонда, перистальтики и усвоения смеси, вводимой давления в манжете эндотрахеальной или трахеостомической трубки, обработки кожных покровов.
2. Прерывание путей передачи инфекции.
Прерывание путей передачи инфекции включает:
• использование одноразового стерильного материала, контактирующего с дыхательными путями пациента
• ежедневная стерилизация небулайзера
• изменение увлажнителя в случае его загрязнения
• своевременное удаление конденсата из дыхательного контура
• использование стерильного раствора для небулайзерной терапии, увлажнения воздуха и др..
• стерилизация многоразового дыхательного контура перед его использованием в нового пациента. Не рекомендуется часто менять контур у одного пациента (целесообразно не чаще чем каждые 48 ч)
• тщательная аспирация секрета из надманжеткового пространства с промывкой катетера только стерильным раствором
• изменение емкости для сбора аспирата перед использованием в другого пациента.
3. Предотвращение переносу бактерий медицинским персоналом.
Предотвращает переносу бактерий медицинским персоналом правильная организация процесса обработки рук: использование жидкого мыла, антисептиков и одноразовых салфеток. Рекомендуется мыть руки перед надеванием и после снятия перчаток. Предотвратить перекрестной контаминации помогает замена перчаток перед началом работы с новым пациентом. Нужно выявлять и проводить санацию носителей MRSA среди персонала лечебного учреждения.
Очень действенной мерой является изоляция пациентов с инфекционными заболеваниями и организация помощи в отделении реанимации и интенсивной терапии по принципу "один пациент - одна медицинская сестра". Такая тактика особенно оправдана в случае инфекций, вызванных полирезистентными штаммами бактерий, такими как MRSA.
4. Ограничение использования сопутствующих лекарственных средств, которые повышают риск эндогенного инфицирования.
Риск инфицирования нижних дыхательных путей микрофлорой ротовой части глотки и пищеварительного тракта неизбежно увеличивается в случае нарушения сознания, угнетение кашлевого рефлекса, повышение рН желудка.
Рациональное назначение снотворных и седативных средств, наркотических анальгетиков, миорелаксантов, антацидов значительно снижает частоту развития госпитальной пневмонии за счет ограничения процесса транслокации микрофлоры в дыхательные пути. Важным подспорьем в этом является использование современных вспомогательных режимов ИВЛ и ненаркотических анальгетиков, устранения пареза кишечника. Для предотвращения стрессовым язвам пищеварительного тракта следует отдавать предпочтение Н 2 -блокаторам.
5. Эпидемиологический контроль.
Эпидемиологический контроль заключается в наблюдении пациентов группы риска развития нозокомиальных инфекций; учета распространенности этих инфекций; анализе этиологической структуры возбудителей, характера и уровня антибиотикоре-резистентности.
6. Селективная деконтаминация ротовой части глотки и пищеварительного канала.
Классическая схема селективной деконтаминации (СДК) ЖКТ основывается на сочетании энтерального (через зонд) назначения неабсорбивних антибиотиков (аминогликозиды и полимиксин) с амфотерицином В, обработки ротовой части глотки 2% пастой, содержащий эти препараты, и парентерального введения антибиотиков широкого спектра действия (цефалоспорины III поколения или ципрофлоксацин). Главная роль СДК - предотвращение избыточной колонизации ротовой части глотки и кишечника грамотрицательными аэробами, а также профилактика первичного и вторичного эндогенного инфицирования.
Комбинация системного назначения антибиотиков с СДК приводит к статистически значимому снижению распространенности инфекций нижних отделов дыхательных путей и летальности в обще?? Ьний популяции пациентов отделения реанимации и интенсивной терапии, находящихся на ИВЛ.
Влияние СДК на снижение летальности у больных терапевтического профиля не доказан. Возможно, отсутствие снижения летальности у этих пациентов связана со значительно меньшей оборачиваемостью основного патологического процесса (острые нарушения мозгового кровообращения, декомпенсация хронической сердечной недостаточности, острая печеночная недостаточность и др.)., А также исключением из анализа некоторых категорий хирургических больных, в том числе с высоким риском развития осложнений (операции на пищеводе и сердце, трансплантация печени).
общем проведения СДК можно рекомендовать отдельным категориям хирургических больных с высоким риском развития ВАП, но потенциально обратимым основным патологическим процессом (например, с политравмой, изолированной черепно-мозговой травмой, абдоминальным сепсисом). Применение СДК как обязательного стандарта профилактики не оправдано с экономической точки зрения и позиций эпидемиологических последствий для данного отделения реанимации и интенсивной терапии.
Риск развития госпитальной пневмонии можно снизить посредством проведения антисептической деконтаминации зубных пластинок 0,2% хлоргек-сидиновим гелем (трижды в сутки) в течение всего периода проведения ИВЛ.
7. Профилактическое назначение антибактериальных препаратов.
На сегодня отсутствуют аргументированные доказательства эффективности системного назначения антибактериальных препаратов с целью профилактики госпитальной пневмонии у пациентов с факторами риска, в том числе и тем, которые находятся на Ш ВЛ.
Назначение цефалоспоринов I-III поколения уменьшает риск возникновения "ранней" госпитальной пневмонии, однако способствует развитию "поздней" госпитальной пневмонии, что вызвано неферментативными грамотрицательными бактериями и MRSA. Нет рекомендаций экспертов относительно обязательного назначения антибиотиков для профилактики ВАП у больных без исходного инфекционного процесса бактериального происхождения. Принятие индивидуального решения должно основываться на характере основной и сопутствующей патологии, прогнозируемой продолжительности ИВЛ и риска аспирации на догоспигальному этапе при наличии нарушений сознания.
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.