Эпидемиология и этиология
Сердечная недостаточность - это клинический синдром, который основывается на неспособности сердца как насоса обеспечить снабжение органов и тканей кровью в объеме, необходимом для их нормального метаболизма . Иными словами, при сердечной недостаточности развивается несоответствие между производительностью сердца и потребностью тканей в кислороде и питательных веществах. Согласно определению, приведенному в Рекомендациях ЕТК (2001), сердечную недостаточность следует рассматривать как "патофизиологический синдром, при котором в результате того или иного заболевания сердечно-сосудистой системы происходит снижение насосной функции сердца, что приводит к дисбалансу между гемодинамической потребностью организма и возможностями сердца" .
Критериями сердечной недостаточности являются:
1) снижение МОС
2) циркуляторная гипоксия с увеличением артериовенозной разницы по кислороду
3) венозный застой, то есть повышение давления на путях кровотока к одного или обоих желудочков сердца.
Сердечная недостаточность означает неспособность поддерживать адекватный сердечный выброс и обеспечения его нормального уровня за счет напряжения компенсаторных механизмов, прежде всего, увеличение конечно-диастолического объема (КДО) и конечно-диастолического давления ( КДТ) в желудочке соответствии с механизмом Франка-Старлинга. В первом случае это явная, а во втором - скрытая (субклиническая) сердечная недостаточность.
Снижение насосной функции сердца, т.е. МОС, бывает абсолютным и относительным. Относительное уменьшение МОС может быть обусловлено первичным повышением метаболических запросов органов и тканей, например, при тиреотоксикозе, или снижением кислороднотранспортной функции крови при анемии (вариант сердечной недостаточности с высоким МОС). Следует отметить, что для ранних стадий сердечной недостаточности характерен неизмененный уровень МОС в состоянии покоя, что, однако, не способен в достаточной степени повышаться при росте метаболических потребностей тканей в условиях физического или эмоционального напряжения.
Эпидемиология . Данные американских и европейских эпидемиологических исследований свидетельствуют о том, что хроническая сердечная недостаточность является одним из самых распространенных и прогностически неблагоприятных состояний. Результаты известного Фремингемского исследования, выполненного в США, показали, что в популяции лиц старше 45 лет количество больных с клинически выраженной ХСН составляет примерно 2,5%. Частота этого синдрома увеличивается с возрастом. Так, если в популяции людей в возрасте 50 - 59 лет его частота составляет 1%, то в возрасте свыше 80 лет его частота достигает 10%. Хроническая сердечная недостаточность является одной из частых причин госпитализации и смертности населения земного шара.
В международных клинико-эпидемиологических исследованиях показано, что последние десятилетия показатель выявления хронической сердечной недостаточности резко возрастает, что связывают с "старением" населения, улучшением диагностики и лечения заболеваний сердечно-сосудистой системы, которые приводят к развитию хронической сердечной недостаточности (прежде всего, ИБС, инфаркт миокарда, артериальная гипертензия). Прогноз при хронической сердечной недостаточности остается неблагоприятным. Летальность при клинически выраженной хронической сердечной недостаточности составляет 40-66% в год, превосходя такую, например, от бронхогенного рака легких и рака предстательной железы и коррелирует со степенью выраженности синдрома, составляя при СН IV ФК 50%, при III ФК 40% и II ФК 30% в год.
Этиология . Хроническая сердечная недостаточность может осложнять течение любого заболевания сердца. Однако наиболее частыми причинами ее развития является ИБС и артериальная гипертензия. При хронической сердечной недостаточности наблюдаются нарушения основных функций сердца: сокращение (систолическая дисфункция) и /или расслабления (диастолическая дисфункция).
Согласно современной нейрогуморальной теории, хроническая сердечная недостаточность развивается по единым патофизиологическими законами независимо от этиологии повреждения миокарда.
Причины
Основными причинами хронической сердечной недостаточности с преимущественно систолической дисфункцией желудочков являются:
1) очаговые поражения миокарда с уменьшением массы жизнеспособного миокарда: инфаркт миокарда, постинфарктный кардиосклероз и диффузный кардиосклероз
2) диффузные поражения миокарда: миокардиты и значительная часть кардиомиопатий, в том числе ятрогенных.
Главными причинами хронической сердечной недостаточности с первичным развитием диастолической дисфункции являются заболевания, сопровождающиеся нарушением наполнения желудочков сердца:
1) стеноз левого или правого предсердно-желудочковых отверстий
2) констриктивный и экссудативный перикардиты, киста или опухоль перикарда
3) заболевания с повышенной жесткостью камеры и (или) миокарда желудочков вследствие его гипертрофии, распространенного фиброза (склероза) или инфильтративного поражения: артериальная гипертензия, рестриктивная кардиомиопатия (эндомиокардиальный фиброз), амилоидоз и другие инфильтративные поражения миокарда, фиброэластоз, некоторые случаи ИБС.
Патогенез
Развернутыей клинической картине сердечной недостаточности обычно предшествует более или менее длительный период бессимптомной дисфункции левого желудочка, что обеспечивается благодаря включению сердечных и периферийных механизмов поддержания его насосной функции.
Сердечные компенсаторные механизмы заключаются в увеличении ЧСС и сократимости миокарда вследствие адренергической стимуляции и увеличение венозного возврата крови, что приводит к увеличению КДО и КДТ в желудочках сердца. Нарастание КДТ, с одной стороны, способствует сохранению сердечного выброса за счет включения механизма Франка-Старлинга, с другой - приводит к увеличению напряжения стенки желудочка (миокардиального стресса). Для его нормализации согласно уравнению Лапласа: 5 = PV /h (8 - конечно-диастолическое напряжение стенки желудочка, Р - конечно-диастолическое давление, V - конечно-диастолический объем, h - толщина стенки желудочка) развивается гипертрофия миокарда, также способствует сохранению его сократительной способности. Сердечные механизмы компенсации тесно взаимосвязаны между собой и реализуются под влиянием циркулирующих и местных нейрогормонов (ренин, альдостерон, эндотелий, вазопрессин, брадикинин, простагландин, азота оксид, натрийуретический пептид, провоспалительные цитокины и др..) И нарушений экспрессии генов, ответственных за синтез коллагенового матрикса.
Гипертрофия миокарда, сначала компенсаторная, приводит к уменьшению расслабления и повышения жесткости миокарда с ухудшением диастолического наполнения желудочка из-за нарушения обмена кальция и отложение коллагена в межклеточном пространстве. Снижение плотности Р-адренорецепторов и нарушение сократительной способности гипертрофированных кардиомиоцитов из-за нарушения синтеза сократительных белков может приводить также к систолической дисфункции. Негативное влияние на насосную функцию желудочка оказывает также ухудшение коронарной перфузии при гипертрофии левого желудочка вследствие увеличения диффузной расстояния для кислорода между капиллярами и кардиомиоцитами и уменьшение эндотелий вазодила-ции.
Периферийные компенсаторные механизмы направленные на противодействие снижению AT и перфузии тканей и способствуют повышению активности вазоконстриктор-ных нейрогормонов (симпатико-адреналовой системы, ренин-ангиотензиновой системы, эндотелина и вазопрессина), АДГ и уменьшению сродства гемоглобина к кислороду.
Уменьшение раздражения барорецепторов аорты как следствие снижение сердечного выброса, а также активация ренина, развивается в случае ухудшения перфузии почек, приводят к активизации симпатической части вегетативной нервной системы и важнейших гуморальных регуляторных систем. При этом стимуляция р,-адренорецепторов способствует повышению сократимости миокарда и ЧСС, а а-адренорецепторов - сужение артериол (поддержание AT) и вен (увеличение венозного кровотока к сердцу). Повышение давления в левом предсердии, развивающаяся при систолической и диастолической дисфункции левого желудочка, стимулирует секрецию предсердного натрийуретического пептида (гормона), а повышение миокардиального стресса в желудочках - секрецию так называемого мозгового натрийуретического пептида. Эти биологически активные вещества способствуют увеличению натрийуреза и диуреза, противодействуют констрикторному воздействии на сосуды норадреналина и ангиотензина II и уменьшают секрецию альдостерона.
При реализации действия факторов компенсации наряду с полезными отмечают более или менее выраженные неблагоприятные эффекты, которые при определенных условиях начинают преобладать. Так, длительная вазоконстрикция способствует прогрессивному ухудшению функции эндотелия, что усиливает сужение сосудов, снижению скорости клубочковой фильтрации, нарушение функции скелетных мышц влияет на способность выполнять физическую нагрузку. При расширении камеры левого желудочка при реализации механизма Франка-Старлинга и растяжении его миокарда более определенную величину прирост ударного выброса прекращается и он даже начинает снижаться, что сопровождается значительным повышением давления на путях кровотока с развитием транссудации жидкой части плазмы в ячейки (альвеолы).
Активизация ренин-ангиотензин-альдостероновой системы, сначала способствует увеличению ударного объема за счет увеличения венозного кровотока к сердцу, впоследствии приводит к обратному результату - снижение ударного объема из-за резкого повышение постнагрузки. При этом значительное увеличение гидростатического давления в капиллярах приводит к развитию отеков, что может сопровождаться снижением концентрация Na + в крови через выраженное задержания воды под влиянием антидиуретического гормона.
В неблагоприятных биологических эффектов нейрогормональной активизации относятся также прямое повреждение кардиомиоцитов, их апоптоз (гибель жизнеспособных клеток, вызванная "запуском" соответствующей программы в случае нарушения экспрессии генов). К уменьшению массы жизнеспособных кардиомиоцитов приводят также активизация свободных радикалов 0 2 , оказывающие непосредственное повреждающее действие на мембраны кардиомиоцитов и стимулируют их апоптоз. Сердечная недостаточность сопровождается также развитием неспецифического асептического с вялым течением системного иммунного воспаления. Активизация металлопротеиназ, возникающая при этом, способствует разрушению в миокарде интерстициальной ткани и, как следствие, активизации фиброза и заместительного склерозв.
Большое значение в компенсации симптомов хронической сердечной недостаточности имеет замедление скорости кровотока, что создает благоприятные условия для увеличения отдачи кислорода и питательных веществ крови тканям и проявляется увеличением артериовенозной разницы по кислороду. Этому же способствует уменьшения сродства гемоглобина к кислороду в условиях гипоксии и ацидоза.
На ранних стадиях хронической сердечной недостаточности компенсаторные механизмы обеспечивают поддержание нормального МОС и давления в полостях сердца как в состоянии покоя, так и во время физической нагрузки. В дальнейшем при сохранении компенсации в состоянии покоя возникает ее срыв во время нагрузки (меньший прирост МОС, снижение ударного объема и фракции выброса и повышение КДТ в желудочке). В развернутой стадии декомпенсации увеличение КДО и КДТ пораженного желудочка отмечается и в состоянии покоя. В случае преимущественного нарушение систолической функции эти показатели растут параллельно друг другу, часто с большим приростом КДО, что сопровождается снижением фракции выброса, тогда как для первичной диастолической дисфункции характерны значительное увеличение КДТ и давления крови на путях кровотока к желудочка при неизменном их КДО и фракции выброса.
При хронической сердечной недостаточности наблюдают также выраженные нарушения метаболизма миокарда, которые включают:
1) нарушение утилизации энергии, т.е. превращение химической энергии АТФ в механическую энергию сокращения миокарда вследствие уменьшения активности Са 2 + -зависимой АТФазы миозина
2) нарушение сочетание возбуждения с сокращением, что приводит к уменьшению количества Са 2 + , поступающих в клетку при ее деполяризации
3) нарушение образования энергии, т.е. окислительного фосфорилирования, с истощением запасов макроэргических фосфатов - АТФ и креатинфосфата.
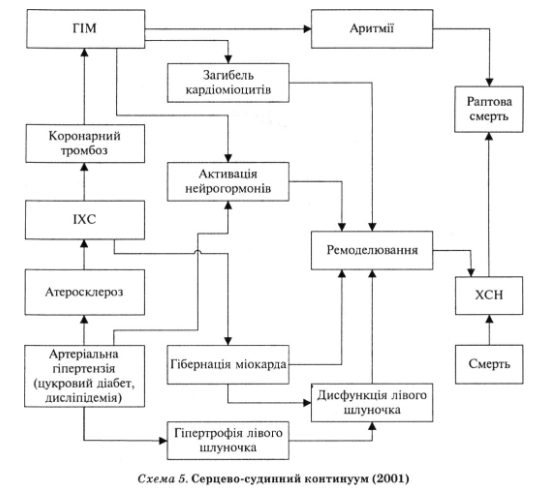
На Европейском конгрессе кардиологов в 2001 г. было предложено теорию единого сердечно-сосудистого континуума, или непрерывного развития сердечно-сосудистых заболеваний от факторов риска до гибели больного (схема 5). Согласно этой концепции, основными факторами риска хронической сердечной недостаточности является артериальная гипертензия, дислипидемия и диабет, которые индуцируют развитие ИБС, в том числе инфаркт миокарда. Следствием этих состояний является гипертрофия миокарда левого желудочка, гибернация (потенциально обратима дисфункция вследствие недостаточного кровоснабжения) и /или гибель кардиомиоцитов с последующей дисфункцией левого желудочка и его ремоделированием.
ремоделирования левого желудочка является патоморфологических субстратов хронической сердечной недостаточности и включает изменение формы и (или) величины его полости, массы, структуры, ультраструктуры и метаболизма миокарда, возникающее в ответ на первичное повреждение миокарда (например, при ИБС) или функционирование в условиях перегрузки объемом и (или) сопротивлением (например, при клапанных пороках сердца).
Главными признаками ремоделирования левого желудочка сердца является его гипертрофия, дилатация камеры (увеличение КДО) и потеря эллиптичности с сферизациею полости, асинхронным сокращением миофибрилл и разрушением соединительнотканного каркаса миокарда.
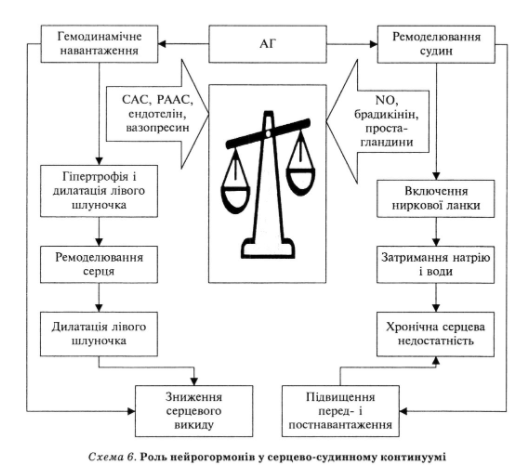
Одной из главных причин ремоделирования является гиперактивация нейрогор-монив (схема 6). Согласно концепции сердечно-сосудистого континуума, при хронической сердечной недостаточности следует говорить не о чрезмерной активизации нейрогормональных систем, а о дисбалансе активности двух групп нейрогормональных факторов:
1) факторов пролиферации клеток (кардиомиоцитов и клеток интерстициальной ткани), их повреждения и, как следствие, ремоделирования желудочков (ренин-ангиотензиновая и симпатико-адреналовой системы, эндотелий, вазопрессин);
2) вазодилатацийних, диуретических и антипролиферативное факторов (NO-эндотелиальный релаксационный фактор, натрийуретический пептид, брадикинин, простациклин).
Большинству заболеваний сердечно-сосудистой системы присущ дисбаланс активности нейрогормонов в сторону преобладания факторов первой группы, что способствует прогрессированию ремоделирования и хронической сердечной недостаточности.
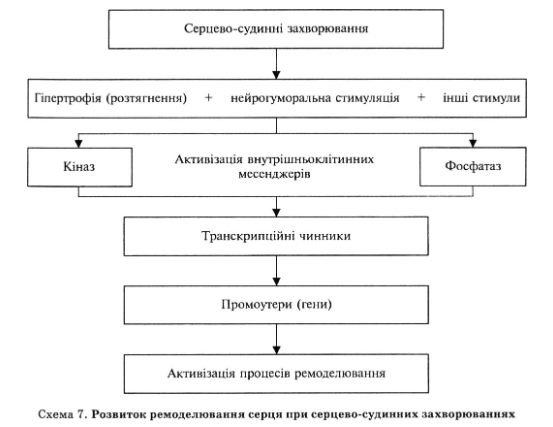
Согласно современным представлениям, различные сердечно-сосудистые заболевания активизируют нейрогормональные системы, вызывают нарушения гемодинамики и некоторые другие факторы (схема 7). В итоге происходит стимуляция внутриклеточных мессенджеров, в частности внутриклеточных ферментных систем (киназы и фосфатазы). Изменения активности внутриклеточных ферментов запускают транскрипционные факторы, влияющие на гены-промоутеры, вследствие чего изменяется экспрессия генов и активизируются процессы ремоделирования сердца.
Выделяют два типа ремоделирования левого желудочка сердца:
1. Концентрический тип, который чаще развивается в случае перегрузки давлением (артериальная гипертензия) и проявляется гипертрофией миокарда левого желудочкабез дилатации его полости. Характеризуется относительно благоприятным течением, длительным сохранением фракции выброса левого желудочка на нормальном уровне, часто наличием асимптоматической диастолической дисфункции.
2. Эксцентричный тип, который развивается в случае перегрузки левого желудочка объемом (пороки сердца с регургитацией, ИБС, дилатационная кардиомиопатия) и проявляется гипертрофией миокарда левого желудочка с дилатацией полости без утолщения стенок левого желудочка. Течение этого типа ремоделирования является менее благоприятным. Он сопровождается снижением фракции выброса по мере прогрессирования расширения полости желудочка.
Переход от концентрического типа ремоделирования до эксцентричного происходит в случае присоединения перегрузки объемом (вероятно, с появлением регургитации на митральном клапане) или увеличение ишемии миокарда.
Классификация хронической сердечной недостаточности
На протяжении многих лет в нашей стране применяли классификацию М.Д. Стражеско и В.Х. Василенко, принятую на XII съезде терапевтов в 1935 г. Она предусматривает выделение острой и хронической недостаточности кровообращения. Острая недостаточность кровообращения включает синдромы острой сердечной, сосудистой, сердечно-сосудистой, левожелудочковой и правожелудочковой недостаточности. Стадии хронической недостаточности кровообращения отображают последовательность ее прогрессирования.
В I стадии симптомы недостаточности кровообращения появляются только во время повышенной физической нагрузки, в покое гемодинамика и функции сердца не нарушены. Во II стадии выделяют два периода. Период А - начало длительной стадии, характеризуется появлением симптомов недостаточности кровообращения во время обычного физической нагрузки. В период Б симптомы отмечаются при незначительной физической нагрузки и в состоянии покоя. Характерны выраженные нарушения функций всех отделов сердца. Работоспособность потеряна. В III стадии нарушения гемодинамики в состоянии покоя резко выражены. Отмечаются необратимые дистрофические изменения всех органов и тканей и стойкие нарушения их функционирования.
Общепринятой является классификация хронической сердечной недостаточности Нью-Йоркской ассоциации сердца (NYHA, 1973), основанный на клиническом оценке наличия и выраженности ограничения функционального состояния больных, то есть их толерантности к повседневной физической нагрузки . Качество жизни больного оценивают по шкале функциональных классов (ФК).
Классификация СН, которая рекомендована ЕТК (2001), базирующийся на классификации М.Д. Стражеско и В.Х. Василенко и NYHA и предусматривает выделение клинических стадий, функциональных классов и вариантов сердечной недостаточности.
Клинические стадии (соответствуют стадиям хронической недостаточности кровообращения по классификации Н.Д. Стражеско и В.Х. Василенко, 1935)
СН I - начальная стадия, одышка при повышенной физической нагрузке, которой раньше не было.
СН НА - клинически выраженная стадия, одышка при умеренной физической нагрузки.
СН II Б - симптомы при незначительной физической нагрузки и в состоянии покоя, потеря трудоспособности.
СН III - конечная стадия поражения сердца с выраженными изменениями гемодинамики и необратимыми структурными изменениями органов.
Функциональные классы (по критериям NYHA, 1973)
ФК И - выполнение обычных физических нагрузок не вызывает одышки, утомляемости и сердцебиение.
ФК II - одышка, утомляемость, сердцебиение появляются во время обычных физических нагрузок, вызывает умеренное ограничение физической активности.
ФК III - в состоянии покоя жалоб нет, но даже при незначительной физической нагрузки возникают одышка, утомляемость и сердцебиение (выраженное ограничение физической активности).
ФК IV - любой уровень физической активности вызывает субъективные симптомы, которые могут возникать также и в состоянии покоя.
Варианты:
- с систолической дисфункцией левого желудочка: фракция выброса левого желудочка 45% и меньше
- с сохраненной систолической функцией левого желудочка: фракция выброса левого желудочка более 45% (больные с первичной диастолической сердечной недостаточностью и клапанными пороками с регургитацией, что вызывает "завышения" фракции выброса левого желудочка).
Стадии хронической сердечной недостаточности отражают этап клинической эволюции этого синдрома, тогда как ФК пациента является динамической характеристикой, которая может меняться в процессе лечения. ФК больного определяют на основании клинических критериев и объективным по данным максимального потребления кислорода при дозированном физической нагрузке во время спировелоергометрии. Определение варианта сердечной недостаточности возможно только при наличии данных эхокардиографического обследования или радиоизотопной или рентгеноконтрастного вентрикулографии.
Клиническая картина . Диагноз хронической сердечной недостаточности основывается на выявлении характерных симптомов этого синдрома при исключении других причин, не связанных с патологией сердца (заболеваний легких, почек, органов кроветворения и эндокринной патологии).
Нарушение систолической функции левого желудочка клинически проявляется симптомами застоя в малом круге кровообращения вследствие венозной легочной гипертензии - одышкой, ортопноэ, сердечной астмой. При нарушении сократимости правого желудочка появляются симптомы застоя в большом круге кровообращения - увеличение печени, асцит, периферические отеки, набухание и пульсация яремных вен.
Одышка как симптом хронической сердечной недостаточности появляется сначала при физической активности, а затем и в состоянии покоя. В положении сидя или лежа с приподнятым изголовьем одышка уменьшается, поскольку при этом венозный кровоток к правым отделам сердца уменьшается. Именно увеличением кровотока в правых отделов сердца можно объяснить развитие приступов сердечной астмы преимущественно ночью. При этом помимо одышки и удушья отмечается сухой или с отделением скудного слизистого мокроты кашель, при аускультации прослушиваются хрипы в нижних отделах легких.
Быстрая утомляемость при физической нагрузке свидетельствует о недостаточном кровоснабжения скелетных мышц, отчасти является следствием выборочной компенсаторной вазоконстрикции, описанной выше.
Сердцебиение является одним из ранних симптомов хронической сердечной недостаточности как попытка организма нормализовать МОС при пониженном ударном объеме сердца вначале при физической нагрузке, а затем и в состоянии покоя.
Периферийные отеки в больных с хронической сердечной недостаточностью сопровождаются другими симптомами задержание жидкости (никтурией, олиго-рию, увеличением массы тела), а их локализация зависит от стадии синдрома. Вначале появляется пастозность стоп и участков косточек конце дня исчезает до утра, постепенно отеки распространяются и могут охватывать все тело (анасарка). Отеки обычно сопровождаются жаждой и значительным потреблением жидкости. Отечный синдром может протекать с гидротораксом, чаще правосторонним, так как больные с хронической сердечной недостаточностью спят преимущественно на правом боку. Гидроторакс может быть признаком венозного застоя как в малом, так и большом круге кровообращения, так как плевральные вены пристеночной плевры относятся к большому кругу, а внутренностный плевры - до малого круга кровообращения.
Увеличение печени при правожелудочковой недостаточности предшествует появлению отеков. Жидкость в брюшной полости (транссудат) появляется вследствие повышенного давления в печеночных венах и венах брюшины.
Согласно Европейскому клинико-эпидемиологического исследования IMPROVEMENT (2000), одышка различной выраженности отмечается в 98,4%, быстрая утомляемость - в 94,3%, сердцебиение - в 80,4 % больных с хронической сердечной недостаточностью. Кашель, ортопноэ, периферические отеки встречаются реже, частота выявления этих симптомов у больных с хронической сердечной недостаточностью не превышает 73%.
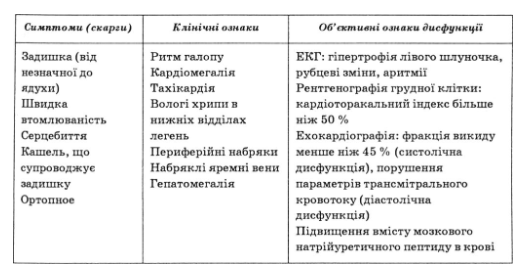
Практически все симптомы хронической сердечной недостаточности встречаются и при других заболеваниях, что обусловливает их низкую специфичность. Диагностическая ценность симптомов повышается в случае сочетания нескольких симптомов. Поэтому в каждом случае диагноз хронической сердечной недостаточности должен быть подтвержден данными объективных методов (табл. 26).
Таблица 26
Критерии диагностики хронической сердечной недостаточности
(Национальные рекомендации по диагностике и лечению хронической сердечной недостаточности, 2003)
Диагностика
При электрокардиографии в 12 отведениях чаще обнаруживают признаки гипертрофии и перегрузки левого желудочка, рубцовые изменения после перенесенного инфаркта миокарда, аритмии, особенно фибрилляцией предсердий. Однако эти изменения неспецифичны. Важнейшее значение имеет нормальная ЭКГ, что свидетельствует об отсутствии хронической сердечной недостаточности с точностью более 90%.
Главными рентгенологическими признаками хронической сердечной недостаточности является увеличение размеров сердца и венозный застой в легких. Увеличение размеров сердца (кардиоторакальной индекс более 50%) характерно для систолической сердечной недостаточности, однако нормальные размеры не исключают диастолической дисфункции. Признаки венозного застоя, интерстициального и альвеолярного отека легких чаще всего свидетельствуют о высоком давлении "заклинивания" легочной артерии и могут отмечаться как при систолической, так и при диастолической дисфункции левого желудочка, однако чувствительность этого признака не превышает 50%.
Эхокардиография позволяет объективизировать наличие дисфункции левого желудочка, уточнить ее характер (систолическая или диастолическая) и выраженность, а также получить важную информацию о характере заболевания сердца как причины хронической сердечной недостаточности и оценить эффективность лечения. Благодаря использованию этого метода можно определить состояние клапанного аппарата (недостаточность, регургитация, стеноз), изменения эндокарда (вегетации) и перикарда (жидкость в полости перикарда), внутриполостные тромбы как очаги тромбоэмболии.
Важнейшим параметром внутрисердечной гемодинамики, определяется при эхокардиографии, является фракция выброса левого желудочка, которую используют для оценки систолической функции левого желудочка. При этом считают, что о наличии систолическомческой дисфункции левого желудочка свидетельствует фракция выброса менее 45%.
С помощью допплеровского исследования трансмитрального кровотока в период диастолы можно получить важную информацию о характере наполнения левого желудочка. Выявление нарушений диастолического наполнения сердца важно не только для определения варианта хронической сердечной недостаточности в каждом конкретном случае. Доказано, что выраженность диастолической дисфункции большей степени, чем систолической, коррелирует с тяжестью течения синдрома, выраженностью снижение толерантности к физической нагрузке и качеству жизни.
Начальная стадия диастолической дисфункции развивается вследствие нарушений активного расслабления миокарда и характеризуется снижением скорости раннего трансмитрального потока (Е), компенсаторным повышением скорости потока в фазе систолы предсердия (А) и снижением соотношения Е /А.
У пациентов с тяжелым поражением сердца может наблюдаться рестриктивный тип наполнения левого желудочка с увеличением скорости Е, укорочением времени замедления пика Е и значительным увеличением соотношения Е /А. Увеличена скорость раннего наполнения левого желудочка (Е) обусловлена увеличением давления в левом предсердии, что приводит к увеличению раннего диастолического трансмитрального градиента давления.
У пациентов с промежуточным между нарушениями расслабления и рестриктивному типу диастолического наполнения левого желудочка соотношения Е /А и время замедления могут не отличаться от нормы ("псевдонормального тип" наполнения левого желудочка). Этот тип отличается от нормального уменьшением пика скорости Е.
Три типа диастолической дисфункции левого желудочка ("нарушение расслабления", "псевдонормального" и "рестриктивной") соответствуют легкой, средней и тяжелой степени диастолической дисфункции.
В табл. 27 представлены основные критерии разграничения систолической и диастолической дисфункции левого желудочка.
Таблица 27
Критерии разграничения систолической и диастолической дисфункции левого желудочка (по Л.Г. Воронковым, 2003, с дополнениями)
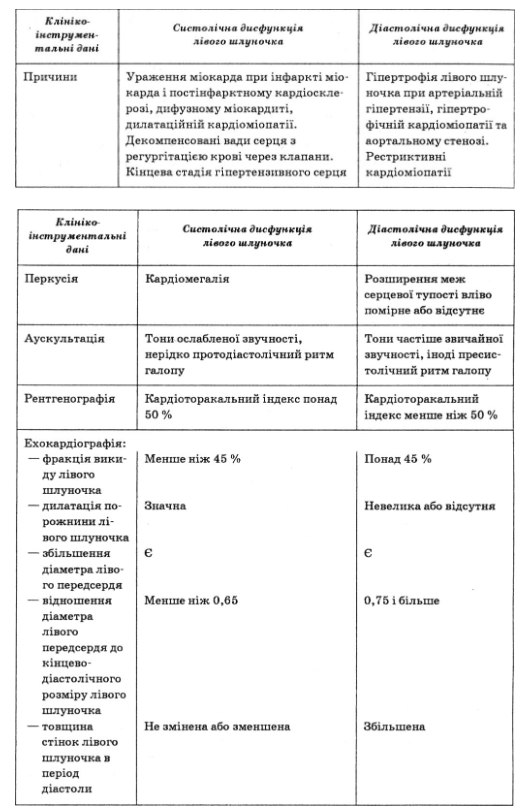
Магнитно-резонансная томография и радиоизотопная ангиография позволяют точнее по сравнению с эхокардиографии, оценить толщину стенок, массу миокарда левого желудочка, объемы камер сердца. Кроме того, благодаря магнитно-резонансной томографии можно определить кровоснабжения миокарда, размеры некроза миокарда или постинфарктного рубца. У больных с хронической сердечной недостаточностью эти методы имеют вспомогательное значение и могут применяться при недостаточной информативности других методик, прежде эхокардиографии.
Нагрузочные тесты на велоэргометре или тредмиле у пациентов с хронической сердечной недостаточностью проводят для оценки их функционального состояния и эффективности лечения. Наиболее информативным показателем для оценки функционального состояния больных с этим синдромом является максимальное потребление кислорода во время физической нагрузки. При хронической сердечной недостаточности наблюдают снижение этого показателя, однако, является неспецифической признаку. Вместе неизмененном максимальное потребление кислорода исключает хронической сердечной недостаточностью. Его величина менее 10 мл кг -1 • мин свидетельствует неблагоприятный прогноз.
В практической деятельности удобно пользоваться заказным NYHA тестом с ходьбой в течение 6 мин с максимально возможной скоростью. Величина пройденного при этом расстояния высоко коррелирует с ФК NYHA и прогнозом больных с хронической сердечной недостаточностью (табл. 28).
Таблица 28
Параметры физической активности при разной выраженности хронической сердечной недостаточности по критериям Нью-Йоркской ассоциации сердца
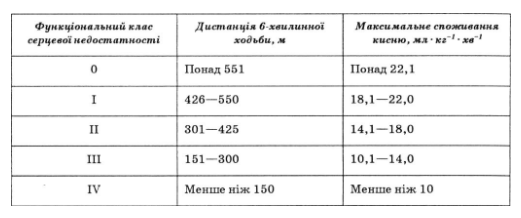
Инвазионные методы исследования применяют для установления причины хронической сердечной недостаточности и оценки прогноза. Коронарную ангиографию следует проводить пациентам с острой сердечной недостаточностью или острой декомпенсацией хронической сердечной недостаточности и пациентам с тяжелой сердечной недостаточностью (шок или острый отек легких), которые плохо реагируют на лечение. Коронаровентрикулография следует проводить пациентам со стенокардией или другими признаками ишемии миокарда при неэффективности соответствующей антиишемической терапии, а также с рефрактерной сердечной недостаточностью неизвестной этиологии.
Мониторирование гемодинамических показателей с помощью катетеризации легочной артерии показано пациентам, которые госпитализированы по поводу кардиогенного шока или не реагируют на начатую терапию.
натрийуретического пептида . На сегодня известны 4 вида натрийуретических пептидов. Предсердный натрийуретический пептид был открыт в 1981 p., А в 1988 г. из мозговой ткани свиньи был выделен так называемый мозговой натрийуретический пептид. Впоследствии было доказано, что главным источником мозгового натрийуретического пептида является кардиомиоциты желудочковсердца. Его выделение в кровь повышается в случае усиления миокардиального стресса. Источником третьей натрийуретического пептида (С-натрийуретический пептид) является эндотелиальные клетки. Четвертый тип (Д-тип) натрийуретического пептида был выделен из яда змеи Green Mamba.
Сейчас определения содержания мозгового натрийуретического пептида в крови для уточнения диагноза хронической сердечной недостаточности содержится во всех международных рекомендациях. Его чувствительность станобить 97%, специфичность 84% и прогностическая ценность 70%, что позволяет рекомендовать определение концентрации мозгового натрийуретического пептида как лабораторный критерий хронической сердечной недостаточности.
В Рекомендации ЕТК (2001) определение мозгового натрийуретического пептида при подозрении на хроническую сердечную недостаточность (например, у больных с одышкой) рассматривается как первый этап диагностики, и в случае его повышения (более 100 пг /мл) рекомендуется дальнейшее обследование больного, включая проведение эхокардиографии. Если содержание пептида меньше указанной величины, рекомендуется искать другие причины одышки и другие симптомы хронической сердечной недостаточности - анемию, дыхательную недостаточность, прежде вследствие хронических обструктивных заболеваний легких, ожирение, почечная недостаточность, венозную недостаточность.
Обследование больных с подозрением на хроническую сердечную недостаточность и в случае установления этого диагноза должны включать проведение таких лабораторных исследований: общий анализ крови и мочи, определение уровня креатинина и глюкозы, печеночных ферментов, концентрации электролитов плазмы.
Анемия, что проявляется одышкой и быстрой утомляемостью, часто является спутником хронической сердечной недостаточности (в 14-79% больных). Ее возникновение при хронической сердечной недостаточности связывают с характерным для этого синдрома хроническим неспецифическим иммунным воспалением и, возможно, вторичным гастритом. Снижение гемоглобина до показателей менее 110 г /л свидетельствует о тяжелом течении хронической сердечной недостаточности и повышение риска смерти. Анемия при хронической сердечной недостаточности обычно нор-моцитна, чаще ее обнаруживают у пациентов с хронической сердечной недостаточностью III-IV ФК (NYHA), у женщин, а также у больных с запущенной хронической сердечной недостаточностью (более 7 лет).
Во время лабораторного исследования могут определяться признаки гепато-цитолиза (повышение активности аланиновои и аспарагиновой трансаминаз) и печеночно-клеточной недостаточности (повышение содержания фракций билирубина, снижение альбумина и протромбинового индекса), обусловленные некрозом гепатоцитов в условиях нарушения кровообращения и гипоксии печени.
Увеличение объема циркулирующей крови, употребление мочегонных средств и ограничение соли у больных с хронической сердечной недостаточностью могут вызвать гипокалиемию и гипонатриемии.
В ходе исследования мочи можно выявить изменения, характерные для "застойной" почки (высокая плотность, различной выраженности протеинурия при скудном мочевом осадке). Снижение почечного кровотока через периферийный спазм в условиях выраженной нейрогуморальной активации может приводить к транзиторного, а при резко выраженной хронической сердечной недостаточности - устойчивого повышение креатинина в крови, считают неблагоприятным прогностическим признаком. Для точного оценки состояния почек у больных с хронической сердечной недостаточностью рекомендуется рассчитывать КК по следующим формулам:
Осложнения хронической сердечной недостаточности
Осложнения вследствие поражения органов дыхания. У больных с хронической сердечной недостаточностью вследствие тесной анатомической и функциональной взаимосвязи между системами кровообращения и дыхания часто наблюдаются сочетанные изменения в этих системах, которые коррелируют с тяжестью и выраженностью легочной гипертензии. Изменения функционального состояния аппарата внешнего дыхания возникают сравнительно рано, часто до появления симптомов хронической сердечной недостаточности, сначала носят компенсаторный характер и направлены на поддержание нормального газового состава крови. В дальнейшем присоединяются структурные изменения легочной ткани, увеличиваются нарушения функционального состояния аппарата внешнего дыхания, развиваются расстройства газового состава артериальной крови.
Снижение максимальной вентиляции легких, ЖЕЛ, неравномерность вентиляции при хронической сердечной недостаточности, вкладываемых в синдром рестриктивной дыхательной недостаточности, обусловленные повышением сопротивления бронхов и снижением растяжимости легких. Увеличение эластичного и неэластичного сопротивления способствует повышению внутригрудного давления, ухудшения условий гемодинамики в малом круге кровообращения и нарастанию работы дыхания, повышает потребность тканей в кислороде, увеличивает гипервентиляцию и приводит к нарушению диффузии газов.
Нарушение вентиляции легких в сочетании с нарушениями гемодинамики в малом круге кровообращения, посткапиллярных легочной гипертензией, застоем и транссудацией жидкой части плазмы крови в ячейки создают благоприятные условия для инфекции и развитию застойной пневмонии.

Характерное для больных с хронической сердечной недостаточностью кровохарканье обусловлено диапедезаили разрывом расширенных легочных и бронхов капилляров. Изредка в случае разрыва мелких бронхов вен может возникнуть легочное кровотечение. Есть относительно ранним осложнением левосторонней сердечной недостаточности. Наблюдается у больных с сердечной астмой, отеком легких, может быть обусловлена тромбоэмболией ветвей легочной артерии.
Следует помнить, что нарушение функции внешнего дыхания не специфичны. Они характерны и для бронхолегочных заболеваний, анемий, тиреотоксикозе.
Нарушения сердечного ритма и внезапная сердечная смерть. Частота внезапной сердечной смерти среди причин летальных исходов больных с застойной сердечной недостаточностью колеблется от 45 до 90%. Главными и независимыми факторами риска внезапной сердечной смерти при хронической сердечной недостаточности является выраженная дисфункция миокарда (фракция выброса левого желудочка менее 45%) и сложные желудочковые аритмии, в том числе бессимптомные.
Дисфункция желудочков, что случается при хронической сердечной недостаточности, с нарушениями регионарного и общего растяжения миокарда, увеличением напряжения стенки приводит к укорочению потенциала действия и эффективного рефрактерного периода, а также деполяризации мембраны в начале диастолы, что может быть триггером и вызвать внеочередной потенциал действия (феномен механико-электрического обратной связи). Гетерогенность напряжение стенки в различных участках желудочка с его дисфункции увеличивает дисперсию де-и реполяризации миокарда и его аритмичную готовность. Изменении электрофизиологических свойств миокарда и их неоднородности способствует также ишемия миокарда.
Существенную роль в аритмогенези играют нейрогуморальные факторы, как прямо влияя на электрофизиологические свойства мембраны кардиомиоцитов, так и косвенно - за счет вторичной гипокалиемии, увеличение объема внутрисосудистой жидкости, пре-и постнагрузки и потребности миокарда в кислороде.
На возникновение аритмий существенно влияют препараты, применяемые для лечения сердечной недостаточности, вследствие выделения почками калия и магния (салуретики) или повышение автоматизма и возбудимости миокарда желудочков (инотропные агенты). Имеются данные об увеличении частоты и тяжести желудочковых аритмий на фоне лечения р-адренорецепторов, ингибиторами фосфодиэстеразы, производными дигидропиридина т.д..
Для возникновения предсердных аритмий, среди которых самая распространенная фибрилляция предсердий, важное значение имеют также дилатация полости сердца, гипоксия и ацидоз.
Осложнения вследствие поражения печени при хронической сердечной недостаточности развиваются часто. Механизмами, приводящими к поражению печени, являются:
1. Венозный застой в печени. Рост венозного давления приводит к атрофии гепатоцитов. Застойные изменения в синусоидах вследствие передачи венозного давления из печеночных венул вызывают перисинусоидальных отек, нарушающий оксигенацию и поступление питательных веществ в гепатоциты. Впоследствии развиваются фиброзные изменения, которые неодинаково выражены в различных участках печени.
2. Гипоксия клеток печени, что обусловлено сниженным сердечным выбросом, с компенсаторной повышенной экскрецией кислорода в ацинусах.
3. Артериальная гипоксемия, значение которой в поражении печени при хронической сердечной недостаточности, вероятно, меньше, чем при хронической обструктивной болезни легких.
Поражение печени при хронической сердечной недостаточности связывают с активизацией печеночных макрофагов (клеток Купффера), которые в ответ на ишемию продуцируют провоспалительные цитокины, в частности фактор некроза опухолей а, индуцирует повреждение печени усилением экспрессии клеточных молекул адгезии и хемокинов. Это приводит к миграции и активизации полиморфно-ядерных лейкоцитов с выделением протеаз, которые повреждают гепатоциты.
Поражение печени при хронической сердечной недостаточности может проявляться застойной Гепатопатии, ишемическим гепатитом и кардиального фиброзом и циррозом печени.
Застойная гепатопатия развивается преимущественно через венозный застой вследствие снижения сердечного выброса. Клинически проявляется гепато (Сплен) мегалиею, асцит наблюдается у 25% таких пациентов. Характерно повышение активности АсАТ и АлАТ (трехразовое), умеренная гипербилиру-бинемия и гипоальбуминемия.
Ишемический гепатит , впервые описан в 1979 г. как поражение печени, вроде вирусного гепатита, в случае быстрого прогрессирования снижает параметры насосной функции левого желудочка (инфаркт миокарда, аритмии, тромбоэмболии ветвей легочной артерии). Клинически ишемический гепатит проявляется симптомами правожелудочковой недостаточности в сочетании с диспепсическим синдромом (тошнотой, рвотой, анорексией), болью в подложечной области, энцефалопатией. Характерные признаки выраженного цитолиза (повышение активности трансаминаз более чем в 10 раз), функциональные нарушения печени (повышение уровня билирубина, азота мочевины, увеличение протромбинового времени и увеличение МНО), функционального состояния почек (повышение уровня креатинина в крови, гиперкалиемия, снижение натрия в моче при нормальном мочевого осадка). Диагноз ишемического гепатита устанавливают на основании розвиткуьминущои высокой гиперферментемии, удлинение протромбинового времени и нарушения функции почек у лиц снизкой фракцией выброса левого желудочка.
Для ишемического гепатита характерен доброкачественное течение, хотя внут-ришньоликарняна смертность составляет 50%. Прогноз определяется не степенью печеночной дисфункции, а тяжестью основного заболевания. Если состояние гемодинамики стабилизируется, то печеночные ферменты нормализуются через 1-2 нед, билирубин - чуть позже.
Кардиальный фиброз и цирроз печени являются поздними стадиями застойных изменений в печени. Морфологические изменения вариабельны: от минимальных депозитов коллагена в синусоидах до широких септ и формированию цирроза. Фиброзные септы распространяются вглубь частицы радиально от центральной вены, могут соединяться с другими центральными венами, что приводит к характерной для кардиального цирроза картины "обратной дольчатого строения". Выраженность фиброза в печени и тяжесть цирроза не коррелируют с функциональным классом хронической сердечной недостаточности и продолжительностью эпизодов декомпенсации. Симптомы кардиального цирроза обычно замаскированы клиническими проявлениями правожелудочковой недостаточности.
У большинства больных с кардиальным печени показатели в норме или тождественны с таковыми при застойной гепатопатии. Несмотря на то, что у значительного количества пациентов выявляют расширенные вены пищевода, кровотечения бывают крайне редко. Выраженность асцита может не соответствовать степени периферийных отеков и клинических проявлений хронической сердечной недостаточности, для асцитической жидкости характерен высокий уровень ЛДГ сравнению с выпотом при вирусных и алкогольных циррозах печени.
Наличие поражения печени у больного с хронической сердечной недостаточностью зачастую не ухудшает прогноз, поэтому не требует применения специфического лечения. Однако антикоагулянты таким больным следует назначать с осторожностью в связи с повышенным риском кровотечения.
Осложнения вследствие стаза крови . При атеросклерозе, является основой большинства заболеваний, которые приводят к хронической сердечной недостаточности, создаются условия для возникновения тромботического процесса в различных сосудистых бассейнах. С другой стороны, присоединение хронической сердечной недостаточности до основного заболевания также усугубляет нарушения свертывающей системы крови. По данным фундаментальных исследований А.И. Грицюка, для хронической сердечной недостаточности характерно прогрессивное усиление патогенетических факторов тромбообразования (замедление кровотока, глубокие изменения сосудистой стенки) на фоне умеренных нарушений гемокоагуляции в сторону гиперкоагуляции крови (однако возможна и небольшая гипокоагуляция), но в условиях угнетения фибринолиза. Такие нарушения усиливают опасность внутрисосудистого тромбоза, особенно при наличии соответствующих факторов (постельный режим, нарушения сердечного ритма, варикозное расширение вен нижних конечностей и др.). Тромбы образуются в венах нижних конечностей и расширенных полостях сердца, являются очагами эмболии и инфаркта легкого и внутренних органов.
Сердечная кахексия. Потеря массы тела, иногда значительная, наблюдается у больных с запущенной сердечной недостаточностью и обусловлена:
а) анорексией вследствие венозного застоя в печени и других органах пищеварения
б) нарушением всасывания жиров
в) повышением обмена веществ вследствие значительного увеличения работы дыхательных мышц.
Лечение
Целью лечения больных с сердечной недостаточностью (ЕТК, 2005; УАК, 2006)
1. Профилактика - первичная цель:
- профилактика и /или лечения заболеваний, которые могут привести к дисфункции левого желудочка и хронической сердечной недостаточности
- профилактика развития хронической сердечной недостаточности в случае выявления сердечной дисфункции.
2. Поддержание и улучшение качества жизни.
3. Улучшение выживания.
Профилактика хронической сердечной недостаточности. Развитие дисфункции желудочков сердца и хронической сердечной недостаточности можно затормозить, излечивая состояния, которые могут к ним привести, прежде АГ и /или ИБС. При наличии дисфункции миокарда, если это возможно, первичной целью является ликвидация причин, которые к ней привели (ишемия, токсические агенты, алкоголь, лекарственные препараты, заболевания щитовидной железы). Если эти причины невозможно ликвидировать, лечение должно быть направлено на замедление или профилактику развития дисфункции левого желудочка, что повышает риск внезапной смерти и развитие хронической сердечной недостаточности.
Общие меры в лечении хронической сердечной недостаточности включают:
1. Лечение основного заболевания и коррекцию факторов риска:
- вторичную профилактику ИБС и решения вопроса о реваскуляры-цию миокарда
- нормализацию и контроль повышенного AT
- хирургическую коррекцию пороков сердца
- диетическую и медикаментозную коррекцию гипер (дис) липопротеидемий
- коррекцию гипергликемии при сахарном диабете
- фармакологической или хирургическую коррекцию тахиаритмий (брадиаритмий)
- отказова от табакокурения и употребления алкоголя
- снижение массы тела при ожирении.
2. Ограничение суточного потребления поваренной соли менее 3 г в сутки при сердечной недостаточности I-II ФК, менее 1,5 г в сутки при сердечной недостаточности III-IV ФК.
3. Регулярная физическая активность: "комфортный", но регулярный двигательный режим.
4. Ограничение количества употребления жидкости при симптомах его задержания до 1 - 1,5 л.
В Европейских рекомендациях по лечению больных с хронической сердечной недостаточностью выделены препараты, которых следует избегать (или назначать осторожно) больным с хронической сердечной недостаточностью:
1) нестероидные противовоспалительные препараты и коксибы
2) антиаритмические препараты 1-го класса
3) антагонисты кальциевых каналов (дилтиазем, верапамил и производные дигид-ропиридонив короткого действия)
4) трицикличные антидепрессанты
5) глюкокортикостероиды
6) препараты лития.
Медикаментозное лечение хронической сердечной недостаточности должно проводиться всю жизнь и предусматривает использование препаратов с доказанной эффективностью по уменьшению симптомов и /или повышение выживаемости и безопасности. К этим препаратам относятся:
1. Ингибиторы АПФ, которые следует назначать всем больным с хронической сердечной недостаточностью, независимо от этиологии, стадии процесса и наличия или отсутствия декомпенсации сердечной деятельности. В случае непереносимости вместо них назначают блокаторы рецепторов ангиотензина II. Многочисленные исследования с плацебо-контролем доказали положительное влияние обеих групп препаратов на выживаемость больных с хронической сердечной недостаточностью и систолической дисфункцией.
2. (С-адреноблокаторы, которые в дополнение к терапии ингибиторами АПФ также следует назначать всем больным с ХСН, не имеющих противопоказаний к такому лечению. Как и ингибиторы АПФ, они влияют на выживаемость больных с систолической дисфункцией, а также, возможно, и с диастолической сердечной недостаточностью
3. Диуретики, которые показаны больным с задержанием натрия и воды в организме, их влияние на выживаемость не изучался.
4. Дигоксин в малых дозах и с осторожностью больным с синусовым ритмом. Включение его к лечению больных с хронической сердечной недостаточностью дополнительно к ингибиторам АПФ и диуретиков не влияет на выживаемость, но снижает частоту госпитализаций в связи с декомпенсацией сердечной недостаточности.
5. Антагонист рецепторов к альдостерона (альдактон). В случае назначения в малых дозах с ингибиторами АПФ больным с хронической сердечной недостаточностью высоких функциональных классов с систолической дисфункцией левого желудочка улучшает выживаемость.
Ингибиторы АПФ относятся к препаратам первой линии в лечении больных с хронической сердечной недостаточностью. их применение способствует уменьшению числа госпитализаций и риска смерти больных с систолической дисфункцией левого желудочка (как бессимптомной, так и с хронической сердечной недостаточностью) на 20-25%. В Европейских рекомендациях по лечению больных с хронической сердечной недостаточностью (2001) было указано, что неназначение ингибиторов АПФ больным с систолической дисфункцией левого желудочка не может считаться оправданным в коем случае и приводит к сознательному повышению риска смерти больных. В Европейских рекомендациях 2005 г. для лечения больных с хронической сердечной недостаточностью рекомендуется применять только 5 препаратов этой группы, эффективность и безопасность которых доказана в крупных многоцентровых исследованиях.
Ингибиторы АПФ влияют на баланс нейрогормонов, уменьшая образование ангиотензина II и, как следствие, катехоламинов и эндотелина, увеличивая содержание брадикинина благодаря блокаде его распада.
Терапию ингибиторами АПФ следует начинать с малых доз, постепенно повышая их (титруемой) до максимальных и, желательно, целевых, эффективность по выживанию доказана в многоцентровых исследованиях (табл. 29).
Ингибиторы АПФ, которые часто применяют в Украине для лечения больных с хронической сердечной недостаточностью (дозы, частота употребления)
Возможными побочными эффектами ингибиторов АПФ является выраженная артериальная гипотензия, гиперкалиемия, повышение уровня креатинина (часто преходящая) и сухой кашель в 1-3% случаев через повышение содержания брадикинина, не сопровождается морфологическими изменениями в легких. Противопоказаны препараты при двустороннем стенозе почечных артерий и ангионевротический отек.
Контроль за лечением (измерение AT, контроль за функциональным состоянием почек и содержанием электролитов в крови) следует проводить через 1-2 нед после каждого повышения дозы.
$-адреноблокаторы долгое время считали противопоказаны в лечении больных с хронической сердечной недостаточностью, связывали с их отрицательным инотропным действием. Однако к середине 1990-х годов была доказана эффективность и безопасность трех препаратов этой группы: карведилола, Бисопролом-лу и метопролола-сукцината длительного действия (CR), которые в многоцентровых исследованиях доказали способность снижать риск смерти больных с хроническойсердечной недостаточностью и систолической дисфункцией левого желудочка на 34 - 35%. Данных по эффективности при хронической сердечной недостаточности других 3-адреноблокаторов, в том числе атенолола и метопролола короткого действия (IR), нет. В 2005 г. перечень рекомендованных для лечения хронической сердечной недостаточности Р-адреноблокаторов был дополнен еще одним препаратом - небивололом, который, по данным контролируемого исследования, влияет на прогноз пациентов с хронической сердечной недостаточностью старше 70 лет.
Доказано двухфазность влияния Р-адреноблокаторов на миокард больных с хронической сердечной недостаточностью:
1) снижение фракции выброса в первые 2 нед лечения
2) последующее увеличение фракции выброса и толерантности к физической нагрузке по данным велоэргометры и тредмил-теста, что связано с уменьшением тахикардии, потребление миокардом кислорода и восстановлением сократимости кардиомиоцитов, находившихся в состоянии оборотной ишемической дисфункции.
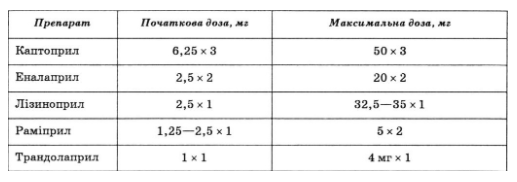
Р-адреноблокаторы следует назначать всем больным с хронической сердечной недостаточностью, не имеющие противопоказаний, дополнительно к терапии ингибиторами АПФ после стабилизации состояния. Лечение начинают с начальной дозы (обычно 1/8 терапевтической), дозу увеличивают через 2 нед и даже реже, до достижения целевой терапевтической (табл. 30).
Таблица 30
Р-адреноблокаторы, применяемые для лечения больных с хронической сердечной недостаточностью (дозы, частота употребления)
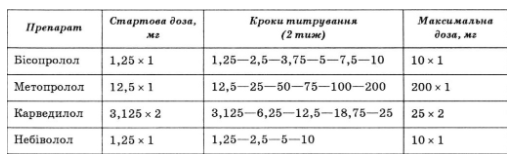
Р-адреноблокаторы противопоказаны больным с бронхиальной астмой, ЧСС менее 55 в 1 мин, систолическом AT 85 мм рт. ст. и ниже, атриовентры-кулярный блокадах высокой степени (если не имплантирован искусственный водитель ритма), тяжелых облитерацийних заболеваниях артерий нижних конечностей с симптомами ишемии в состоянии покоя.
Во время проведения терапии р-адреноблокаторами необходим контроль уровня AT и ЧСС, симптомами хронической сердечной недостаточности, признаками задержание жидкости. В случае нарастания симптомов хронической сердечной недостаточности прежде всего следует увеличить дозу диуретиков и ингибиторов АПФ, и только при неэффективности такой тактики - временно снизить дозу р-адренорецепторов. При развитии артериальной гипотензии, прежде симптоматической, рекомендуется уменьшить дозу вазодилататора, и только если это не дает эффекта - временно снизить дозу Р-адренорецепторов. При развитии брадикардии (ЧСС менее 55 в 1 мин) нужно временно уменьшить дозу р-адренорецепторов.
диуретики назначают больным с хронической сердечной недостаточностью, у которых имеются признаки задержание жидкости в организме (отеки, одышка с застойными хрипами в легких, увеличение массы тела). Препараты этой группы существенно уменьшают симптомы хронической сердечной недостаточности, но не замедляют ее прогрессирование и не улучшают прогноза, что связано с их способностью активизировать ренин-ангиотензиновую и симпатико-адреналовой системы в ответ на снижение объема циркулирующей плазмы крови. Поэтому их рекомендуют назначать только вместе с препаратами, снижающими нейрогуморальную активизацию - ингибиторами АПФ и /или Р-адреноблокаторами.
При хронической сердечной недостаточности предпочтение следует отдавать петлевые-ным диуретикам (фуросемид, торасемид, этакриновая кислота), хотя больным с умеренными нарушениями гемодинамики Европейское общество кардиологов предлагает мочегонным терапию начинать с применения более слабых препаратов - тиазидных диуретиков. Калийзберигальни диуретики (триамтерен, амилорид и спиронолактон) используют только при наличии гипокалиемии после назначения ингибиторов АПФ и диуретиков.
Лечение обычно начинают с малых доз, в дальнейшем подбирая дозу для достижения желаемого эффекта: гидрохлоротиазида 25 мг (максимально 100 мг), фуросемида 20-40 мг (максимально до 500 мг), торасемида 10-20 мг (максимально до 100 мг) в сутки. Препараты обычно назначают утром натощак.
Больным с рефрактерными отеками рекомендуется:
1. Применение петлевых диуретиков в сочетании с тиазидными и калий-сберегательные (лучше спиронолактон) для так называемой последовательной блокады реабсорбции натрия в нефроне. Сочетание двух петлевых диуретиков не усиливает эффекта и поэтому нецелесообразно.
2. Введение петлевых диуретиков, обычно струйное.
3. При наличии гипопротеинемии (гипоальбуминемии) ее корректируют инфузией альбумина.
4. Длительное (в течение нескольких суток) введение допамина в диуретических дозах (1-5 мкг? Кг -1 • мин -1 ).
5. Изолированная ультрафильтрация крови (если сохранен сердечный выброс и отсутствуют АГ и стенозы клапанов).
При гидроторакс и асците, резистентных к медикаментозной терапии, показана эвакуация жидкости.
Оценка эффективности и коррекцию дозы диуретиков проводят на основании регулярного определения массы тела (в период активной диуретической т?? Рапии - ежедневно, в поддерживающий период - 1-2 раза в неделю).
Сердечные гликозиды . Единственным сердечными гликозидами, эффективность и безопасность которого доказана, является дигоксин. Именно этот препарат рекомендован для лечения больных с хронической сердечной недостаточностью и систолической дисфункцией левого желудочка. Результаты плацебо-контролируемых многоцентровых исследований свидетельствуют, что длительное употребление дигоксина в сочетании с ингибиторами АПФ и диуретиком существенно не влияют на показатели выживаемости больных с хронической сердечной недостаточностью, однако снижают частоту декомпенсации и случаев госпитализации.
При синусовом ритме дигоксин применяют в малых дозах (0,25 - 0,375 мг), которые способствуют снижению активности симпатико-адреналовой системы, без предварительной дигитализации. Высокие дозы оказывают негативное влияние на прогноз больных с хронической сердечной недостаточностью. У больных с почечной недостаточностью и лиц пожилого возраста доза должна быть уменьшена до 0,0625-0,125 мг. При выраженной ХПН возможна замена дигоксина на дигитоксин, который выводится преимущественно с желчью.
При фибрилляции предсердий дигоксин является средством первой линии благодаря его способности замедлять атриовентрикулярного проведения и снижать ЧСС. При наличии синусового ритма этот препарат показан больным с систолической дисфункцией левого желудочка в случае недостаточной эффективности ингибиторов АПФ, (и-адреноблокаторов и диуретиков при частых декомпенсация сердечно-сосудистой деятельности и госпитализациях.
Антагонисты альдостерона (спиронолактон, эплеренон). Последнее время описан феномен "ускользания" ренин-ангиотензиновой системы из-под контроля ингибиторами АПФ или антагонисты рецепторов ангиотензина II, состоит в восстановлении повышенного уровня альдостерона на фоне применения этих препаратов. Полная длительная (так называемая твердая) блокада ренин-ангиотензин-аль-достероновои системы возможна лишь в случае сочетания ингибиторов АПФ или антагонистов рецепторов ангиотензина II с антагонистами альдостерона. Установлено также самостоятельную антипролиферативное и антиапоптичну действие антагонистов альдостерона.
Доказано, что комбинация ингибиторов АПФ с малыми дозами спиронолак-тона (25-50 мг в сутки) достоверно снижает общую смертность (на 7%), смертность вследствие прогрессирования хронической сердечной недостаточности ( на 28%), внезапную смерть (на 26%) и количество госпитализаций в связи с декомпенсацией хронической сердечной недостаточности (на 30%).
Возможными побочными эффектами спиронолактона является гиперкалиемия, нарастание уровня креатинина, а также развитие гинекомастии (в 10% случаев), нарушения менструального цикла (в 2% случаев), что связывают с неселективнистю действия препарата на рецепторы альдостерона. Хотя доказано, что сочетанное применение малых доз спиронолактона (25 мг в сутки) с ингибиторами АПФ практически не вызывает увеличения уровня калия в плазме крови, этот показатель все же следует контролировать во время лечения.
Рекомендации по назначению этих препаратов у больных с хронической сердечной недостаточностью включают (ЕТК, 2005)
1. Тяжелой хронической сердечной недостаточностью, несмотря на терапию ингибиторами АПФ и диуретиками.
2. Уровень калия в сыворотке крови менее 5 ммоль /л и креатинина менее 250 ммоль /л.
3. Применять малые дозы (спиронолактона 25 мг эплеренона 25 мг).
4. Контролировать уровень калия и креатинина через 4-6 дней.
5. Прекратить употребление, когда уровень калия составит более 5,5 ммоль /л.
6. Если симптомы сердечной недостаточности продолжаются в течение 1 мес и уровень калия в норме, следует увеличить дозу до 50 мг в сутки и повторно определить уровень калия и креатинина через 1 нед.
Дополнительные средства в лечении хронической сердечной недостаточности. К ним относятся антагонисты рецепторов ангиотензина II, периферийные вазодилататоры, амиодарон, Негликозидные инотропные средства, антикоагулянты и анти-тромботические средства.
Антагонисты рецепторов к ангиотензину II первого типа рекомендованы для лечения больных с хронической сердечной недостаточностью при непере-носимости ингибиторов АПФ. Прямые и косвенные сравнительные исследования показали одинаковую клиническую эффективность блокаторов рецепторов ангиотензина II и ингибиторов АПФ по повышению выживания и снижение частоты декомпенсации сердечно-сосудистой деятельности у больных с хронической сердечной недостаточностью и систолической дисфункцией при использовании их целевых доз. На сегодня рекомендованы к применению только два препарата этой группы - вальсартан (80-160 мг в сутки) и кандесартана цилексетил (32 мг в сутки).
Положительное влияние периферических вазодилататоров кроме амлодипина и фе-лодипину на прогноз, количество госпитализаций и прогрессирования хронической сердечной недостаточности не доказан. При этом настораживает их способность вызывать более или менее выраженную рефлекторную активизацию симпатико-адреналовой системы в ответ на вазодилатацию, которые может негативно сказаться на прогнозе. Препаратами этой группы, безопасность назначение которых в дополнение к препаратам первой линии доказано в многоцентровых исследованиях, является амлодипин и фелодипин. Применять препараты этой группы вар?? В только при наличии прямых показаний (стенокардия, артериальная гипертензия). Следует учитывать, что использование периферических вазодилататоров может ухудшить переносимость препаратов первой линии (ингибиторов АПФ и Р-адреноблокаторов) из-за их способности снижать AT.
блокаторы кальциевых каналов, замедляющие ЧСС (верапамил и дилтиазем) могут использоваться у больных с начальной хронической сердечной недостаточностью вследствие диастолической дисфункции левого желудочка, однако их способность влиять на ход и последствия хронической сердечной недостаточности в таких случаях не установлено. У больных с систолической дисфункцией левого желудочка их назначение ухудшает клиническое течение хронической сердечной недостаточности. Дигидропиридины короткого действия при хронической сердечной недостаточности противопоказаны.
Антиаритмическое терапия и профилактика внезапной смерти
При хронической сердечной недостаточности лечение нуждаются лишь опасные для жизни и симптоматические желудочковые нарушения ритма сердца. Препаратами выбора в этом случае является Р-адреноблокаторы, а при их неэффективности - амиодарон в малых поддерживающих дозах (100-200 мг в сутки) или комбинация этих препаратов. их применение снижает риск внезапной сердечной смерти больных с хронической сердечной недостаточностью, даже при отсутствии симптоматических желудочковых аритмий. Все другие антиаритмические препараты у больных с хронической сердечной недостаточностью противопоказаны из-за установленной способностью снижать выживаемость как следствие Проаритмические эффекта. У больных, перенесших симптоматическую желудочковую тахикардию или внезапную остановку кровообращения, единственным эффективным методом лечения, что обеспечивает повышение выживаемости, является профилактическая имплантация автоматического кардиовертера-дефибриллятора. Обычно одновременно назначают поддерживающую дозу амиодарона.
Убедительных данных о целесообразности применения антиагрегантов для лечения больных с хронической сердечной недостаточностью нет. Для предотвращения тромбоза периферических венах и тромбоэмболии ветвей легочной артерии у больных с хронической сердечной недостаточностью и выраженным венозным застоем, особенно тех, кто находится на постельном режиме, эффективным является лечение профилактическими дозами НМГ (эноксапарина 1 мг /кг), а при наличии хронического тромбофлебита и /или перенесенного эпизода тромбоэмболии ветвей легочной артерии - постоянное употребление непрямых антикоагулянтов под контролем МНО 2-3 ед. Для профилактики тромбообразования в предсердиях и тромбоэмболии у больных с хронической сердечной недостаточностью и постоянной формой фибрилляции предсердий, особенно при тромбоэмболиях в анамнезе и митральном стенозе, показаны антикоагулянты (МНО 2-3 ед). Назначение ацетилсалициловой кислоты пациентам с частыми госпитализации по поводу хронической сердечной недостаточности следует избегать из-за риска увеличения симптомов этого синдрома.
Длительное применение Негликозидные инотропных препаратов (Р-адрено-стимуляторов и ингибиторов фосфодиэстеразы) повышает риск смерти больных с хронической сердечной недостаточностью, вероятно, вследствие нейрогуморальной активизации. Поэтому эти препараты применяют исключительно для кратковременного (в течение 2-5 суток) инотропного поддержания в период декомпенсации (добутамина 2-5 мкг • кг " 1 ? Мин" 1 ).
Лечение больных с сохраненной фракцией выброса левого желудочка (диастем-Лично дисфункцией) должно включать вышеперечисленные ингибиторы АПФ и P-адреноблокаторы. Диуретики следует назначать с осторожностью из-за вероятности чрезмерного уменьшения преднагрузки. В Европейских рекомендациях 2005 г. для лечения этой категории больных предложено использовать антагонист рецепторов ангиотензина II кандесартан (32 мг в сутки).
Хирургические методы улучшение насосной функции сердца
Хирургическая реваскуляризация миокарда у больных с ИБС и ХСН позволяет повысить фракцию выброса левого желудочка в среднем на 19% и уменьшить его диаметр на 14%. Метод обычно эффективен при наличии жизнеспособного миокарда. Миокард больных с хронической сердечной недостаточностью в условиях гипоперфузии часто содержит "спящие", или гибернувальни, кардиомиоциты, сократимость которых снижена, поэтому они потребляют минимум кислорода. Успешная реваскуляризация может полностью восстановить их сократимость. Однако у больных с крупными очагами диффузного или очагового кардиосклероза такое лечение может оказаться неэффективным. Консультация кардиохирурга для решения вопроса о целесообразности реваскуляризации миокарда показана всем больным с хронической сердечной недостаточностью ишемического генеза.
Трансплантация сердца впервые была осуществлена в 1967 г. К. Барнардом. Сейчас в США проводится более 2,5 тысячи таких операций в год. Средняя продолжительность жизни больных, перенесших операцию трансплантации сердца, составляет 9,1 года, что значительно превышает результаты медикаментозного лечения. Широкое внедрение такой терапии существенно ограничивают проблемы донорства, высокая стоимость и побочные эффекты сопроводительной иммуносупрессивной терапии, необходимость частых повторных эндомиокардиальный биопсий, болезнь коронарных сосудов пересаженного сердца. В последнее время обсуждается нецелесообразности массового применения трансплантации сердца и перспективность этого метода рассматривается как сомнительноеа.
Перспективные хирургические методы лечения хронической сердечной недостаточности. Одним из наиболее изученных и перспективных методов хирургического лечения больных с хронической сердечной недостаточностью метод вспомогательного кровообращения, или "искусственный левый желудочек". Метод имеет доказанную эффективность, что дало основание Обществу кардиологов России рекомендовать длительную (на несколько месяцев) имплантацию искусственного левого желудочка как альтернативу трансплантации сердца для лечения больных с критическими нарушениями гемодинамики вследствие хронической сердечной недостаточности. Результаты контролируемого исследования по имплантации искусственного левого желудочка свидетельствуют, что такое лечение способствует снижению риска смерти больных с хронической сердечной недостаточностью на 48% в течение 2 лет.
Эффективность хирургического ограничения ремоделирования левого желудочка через удаление части стенки для уменьшения размеров полости и снижение миокардиального стресса (операции Батиста и аневризмектомии). Эти методы не имеют самостоятельного значения в лечении хронической сердечной недостаточности и могут рассматриваться как "мостики" к трансплантации сердца.
Электрофизиологические методы лечения больных с хронической сердечной недостаточностью включают имплантацию кардиостимуляторов с адаптированной к физической нагрузке частотой стимуляции и кардиовертеров-дефибрилляторов пациентам с хронической сердечной недостаточностью и опасными для жизни нарушениями ритма сердца и проводимости. Европейскими рекомендациями 2005 предложено использовать этот метод для улучшения прогноза больных постинфарктный кардиосклероз с высоким риском внезапной смерти (снижение до 35% фракции выброса левого желудочка через 40 дней от момента развития инфаркта миокарда).
Перспективным методом является ресинхронизации сокращения сердца с помощью трехкамерной стимуляции его (с обоих желудочков и правого предсердия). Метод позволяет устранить асинхронию в сокращении желудочков и предсердий и установить оптимальную для каждого больного атриовентрикулярную задержку (время между сокращениями предсердий и желудочков), что обеспечивает оптимальное диастолическое наполнение и сердечный выброс. Ресинхронизации работы сердца позволяет достигать клинического улучшения, замедлять ремоделирования сердца и повышать качество жизни. Показана пациентам с желудочковой десинхрониею (продолжительностью более 120 мс) и тяжелой хронической сердечной недостаточностью, резистентной несмотря оптимальную медикаментозную терапию.
В Европейских рекомендациях 2005 г. для лечения больных с тяжелой хронической сердечной недостаточностью (выше III функциональный класс по NYHA и фракцией выброса левого желудочка менее 35%) рекомендуется также комбинация кардиовертеров- дефибрилляторов и бивентрикулярнои электрокардиостимуляции.
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.