Эпидемиология и этиология
Фибрилляция (мигание) предсердий основывается на неправильной, дезорганизованы электрической активности предсердий, которая приводит к асинхронного возбуждения и сокращения их отдельных участков с частотой свыше 350 за 1 мин и сопровождается неправильным ритмом желудочков.
По характеру течения различают пароксизмальной (ритм восстанавливается самостоятельно в течение 48 ч), ПЕРСИСТИРУЮЩЕЙ (для восстановления синусового ритма необходимо вмешательство) и постоянную (синусовый ритм восстановить невозможно или нецелесообразно) формы фибрилляции предсердий.
Эпидемиология . Фибрилляция предсердий - самая распространенная из всех аритмий. Частота ее выявления среди взрослого населения в значительной степени зависит от возраста, несколько чаще она встречается у мужчин. Среди лиц в возрасте до 40 лет ее частота составляет менее 0,5%, у лиц старше 70 лет - более 10%.
Кроме пожилого возраста, к факторам риска фибрилляции предсердий относят органические заболевания сердца, повышают вероятность ее возникновения в среднем в 3-5 раз.
Этиология. Основными этиологическими факторами фибрилляции предсердий является системная артериальная гипертензия, различные формы ИБС, пороки митрального клапана (стеноз и недостаточность) ревматического и неревматического происхождения и гипертиреоз .
Хотя сейчас в промышленно развитых странах распространенность ревматических пороков сердца и, следовательно, связанной с ними фибрилляции предсердий значительно уменьшилась, эта патология представляет наибольший риск возникновения фибрилляции предсердий, повышая его, по данным Фремингемского исследования, у мужчин в 8 раз, а у женщин - в 27. При наличии застойной сердечной недостаточности риск возрастает соответственно в 9 и 14 раз, а при АГ с признаками гипертрофии левого желудочка на ЭКГ и (или) кардиомегалией - в 5 и 4 раза. ИБС способствует развитию фибрилляции предсердий основном в случае осложнения ее острой или хронической сердечной недостаточностью, митральной регургитацией вследствие дисфункции сосочковых мышц. При остром инфаркте миокарда фибрилляция предсердий встречается в 20-30% случаев.
Независимо от характера заболевания сердца возникновения фибрилляции предсердий приводит дилатацию левого предсердия, часто наблюдается с возрастом, а также при наличии системной артериальной гипертензии, гипертрофической кардиомиопатии и сердечной недостаточности различного генеза, причем не только систолической, но и диастолической.
При аортальных пороках сердца фибрилляция предсердий бывает очень редко, и такие случаи должны настораживать относительно возможности сопутствующей недостатки митрального клапана, даже если нет типичной мелодии сердца.
Фибрилляция предсердий часто встречается у больных с дефектом межпредсердной перегородки и аномалией Ебштайна. Среди больных с дефектом межпредсердной перегородки она возникает обычно у лиц старше 40 лет и наблюдается более чем у 50% пациентов старше 60 лет.
Пароксизмальная фибрилляция предсердий - частое осложнение кардиохи-рургичних операций, особенно аортокоронарного шунтирования и протезирования клапанов сердца. Она развивается во время операции и в раннем послеоперационном периоде в 5-40% таких больных, чаще пожилого возраста, в связи с повышенной активностью симпатико-адреналовой системы, острой сердечной недостаточностью, гипоксией миокарда и повреждением перикарда и обычно проходит самостоятельно.
Распространенными позасерцевимы этиологическими факторами фибрилляции предсердий является злоупотребление алкоголем и гипертиреоз. В первом случае она может развиваться при острой интоксикации, в период абстиненции и при алкогольной кардиомиопатии. Этиловый спирт приводит к возникновению фибрилляции предсердий через способность продлевать внутрипредсердную проводимость.
В случае манифестного гипертиреоз фибрилляция предсердий развивается в 10-20% случаев, чаще у лиц старше 60 лет, особенно у мужчин (более 25%). Считают, что возникновение этого нарушения ритма при гипертиреоз связано с потенцированием действию катехоламинов и повышением возбудимости миокарда предсердий.
В 20-30% случаев причину фибрилляции предсердий не удается установить и считается идиопатической, или изолированной. При этом нет также признаков дисфункции желудочков по данным эхокардиографии.
Патогенетические механизмы
Электрофизиологические механизмы фибрилляции предсердий является образование множественных, не менее 5-6, волн микрориентри в предсердиях. Они в основном неустойчивы, не имеют фиксированного пути циркуляции и, встречая группы мышечных волокон, находящихся в состоянии реф-рактерности, делятся на дочерние волны.
Условиями для возникновения фибрилляции предсердий является малая длина волны риентри и размеров предсердий. Возникновения коротких волн обусловлено замедлением локального проведения импульсов возбуждения и укорочением эффективного рефрактерного периода миокарда предсердий. Первом способствуют очаги фиброза, ишемии, воспаления, нарушения электролитного обмена, повышения тонуса парасимпатической и снижение тонуса симпатической части вегетативной нервной системы, а второй - повышение тонуса как парасимпатической, так и симпатической частей. Фибрилляцией предсердий вызывают предсердные экстрасистолы или импульсы электрокардиостимуляции, которые попадают в "уязвимый" период сердечного цикла, а также (в единичных случаях) при наличии способных к ретроградного проведения дополнительных пе-редсердно-желудочковых путей - желудочковые экстрасистолы.
К желудочков проводится лишь малая часть импульсов, которые, имея достаточную силу, смогли застать предсердно-желудочковый узел в редкие моменты выхода из состояния рефрактерности. Существенное влияние на проводимость и эффективный рефрактерный период предсердно-желудочкового узла тонус парасимпатической и симпатической частей вегетативной нервной системы.
Фибрилляция предсердий сопровождается правильным ритмом желудочков только в сочетании с полной предсердно-желудочковой блокадой (синдром Фредерика), когда нарушения и сокращения желудочков обеспечивается узловым или идиовентрикулярного водителем ритма.
Патологическая анатомия . Морфологические изменения в предсердиях при фибрилляции включают их дилатацию различной степени выраженности, уменьшение площади мышечных волокон и увеличение площади фиброзной и жировой ткани. При воспалительных заболеваниях миокарда в ткани предсердий обнаруживают воспалительные инфильтраты. Часто наблюдают также дистрофические изменения кардиомиоцитов.
Особое значение для развития фибрилляции предсердий имеют потеря части их мышечных волокон и увеличение распространенности соединительной ткани. Это обусловлено тем, что импульс возбуждения предсердиями в отличие от желудочков проводится не специальными клетками проводящей системы, а исключительно "рабочими" кардиомиоцитами.
В целом морфологические изменения в миокарде у больных с фибрилляцией предсердий неспецифичны и аналогичны таковым при старении, что согласуется с хорошо известным фактом о прогрессивное повышение ее частоты с возрастом.
У значительной части больных в предсердиях обнаруживают тромбы, излюбленной локализацией которых ушки. их возникновению способствуют присущие фибрилляции предсердий гиперкоагуляционные изменения в плазме крови и активация тромбоцитов. Эти тромбы является очагом тромбоэмболий - распространенного осложнения фибрилляции предсердий. Частота выявления внутрипредсердную тромбов возрастает с увеличением продолжительности аритмии.
Клиническая картина
Выраженность симптомов фибрилляции предсердий может быть разной и отчасти зависит от ЧСС и степени дисфункции желудочков вследствие основного заболевания. В некоторых случаях больные не ощущают аритмии и она может обнаруживаться случайно.
Распространенными жалобами является сердцебиение, одышка, головокружение и слабость. Эти жалобы, однако, неспецифичны и часто наблюдаются при синусовом ритме. Относительно более редкими симптомами являются обморочные при длинных паузах и стенокардия, вплоть до нестабильной, вызываемая увеличением гипоперфузии миокарда вследствие снижения МОС. Описаны также увеличение количества мочи, что может быть связано с усилением образования передсер-дного натрийуретического гормона или повышенным тонусом симпатической части вегетативной нервной системы.
У большинства больных аритмия возникает без видимой причины. Реже можно установить ее связь со злоупотреблением алкоголем, крепким кофе, курением, стрессом и значительной физической нагрузкой. У части больных при тщательном сборе анамнеза удается обнаружить указания на возникновение приступов аритмии на фоне гиперпарасимпатикотонии или симпатикотонии.
В ходе клинического исследования характерно нерегулярный пульс без каких-либо закономерностей изменений его ритма и частоты, в результате чего фибрилляцией предсердий образно называют полной аритмией (arrhythmia completa). Все пульсовые волны разного наполнения, что приводит непрерывное колебание величин AT. Основном пульс частый (тахисистолическая форма фибрилляции предсердий), но может отмечаться и брадикардия, свойственна фибрилляции предсердий при синдроме слабости пазушные-предсердного узла или обусловлена применением лекарственных препаратов, которые замедляют предсердно-ШЛУ-ночкову проводимость. При тахикардии часто наблюдают дефицит пульса, связан со значительным снижением ударного выброса после короткой диастолы. При аускультации отмечают неодинаковую звучность и тона. После короткой диастолы - хлопанье И тона. Однако эти клинические признаки не позволяют достаточно надежно отличить фибрилляцией предсердий от других аритмий.
Диагностика
Диагностика включает регистрацию ЭКГ в 12 отведениях для оценки ритма сердца и эхокардиографию для определения этиологии аритмии. Для уточнения последней по показаниям используют также специальные методы исследования: определение функции щитовидной железы, нагрузочные тесты, коронарографию, рентгенографию грудной клетки и другие методы исследования органов дыхания.
Электрокардиография в 12 отведениях является основным и високоинформатив-ным методом распознавания фибрилляции предсердий (рис. 59), диагностические признаки которого включают:
1) отсутствие зубцов Р, вместо которых определяются беспорядочные волны фибрилляции f с частотой 350-600 в 1 мин. Эти волны, отражающие нарушения отдельных участков предсердий очагами микрориентри, могут иметь разную амплитуду и длительность
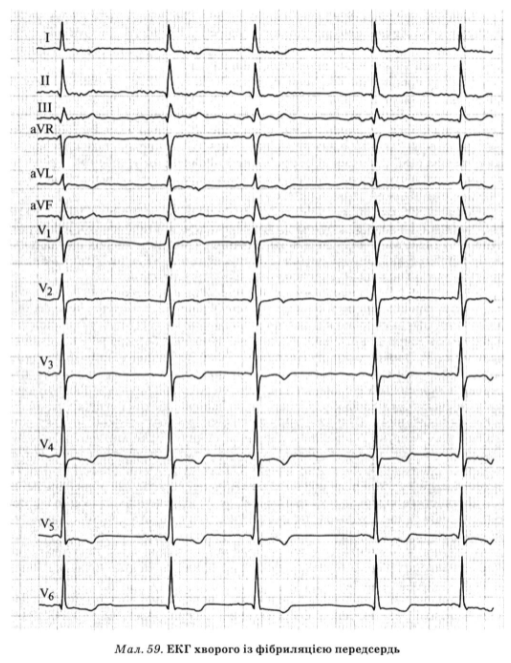
2) неправильный ритм желудочков. При этом все интервалы R-R разные, без каких-либо закономерностей колебаний их величин
3) электрическую альтернации, есть небольшие колебания амплитуды зубцов комплекса QRS, форма которого в основном не изменена по сравнению с таковой при синусовом ритме.
Электрокардиография позволяет также выявить признаки гипертрофии и ишемии миокарда желудочков, перенесенного инфаркта миокарда и сопутствующие желудочковые аритмии, имеет определенное значение для оценки этиологии фибрилляции предсердий и выбора тактики лечения.
Эхокардиография является обязательным методом обследования больных с фибрилляцией предсердий. При этом определяют диаметр предсердий, прежде левого, показатели функции левого желудочка, наличие пороков и других структурных изменений сердца. Важное значение имеет выявление тромбов в предсердиях.
Дифференциальная диагностика . Великохвильову фибрилляцией предсердий необходимо дифференцировать с трепетанием предсердий. При дрибнохвильовои фибрилляции признаки электрической активности предсердий на ЭКГ могут не определяться, что склонности к брадикардии может напоминать ритм, уходящую предсердно-желудочкового соединения. Характерными признаками фибрилляции предсердий в этом случае является вариабельность интервала R-R, а также выявление волн f при регистрации ЭКГ с усилением или при проведении чреспищеводной электрокардиографии.
Еще большие проблемы возникают при дифференциальной диагностики фибрилляции предсердий с широкими комплексами QRS причине "древней" сопутствующей блокады ножки предсердно-желудочкового пучка или синдрома Вольф-фа-Паркинсона-Байта и желудочковой тахикардии , особенно при частом ритме желудочков, когда колебания интервала R-R минимальны. При этом следует учитывать, что желудочковая тахикардия основном сопровождается нарушениями гемодинамики и, отличаясь нестабильностью, довольно быстро переходит в фибрилляцию желудочков.
общем диагноз фибрилляции предсердий чаще всего устанавливают на основании характерных данных электрокардиографии в 12 отведениях, и применение сложных методов исследования, в частности электрофизиологического исследования, не нужно.
Осложнения
Основными осложнениями фибрилляции предсердий является сердечная недостаточность и системные тромбоэмболии.
При возникновении тахисистолической формой фибрилляции предсердий нарушение опорожнения левого предсердия и левого желудочка у некоторых больных может приводить к резкому повышению давления в легочных венах и капиллярах, вплоть до развития сердечной астмы и альвеолярного отека легких . К острой левожелудочковой недостаточности особенно подвержены больные с митральным стенозом и гипертрофической кардиомиопатией. Однако самым распространенным осложнением является развитие или усиление хронической сердечной недостаточности.
Фибрилляция предсердий - причина более 85% всех случаев тромбоем-боли в артериях большого круга кровообращения, очагом которых внутрисердечные тромбы; 2/3 тромбоэмболий попадает в сосуды головного мозга. Нарушения мозгового кровообращения ишемического генеза наблюдается почти у 1/3 больных с фибрилляцией предсердий. С ней связано целом примерно 15% всех случаев инсульта, причем с возрастом этот процент возрастает в связи с увеличением распространенности фибрилляции предсердий.
К независимых факторов риска инсульта и периферийных тромбоэмболий при фибрилляции предсердий относят:
1) возраст 65 лет
2) транзиторную ишемическую атаку или мозговой инсульт, или тромбоэмболии любой другой локализации в анамнезе
3) сахарный диабет
4) системную АГ
5) застойную сердечную недостаточность.
При наличии этих факторов риска частота инсульта превышает 5-7% в год, тогда как без них составляет лишь около 1%.
Лечение и вторичная профилактика. Стратегия и тактика ведения больных с различными формами фибрилляции предсердий определены Рекомендациями рабочей группы по нарушениям сердечного ритма УНТК (2002) и предусматривает решение двух основных задач:
1) уменьшение клинических симптомов
2) предотвращение осложнений (инсульты, сердечной недостаточности и инфаркта миокарда), что позволяет уменьшить смертность.
Лечение
Лечебная тактика следует из определения в любом случае принципиальной стратегии лечения: либо стремиться к восстановлению и содержанию синусового ритма, или, не ставя это целью, обеспечить оптимальный контроль за ЧСС. Обе стратегии имеют "за" и "против". Преимущества сохранения синусового ритма включают устранение симптомов аритмии и связанных с ней нарушений гемодинамики, повышение толерантности к нагрузкам, улучшение качества жизни, отсутствие потребности в антикоагулянтной терапии и уменьшения риска тромбоэмболий. Основными недостатками такого подхода является ограниченная эффективность используемых с этой целью методов и опасность побочных эффектов, прежде Проаритмические, при использовании лекарственных препаратов, а также "нормализационного" тромбоэмболий. Вместе контроль ЧСС при сохранении фибрилляции предсердий не связананий с риском аритмогенности, однако дает худший симптоматический эффект и требует неопределенно длительного проведения антикоагулянтной терапии у большинства больных.
Контроль ЧСС при подготовке к восстановлению синусового ритма. При отсутствии у больного с фибрилляцией предсердий клинических симптомов и нарушений гемодинамики проводят обследование с целью выбора оптимальной тактики его ведения. Это обусловлено тем, что в течение 72 ч у 40-50% больных синусовый ритм сердца восстанавливается самостоятельно. При наличии выраженной тахикардии в этот период целесообразно назначать p-адреноблокаторы и седативные препараты. При сохранении фибрилляции предсердий синусовый ритм восстанавливают анти-аритмичным препаратами или с помощью электрической кардиоверсии.
Снижение ЧСС до проведения антиаритмической терапии обязательна также и у больных с симптоматической фибрилляцией предсердий. Для этого рекомендуют назначать дигоксин (0,25 мг внутривенно или перорально каждые 2 ч до 1,5 мг), амиодарон (800 мг перорально в сутки), Р-адреноблокаторы (пропранолол 0,15 мг /кг в сутки) или недигидроперидинови антагонисты кальция (верапамил 0,15 мг /кг за 2 мин). Параллельно с мероприятиями, направленными на снижение ЧСС, проводят ЭКГ-обследования больного с оценкой структурных изменений сердца и наличии тромбов в его полостях, определение состояния свертывающей системы крови, назначают антикоагулянты. Синусовый ритм восстанавливают только после адекватного снижения ЧСС.
Восстановление синусового ритма. Вероятность восстановления и устойчивого сохранения синусового ритма у больных с фибрилляцией предсердий с помощью лекарственных препаратов и электроимпульсной терапии зависит от запущенности фибрилляции предсердий и ее причины. При прочих равных условиях она меньше у больных с митральным стенозом.
Медикаментозная кардиоверсия . При восстановлении синусового ритма у больных с фибрилляцией предсердий без выраженных структурных изменений сердца предпочтение отдается пропафенона и хинидина. Если эти препараты не дают эффекта, можно использовать амиодарон или прокаинамид. При наличии застойной сердечной недостаточности препаратом выбора является амиодарон, отрицательный инотропный эффект которого выражен в меньшей степени, чем антиаритмических препаратов I класса. Кроме того, амиодарон уменьшает ЧСС, предотвращая перехода фибрилляции предсердий в трепетание предсердий с проведением 1:1 или 1:2.
Препарат 1С класса пропафенон позволяет восстановить синусовый ритм у 50% пациентов с ПЕРСИСТИРУЮЩЕЙ фибрилляцией предсердий, однако следует помнить о способности этого препарата в отдельных случаях увеличивать ЧСС вследствие перехода фибрилляции предсердий в их трепетание или предсердную тахикардию с предсердно-желудочковым проведением 1:1.
Среди препаратов, которые назначают для восстановления синусового ритма, наибольший опыт накоплен по применению прокаинамида (новокаинамида). Его общепринятая доза 5-15 мг /кг (вводят внутривенно капельно в течение 10-15 мин).
К эффективных средств медикаментозной кардиоверсии "свежей" фибрилляции предсердий относится также антиаритмический препарат III класса амиодарон. Вследствие специфики фармакокинетики введенный внутривенно амиодарон менее способен быстро восстановить синусовый ритм, чем предотвратить рецидивы фибрилляции предсердий. Однако кардиоверсия достигается в 64-80% больных.
Нагрузочная доза амиодарона для купирования фибрилляции предсердий колеблется в пределах от 800 до 2000 мг в сутки. Существенным преимуществом амиодарона перед другими антиаритмическими препаратами одновременное угнетение предсердно-желудочковой проводимости, что обеспечивает контроль ритма желудочков, а также наименьшая аритмогенность и практически полное отсутствие отрицательного инотропного действия.
недавнего времени для медикаментозной кардиоверсии широко использовали хинидин. Восстановление синусового ритма этим препаратом начинают с нагрузочной дозы 300-600 мг с последующим назначением поддерживающей дозы 200-400 мг каждые 6 ч (20 мг /кг в сутки).
Электрическая кардиоверсия . Соответствии с Рекомендациями УНТК (2002), показаниями к срочной электрической кардиоверсии является пароксизм фибрилляции предсердий
1) с высокой частотой на фоне острого коронарного синдрома
2) в сочетании с артериальной гипотензией, острой или прогрессивной хронической сердечной недостаточностью
3) не поддается медикаментозному лечению.
Существенными преимуществами срочной кардиоверсии есть возможность улучшения состояния гемодинамики и уменьшения проявления сердечной недостаточности, в том числе за счет исключения препаратов с отрицательным инотропным действием, предотвращения электрическом ремоделированию сердца. Однако во время проведения срочной кардиоверсии риск "нормализационного" эмболии и осложнений общей анестезии у больных с отеком легких или тяжелой сердечной недостаточностью.
Плановая электрическая кардиоверсия при фибрилляции предсердий показана в случае:
1) неэффективности медикаментозной терапии
2) непереносимости антиаритмических препаратов или риска, связанного с их назначением
3) прогрессирование сердечной недостаточности, ухудшение кровообращения мозга, нижних конечностей вследствие тахиаритмии
4) наличия сведений о предыдущих удачных кардиоверсии.
Осложнения электроимпульсной терапии: системная эмболия, желудочковые тахикардия и фибрилляция желудочков, острая левожелудочковая недостаточность, повреждения миокарда, экстрасистолия, синусовая тахикардия, синусовая брадикардия и гипотензия.
Противопоказаниями к плановой электрической кардиоверсии является интоксикация сердечными гликозидами, гипокалиемия, острые инфекционные заболевания, не-компенсированная сердечная недостаточность.
Подготовка к плановой электрической кардиоверсии включает:
1) отличие сердечных гликозидов и диуретиков за 5 дней до кардиоверсии
2) коррекцию нарушений электролитного обмена (введение глюкозоинсулинокалиевои смеси)
3) назначение антиаритмических препаратов (хинидин, дизопирамид, етацы-зин в средних суточных дозах, амиодарон в насыщающей дозе)
4) назначение прямых или непрямых антикоагулянтов
5) проведение премедикации, включающий подкожное введение 1 мл 2% раствора промедола и 0,4-1 мл 0,1% раствора атропина, инфузию глюкозоинсулинокалиевои смеси.
Восстановление синусового ритма у больных с фибрилляцией предсердий путем трансторакальной деполяризации впервые было предложено В. Lown и соавт. в 1962 p. Успешная электрическая кардиоверсия достигается в 70-95% случаев, в значительной мере зависит от особенностей контингента больных, давности фибрилляции предсердий, характера основного заболевания.
Активный электрод дефибриллятора располагают в области верхушечного толчка, второй - справа от грудины в области второго-третьего межребрових промежутков под правой ключицей или между лопатками слева. Минимальная мощность первого разряда для трансторакальной электрической кардиоверсии составляет 50-100 Дж. При отсутствии эффекта ее постепенно повышают до 360 Дж.
Поддерживающая антиаритмическое терапия
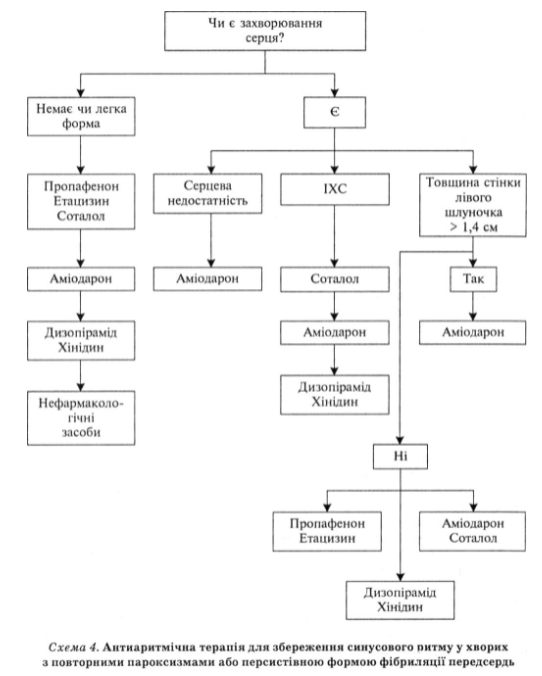
Выбор тактики ведения больных с пароксизмальной фибрилляцией предсердий зависит от наличия и характера заболевания сердца, частоты и клинического течения пароксизма (схема 4).
Для предотвращения рецидивов фибрилляции предсердий после восстановления синусового ритма используют антиаритмические препараты, которые назначают перед электрической кардиоверсии или сразу после нее. До недавнего времени для этого применяли хинидин, что, по данным некоторых рандомизированных исследований и их мета, увеличивал частоту сохранения синусового ритма через год после кардиоверсии в 2 раза - с 25 до 50%. Однако длительное употребление этого препарата сейчас считают нецелесообразным из-за побочных эффектов и сведения о росте вероятности смерти от разных причин.
Высокую эффективность в предотвращении рецидивов фибрилляции предсердий имеют препараты 1С класса (пропафенон), обеспечивающих сохранение синусового ритма в течение 1 года у 40% больных, резистентных к препаратам ИА класса. Однако их назначение не показано после инфаркта миокарда и при наличии дисфункции левого желудочка из-за опасности аритмогенного действия.
Проведенные до сих пор немногочисленные контролируемые исследования дают основание полагать, что наиболее эффективным в предотвращении рецидивов фибрилляции предсердий является амиодарон. В случае его применения в средней дозе 200 мг в сутки в течение 1 года синусовый ритм сохраняется у 2/3 больных, а к концу 3-го года - в 53%. Длительное использование малых поддерживающих доз амиодарона (200 мг в сутки и меньше) не вызывает существенного риска тяжелых побочных явлений.
Медикаментозную профилактику рецидива фибрилляции предсердий после успешной кардиоверсии проводят у больных с повышенным риском его возникновения и (или) в случае, когда такой рецидив может вызвать значительное ухудшение состояния больного. После первого пароксизма идиопатической фибрилляции предсердий обычно ограничиваются рекомендациями избегать возможных провокувальних факторов. Нет необходимости в профилактической антиаритмической терапии также при исчезновении причины аритмии, как, например, фибрилляции предсердий, связанной с острым инфарктом миокарда, кардиохирургической операции, острой алкогольной интоксикации. В случае установления потенциально обратимой причины фибрилляции предсердий (гипертиреоз, митральный стеноз, дефект межпредсердной перегородки) рекомендуют лечение основного заболевания.
Немедикаментозная профилактика парокеизмив фибрилляции предсердий последнее время приобретает широкое распространение, что обусловлено повышением эффективности и устранением риска побочных эффектов, связанных с употреблением антиаритмических препаратов. Ее применяют в случае рефрактерности к медикаментозной терапии или ее непереносимости, включая различные методы катетерной абляции, постоянной электрокардиостимуляции и хирургического лечения.
Для контроля желудочкового ритма при пароксизмах фибрилляции предсердий, сопровождающихся нарушениями гемодинамики и (или) тяжелыми симптомами, обусловленными выраженной тахикардией, применяют катетерная абляция предсердно-желудочкового вузла.
Весьма перспективной является линейная абляция предсердий с целью создания в них нескольких барьеров для циркуляции волн возбуждения. При этом также изолируют легочные вены. Хорошего эффекта оперативного вмешательства, что позволяет полностью отказаться от медикаментозной терапии, достигают примерно у 40% больных.
Хирургическое лечение имеет целью создание барьеров для риентри в большей части миокарда предсердий, устраняет условия для их фибрилляции (хирургическая изоляция предсердий англ. maze).
Показания к хирургическому лечению целом те же, что и к катетерной абляции предсердно-желудочкового узла, и включают плохую переносимость фибрилляции предсердий (как пароксизмальной, так и устойчивой) и ее рефрактерность к медикаментозной терапии, а также рецидивирования тромбоэмболий несмотря адекватную антикоагулянтную терапию. Опыт этой операции еще относительно невелик и свидетельствует о возможности устойчивого восстановления синусового ритма у большинства больных не только с пароксизмальной формой фибрилляции предсердий, но и с постоянной формой. Однако у 20-50% больных в послеоперационный период возникает потребность в постоянной электрокардиостимуляции вследствие развития дисфункции пазушные-предсердного узла. Это обстоятельство, а также риск послеоперационных осложнений, как при любом достаточно длительном хирургическом вмешательстве с искусственным кровообращением, ограничивают сферу применения хирургической изоляции предсердий случаями тяжелого течения фибрилляции предсердий, которая не поддается другим методам лечения. Ее выполнение обоснованное также у больных, подлежащих кардиохирургической операции по поводу сопутствующего заболевания сердца, в частности митрального порока.
Контроль ЧСС у больных с постоянной формой фибрилляции предсердий
Контроль ЧСС при постоянной форме фибрилляции предсердий предотвращает развитие аритмической кардиомиопатии и способствует оптимизации гемодинамики. ЧСС у больных с фибрилляцией предсердий считается контролируемой, если ее величина не превосходит 90 за 1 мин, а при субмаксимальной физической нагрузке - 120 за 1 мин. При этом среднесуточная ЧСС, по данным холл-теривського мониторирование ЭКГ, не должна превышать 80 в 1 мин, а также не должно быть эпизодов тахиаритмии с частотой более 100 сокращений за 1 мин продолжительностью более 1 часа.
Медикаментозный контроль частоты ритма желудочков основывается на применении препаратов, которые удлиняют эффективный рефрактерный период и замедляют проведение импульсов в предсердно-желудочковом узле. К ним относятся дигоксин, p-адреноблокаторы и блокаторы кальциевых каналов верапамил и дилтиазем. Эти препараты не дают столь тяжелых побочных эффектов, как антиаритмические средства ИА, 1С и III классов, используемые для купирования и предупреждения пароксизмов фибрилляции предсердий, что приводит лучшую переносимость медикаментозного контроля ЧСС.
Дигоксин замедляет предсердно-желудочковое проведение косвенно, за счет ваготоничного эффекта, нивелируется при повышении активности симпатико-адреналовой системы. Поэтому он значительно хуже снижает ЧСС во время физической нагрузки, чем у покое. Дигоксин является препаратом выбора для контроля ЧСС при постоянной форме фибрилляции предсердий у больных с застойной сердечной недостаточностью, а также у больных пожилого возраста. Препарат назначают внутрь в суточной дозе 0,125-0,375 мг.
В отличие от дигоксина, p-адреноблокаторы, верапамил и дилтиазем у больных с фибрилляцией предсердий уменьшают ЧСС не только в состоянии покоя, но и во время физической нагрузки, а в случае введения их действие наступает быстро - через 5-10 мин.
p-адреноблокаторы являются препаратами, рекомендованными при сердечной недостаточности. их можно с успехом сочетать с дигоксином, что позволяет использовать меньшие дозы.
В неотложных ситуациях пропранолол назначают внутривенно начиная с 1 мг за 1 мин до общей дозы 5 мг. В случае недостаточного эффекта и стабильности гемодинамики препарат вводят малыми дозами повторно до достижения дозы 0,15 мг /кг. Поддерживающая доза для приема внутрь - 20-80 мг каждые 6-8 часов.
Р-адреноблокаторы также препаратами выбора у больных с постоянной фибрилляцией предсердий на фоне ИБС, артериальной гипертензии, при систолической дисфункции и застойной сердечной недостаточности. Для контроля за ЧСС у таких пациентов можно использовать метопролол или атенолол (25-500 мг в сутки).
Недигидропиридинови антагонисты кальция (дилтиазем, верапамил 120-360 мг) применяют у больных с постоянной фибрилляцией предсердий при бронхообструктивном синдроме, нарушениях периферического кровообращения и сахарном диабете.
Предотвращение тромбоэмболии
Системные тромбоэмболии, прежде сосудов головного мозга, - довольно частое осложнение фибрилляции предсердий, может развиваться при любой формы фибрилляции, а также в ранние сроки после успешной предсердной дефибрилляции (так называемые нормализационного тромбоэмболии). Поэтому их профилактика является важной составляющей лечения при этом нарушении ритма.
Подходы к антикоагулянтной терапии больных с фибрилляцией предсердий определены Рекомендациями рабочей группы по нарушениям сердечного ритма УНТК (2002).
Пароксизмальная фибрилляция предсердий, впервые (ритм восстановился самостоятельно в течение 48 ч), при отсутствии гипотензии, сердечной недостаточности и стенокардии обычно не требует лечения. Антикоагулянтную терапию проводят при наличии факторов риска тромбоэмболий.
Факторами риска развития цереброваскулярных осложнений являются: митральная порок сердца, перенесенные ранее эмболии и инсульт, артериальная гипертензия, возраст 65 лет, инфаркт миокарда в анамнезе, ИБС, сахарный диабет, выраженная систолическая дисфункция левого желудочка или застойная сердечная недостаточность, увеличение размера левого предсердия более чем на 50 мм и тромб в левом предсердии.
Стратификация риска инсульта является сейчас ведущим критерием подбора антикоагулянтной терапии у больных с постоянной формой фибрилляции предсердий.
Антитромботической терапии у пациентов любого возраста с фибрилляцией предсердий без заболеваний сердца и факторов риска, а также пациентов с заболеваниями сердца, но без факторов риска в возрасте до 60 лет проводят аспирином в дозе 365 мг в сутки. Больные с фибрилляцией предсердий старше 65 лет, имеющие факторы риска инсульта, должны получать антикоагулянты (варфарин) в дозах, обеспечивающих снижение про-тромбинового индекса до 45-55%. Непрямые антикоагулянты назначают в течение 3 нед, после кардиоверсии - в течение 4 нед.
При необходимости быстрого проведения кардиоверсии возможно использование прямых антикоагулянтов - нефракционированного гепарина или низкомолекулярных гепаринов.
При персистивний форме фибрилляции предсердий, возникла впервые, проводят антикоагулянтную терапию и контроль за ЧСС, рассматривают возможность медикаментозной терапии или кардиоверсии. Чаще потребности в длительной медикаментозной терапии нет.
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.