Эпидемиология и этиология
Инфекционный эндокардит - это заболевание, вызванное микробным инфицированием касающихся крови внутрисердечных структур и инородных тел, а также крупных внутригрудных сосудов с образованием вегетаций, которые представляют собой конгломерат из фибрина, тромбоцитов и микробных тел.
Эпидемиология. Заболеваемость инфекционный эндокардит у США и странах Западной Европы колеблется от 25 до 93 на 1 млн населения. На его долю приходится около 1 из 1000 случаев госпитализации по разным причинам. Несмотря на применение новых антибактериальных средств и широкое использование хирургических методов лечения этого заболевания, летальность остается высокой - 18-36%.
В последние десятилетия наблюдается рост заболеваемости инфекционный эндокардит. Так, по данным Института сердечно-сосудистой хирургии АМН Украины, с 1982 до 1996 г. распространенность этого заболевания в структуре причин приобретенных пороков сердца у оперированных больных увеличилось в 8 раз.
Существенное влияние на заболеваемость оказывает наркомания и рост числа различных инвазионных медицинских манипуляций. Так, у лиц, вводящих наркотики внутривенно, риск возникновения инфекционного эндокардита в 30 раз выше, чем у больных с ревматическими пороками сердца. Инфекционный эндокардит у пациентов с протезированными клапанами сердца в течение 1-го года после операции развивается в 1-4%, а в более поздний срок - почти у 1% больных в год.
Мужчины болеют инфекционный эндокардит в 2-3 раза чаще, чем женщины. В промышленно развитых странах в течение последних 30 лет наблюдается выраженная тенденция к "старению" инфекционного эндокардита. Средний возраст таких больных достигает 50 лет, а лица старше 60 лет составляют более 25% (в США - 50%).
Этиология. Хотя инфекционный эндокардит могут вызвать практически все патогенные микроорганизмы, в подавляющем большинстве случаев (70-80%) он стрептококковой или стафилококковой этиологии.
Стрептококки. Среди этих микроорганизмов чаще всего причиной инфекционного эндокардита является S. viridans, или а-гемолитические стрептококки - их обнаруживают в 35-40% случаев. Среди них инфекционный эндокардит чаще вызывают S. mitior, S. mutans, S. sanguis, S. anginosus.
Второе место по частоте занимают стрептококки группы D, так называемые фекальные стрептококки, в большом количестве содержатся в нижней части пищеварительного тракта, в мочевой и половой системах. Среди них самым распространенным этиологическим фактором инфекционного эндокардита является S. bovis (20% всех случаев стрептококкового эндокардита). Содержимое S. bovis в толстой кишке увеличивается с возрастом и особенно в случае развития в ней злокачественных опухолей. К стрептококков группы D относят также энтерококки, среди которых инфекционный эндокардит чаще вызывает Enterococcus faecalis (около 10% всех случаев стрептококкового эндокардита).
После широкого внедрения в клиническую практику антибиотиков пневмококковый эндокардит случается довольно редко и преимущественно у ослабленных больных, часто у лиц, зависимых от алкоголя, а также у больных с пневмококковой пневмонией или менингитом.
Стафилококки . За последние 40 лет частота инфекционного эндокардита, вызванного S. aureus, выросла с 5-7% до 20-30%. Стафилококк попадает в кровь преимущественно через кожу, реже - через слизистую оболочку носа и поэтому является основной причиной инфекционного эндокардита у наркоманов, которые вводят наркотики внутривенно, и довольно часто при раннем инфекционном эндокардите протезированных клапанов.
Низьковирулентний комменсалом кожи S. epidermidis (albus) приводит к развитию инфекционного эндокардита собственно клапанов сравнительно редко. Однако в последнее время количество вызванных S. epidermidis случаев инфекционного эндокардита увеличилось. Этот возбудитель часто является причиной инфекционного эндокардита протезированных клапанов - как раннего, так и позднего с острым или подострым течением.
грамотрицательные бактерии, несмотря на большую частоту бактериемии, редко приводят к инфекционного эндокардита собственно клапанов. Это, возможно, связано с их слабо выраженной адгезией к клапанного эндокарда и компонентов тромба и склонностью к лизису под действием комплемента. Риск возникновения такого инфекционного эндокардита, однако, значительно возрастает у больных с протезированными клапанами сердца, особенно в ранние сроки после операции, в меньшей степени - у наркоманов и тех, кто длительное время лечился антибиотиками широкого спектра действия. Среди грамотрицательных бактерий чаще всего вызывают инфекционный эндокардит кишечные микроорганизмы: Pseudomonas, Enterobacter, Klebsiella и Serratia marcenscens, Escherichia coli и протей.
Следует заметить, что анаэробные бактерии вызывают инфекционный эндокардит редко - менее чем в 5% случаев, возможно, из-за относительно высокое парциальное напряжение кислорода в крови, что препятствует их росту на поверхности эндокарда.
Грибы, преимущественно Candida (главным образом Candida albicans), Aspergillus и Histoplasma относят к числу редких этиологических факторов инфекционного эндокардита. Возникновению такого эндокардита способствуют состояние иммунодефицита вследствие длительного применения ГКС, цитостатич-ных иммуносупрессантов, антибиотиков широкого спектра действия или связанный со злокачественными новообразованиями, наличием имплантированных протезов клапанов, элекрокардиостимуляторив, автоматических кардиовертеров-дефибрилляторов, а также долговременное применение внутривенных катетеров, длительное пребывание в стационаре и внутривенное введение наркотических средств.
Еще реже случается инфекционный эндокардит, вызванный возбудителем Q-лихорадки Coxiella burnetti и Chlamidia. Установить этиологический диагноз помогают данные анамнеза (контакт с крупным рогатым скотом и овцами в первом случае и птицами - во втором), а также соответствующие серологические исследования.
высоковирулентные возбудителем, способным вызвать острый инфекционный эндокардит, является Neisseria gonorrhoeae. Однако сейчас благодаря широкому применению антибиотикотерапии случаи гонорейного эндокардита стали единичными.
Роль вирусов в возникновении инфекционного эндокардита не доказано.
Первичный инфекционный эндокардит поражает морфологически неизмененные клапаны и другие структуры сердца. Хотя удельный вес таких больных в последние годы возросла до 30-40%, у большинства больных инфекционный эндокардит, по-прежнему наблюдается его вторичная форма. Процесс развивается на измененном вследствие всяких приобретенных и врожденных аномалий клапанном и пристеночного эндокарда и эндотелия сосудов.
Особой формой вторичного инфекционного эндокардита является эндокардит, который развивается после кардиохирургических операций. В основном это эндокардит протезированных клапанов сердца, который в зависимости от времени возникновения после операции может быть ранним (до 12 мес) и поздним (возникает в более поздние сроки).
Патогенез и патологическая анатомия
Здоровый эндотелий эффективную систему защиты от образования на нем тромбов и развития инфекции. Однако эта система нарушается в случае повреждения эндотелия. В месте нарушения целости эндотелия обнажается соединительная ткань, содержащая коллагеновые волокна, фибронектин и другие соединения, стимулирующие адгезию и активацию тромбоцитов. Тромбоцитни тромбы, образующийся, сначала имеют микроскопические размеры и могут легко отрываться без каких-либо последствий. При откладывании фибрина эти тромбы стабилизируются и постепенно размеры их увеличиваются. Такие стерильные тромботические массы, состоящие из тромбоцитов и переплетенных нитей фибрина с вкрапленными между ними единичными лейкоцитами, имеющие вид разрастаний на поверхности эндокарда, называются вегетациями. Они присущи так называемому Абактериальный, или неинфекционном, тромбоендокардиту.
Инфицирование фибринового матрикса стерильных вегетаций микроорганизмами из крови приводит к возникновению инфекционного эндокардита. Преходящую бактериемии наблюдают довольно часто при различных инвазионных диагностических и лечебных манипуляциях, например при экстракции зуба (в 50-100% случаев), ендотрахейний интубации (в 5-7% случаев). Даже жевания пищи и чистка зубов могут вызвать бактериемии, особенно при наличии стоматита.
омываемых кровью тромботические наложения на эндокарде является наилучшей средой для размножения микроорганизмов. Возбудители накапливаются в большом количестве и стимулируют дальнейшее образование фибрина, что приводит к увеличению размеров вегетаций. С ростом вегетаций микроорганизмы покрываются новыми слоями фибрина, который защищает их от эрадикации.
Хотя воспалительная реакция в месте прикрепления вегетаций может достигать значительной выраженности, вплоть до образования абсцесса, количество лейкоцитов и макрофагов в самых вегетации довольно незначительна. Вегетации лишены сосудов. Лишь в процессе заживления под влиянием лечения у них появляются капилляры и фибробласты.
Вегетации при инфекционном эндокардите могут иметь различные размеры и форму - от мелких узелков диаметром в несколько миллиметров до больших разрастаний, достигающих нескольких сантиметров, в виде полипов или цветной капусты. Создавая препятствие для смыкания створок клапанов и вызывая разрушение их краев, вегетации приводят к развитию или прогрессированию регургитации крови через клапаны. Регургитация может увеличиваться в случае возникновения перфорации створки или разрыва хорды клапана вследствие выраженных эрозивно-некротических изменений в месте прикрепления вегетаций. В случае успешного лечения во время заживления воспаления в процессе рубцевания створки сморщиваются и регургитация крови через пораженный клапан сохраняется.
С вегетацией на створках клапанов инфекция может распространяться на клапанное кольцо и соседней миокард с образованием абсцессов. При этом повреждения корня аорты может сопровождаться его перфорацией с возникновением сообщения между аортой и левым предсердием, правым предсердием и выносным трактом левого желудочка. Распространение инфекции по миокарда межжелудочковой перегородки способно вызывать нарушения проводимости, а прорыв абсцесса в перикард приводит к развитию гнойного перикардита.
Факторы, способствующие возникновению инфекционного эндокардита. Среди таких факторов наибольшее значение имеет наличие различных приобретенных и врожденных аномалий сердца. Среди них у детей преобладают врожденные пороки, чаще открытый артериальный проток и дефект межжелудочковой перегородки. Довольно часто развития инфекционного эндокардита способствуют врожденные пороки сердца синего типа - тетрада Фалло, атрезия легочной артерии и др.. Этот риск хотя и уменьшается, но не исчезает и после их паллиативной и даже радикальной коррекции, почемув способствуют остаточные аномалии и имплантация в сердце искусственных материалов.
В странах с рыночной экономикой, развивающейся значительной проблемой является инфекционный эндокардит у больных с ревматическими пороками сердца. Причем при пороках митрального клапана заболевание возникает чаще, чем при пороках аортального клапана. В странах с развитой рыночной экономикой в последние десятилетия среди взрослых больных с вторичным инфекционным эндокардитом преобладают больные с Неревматические (дегенеративными) приобретенными пороками, прежде аортального, развивающихся в пожилом возрасте. Возросло количество случаев этого заболевания при пролапсе митрального клапана с наличием регургитации. У таких больных риск возникновения инфекционного эндокардита повышается в 5-8 раз.
Пусковым моментом для развития инфекционного тромбоендокардиту могут быть также микротравмы, образующиеся в местах соприкосновения створок неизмененных клапанов.
Наряду с вирулентностью возбудителя развития инфекционного эндокардита способствует нарушение защитных реакций организма, которые должны обеспечивать устранение инфекции. Риск его возникновения повышается при наличии иммунодефицита, например, в связи с сопутствующими хроническими заболеваниями или длительным употреблением препаратов иммуносупрессивной действия.
Для инфекционного эндокардита характерны выраженные позасерцеви проявления, к которым относят эмболии сосудов большого и малого круга кровообращения, микотического сосудистые аневризмы и системную иммунокомплексной патологии.
При поражении левой половины сердца эмболы локализуются в артериях большого круга кровообращения - головного мозга, селезенки, почек, печени, реже - конечностей (грибковый инфекционный эндокардит). При локализации вегетаций в правой половине сердца возникает эмболия ветвей легочной артерии, часто рецидивирующая, которой подвергаются и больные с инфекционным эндокардитом на фоне дефекта межжелудочковой перегородки.
микотического аневризмы обусловлены истончением и выбуханием участка стенки артерии из-за разрушения ее элементов вследствие воспаления, вызванного эмболией инфицированным фрагментом вегетации, обычно без окклюзии просвета сосуда. Серьезным осложнением является кровотечение вследствие разрыва аневризмы, может возникать через несколько недель и месяцев после клинического выздоровления от инфекционного эндокардита.
Полиорганная иммунокомплексной патологии обусловлена "избыточным" ответом иммунной системы на ее длительное антигенное раздражение в связи с долговременной бактериемии. Наряду с усилением образование специфических противомикробных антител отмечают генерализованную гипер-у-глобулинемия, что нарастает с увеличением длительности заболевания при отсутствии адекватного лечения. В крови больных появляются аутоантитела к собственным имуногло-Булин, включая специфические антитела к бактериям, и различные протитканинни аутоантитела к автоантигенив, "обнаженных" вследствие повреждения клеток. Активизация гуморального иммунного ответа сопровождается увеличением образования циркулирующих иммунных комплексов, в повышенном количестве определяются в крови, проникают через стенку капилляров, откладываются в суб-эндотелии и, активизируя комплемент, вызывают повреждения тканей. Наиболее характерными проявлениями иммунокомплексной патологии при инфекционном эндокардите является кожный васкулит, очаговый или диффузный гломерулонефрит. В других, более редких, проявлений иммунокомплексной патологии относят миокардит (очаговый или диффузный) и артрит.
Классификация инфекционного эндокардита (МКБ-10; ЕТК, 2004)
I. Активность процесса: активный, вылечен, рецидивный.
II. Статус диагноза: определенный или вероятен.
III. Эндокардит:
• естественных клапанов,
• протезированных клапанов (ранний, поздний)
• на фоне внутривенного введения наркотических веществ.
IV. Локализация:
• аортальный клапан,
• митральный клапан,
• трехстворчатый клапан,
• клапан легочной артерии,
• эндокард предсердий и желудочков.
V. Возбудитель (грамположительные и грамотрицательные микроорганизмы, L-формы риккетсий, грибы, установлен возбудитель).
VI. Стадия клапанной недостатки; стадия сердечной недостаточности.
VII. Осложнения.
Клиническая картина
Клиническая картина инфекционного эндокардита достаточно полиморфная, что обусловлено неспецифичностью и разнообразием его проявлений, многие из них могут быть скрыты или отсутствуют.
Клинические проявления инфекционного эндокардита можно разделить на 3 группы:
1) симптомы и признаки общей инфекции
2) симптомы и признаки поражения сердца
3) позасерцеви проявления, обусловленные:
а) поражением кожи и слизистых оболочек
б) эмболических осложнениями
в) аутоиммунной патологией.
Клинические проявления общего инфекционного заболевания включают повышение температуры тела, что сопровождается ознобом и потоотделением, болью в суставах конечностей, позвоночнике, мышцах, головной болью, общей слабкистю, ухудшением аппетита, потерей массы тела.
Температура тела повышается у 85-95% больных. Высокая лихорадка с ознобом и обильным потоотделением, которую раньше считали классическим симптомом заболевания, сейчас встречается реже. Такие больные преимущественно жалуются на общую слабость, а повышение температуры тела до субфебрильных цифр обнаруживают лишь при ее измерения в течение суток. Слабую выраженность температурной реакции часто наблюдают у больных пожилого возраста и при развитии почечной и сердечной недостаточности.
Примерно в 40-50% случаев отмечают артралгия и миалгия.
В клинических признаков общеинфекционного синдрома, кроме температурной реакции, относят бледность кожи, спленомегалию, лимфаденопатию и симптом барабанных палочек.
Умеренное увеличение селезенки отмечают у 30-50% больных. При пальпации селезенка обычно безболезненна, за исключением ее инфаркта и абсцесса.
Симптом барабанных палочек, считавшийся ранее классическим признаком инфекционного эндокардита, сейчас случается редко - менее чем у 10% больных. После эрадикации инфекции этот симптом исчезает.
редкое, но тяжелое проявлением общеинфекционного синдрома является токсическая энцефалопатия, сопровождающаяся головной болью, нарушением сознания, а в некоторых случаях очаговой неврологической симптоматикой, может развиваться в начале заболевания.
Клинические проявления поражения сердца - это прежде всего шум и признаки застойной сердечной недостаточности. Значительно реже встречаются блокады сердца и перикардит.
Шум в сердце отмечают у 85-95% больных. Он может не определяться в ранние сроки заболевания, особенно при его остром течении, а появляться гораздо позже - через 2-3 мес. При поражении париетального эндокарда и в некоторых случаях - трехстворчатого клапана шум не обнаруживают даже в случае длительного динамического наблюдения. В таких случаях заподозрить инфекционный эндокардит позволяет сочетание общевоспалительных синдрома при отсутствии видимых очагов инфекции с эмболиями.
Само по себе наличие шума - неспецифическая признак инфекционного эндокардита, потому что он может быть обусловлен предшествующим заболеванием сердца, анемией или лихорадкой. Диагностическое значение шума, однако, возрастает, если он сопровождается тахикардией и другими признаками сердечной недостаточности, остро возникла или усилилась. Наибольшее диагностическое значение имеет систолический шум митральной и трехстворчатого регургитации и протодиастолический шум регургитации крови через аортальный клапан. Шума может не быть также в ранние сроки первичного инфекционного эндокардита и у пациентов с локализацией вегетаций на пристеночного эндокарда или эндотелии крупных сосудов.
Появление в процессе динамического наблюдения нового шума, особенно протодиастолический, вдоль левого края грудины является надежной, хотя и не четко специфической, признаком инфекционного эндокардита, чем увеличение звучности и продолжительности "старого" шума .
Поражение кожи и слизистых оболочек к широкому применению антибиотиков принадлежало к числу довольно распространенных признаков инфекционного эндокардита и отмечалось в 50-90% случаев. Сейчас их наблюдают значительно реже, однако обнаружение этих признаков имеет важное значение для подтверждения диагноза у больных с подозрением на инфекционный эндокардит. Появление кожных проявлений на фоне антибиотикотерапии удостоверяющий его недостаточную эффективность. К кожным проявлениям относят:
1) петехии (в 10-15% случаев), излюбленной локализацией которых конъюнктива (так называемые пятна Лукина-Либмана), слизистая оболочка полости рта в области щек и м 'мягкого неба, дистальные отделы конечностей и туловища. Обычно петехии появляются группами, через 2-3 суток бледнеют и бесследно исчезают. Образование петехий обусловлено микроэмболии сосудов кожи и слизистых оболочек, вызванными высоковирулентные возбудителями, ДВС и повышением проницаемости капилляров
2) линейные геморрагии под ногтевой пластинкой пальцев верхних и нижних конечностей. Размещаются в продольном направлении, не доходя края ногтя, длиной 1-2 мм. Выявляют примерно у 20% больных инфекционный эндокардит. Считают, что причиной таких геморрагий является микроэмболии капилляров ногтевого ложа
3) узелки Ослера - это подкожные узелки, обычно множественные, диаметром 2-5 мм, локализуются на "подушечках" пальцев верхних и нижних конечностей, реже в области тенара и гипотенара. Кожа над ними гиперемирована. их выявляют примерно в 10-15% случаев. Поскольку при биопсии таких узелков обнаруживают инфекционные возбудители, считают, что образование их обусловлено воспалением мягких тканей вокруг септических эмболов в дистальных артериолах
4) пятна Джейнуэя имеют вид красных макулы на коже ладоней и подошв, напоминающие узелки Ослера, отличаясь от них в основном отсутствием болезненности. Наблюдают примерно в 5% случаев. Предполагают, что они представляют собой микроабсцессы вокруг мелких септических эмболов или проявления поверхностного васкулита, связанного с реакциями гиперчувствительности
5) пятна Рота - микроинфаркт сетчатки, обусловленные воспалением ее мелких артериол. Имеют вид красных пятен с неровными контурами (результат кровоизлияния) и бледным центром.
Осложнения
Застойная сердечная недостаточность - распространенное и одно из самых тяжелых осложнений инфекционного эндокардита. Несмотря на антибактериальную терапию, ее частота у больных инфекционный миокардит последние годы мало изменилась и составляет около 50-60%. Основной причиной сердечной недостаточности при инфекционном эндокардите является острое возникновения перегрузки сердца вследствие развития недостаточности клапанов. Гораздо меньшее значение имеет миокардит. Сердечную недостаточность чаще отмечают при эндокардите аортального (примерно в 75% случаев), реже - митрального (50%) и с наименьшей частотой - трехстворчатого (19%) клапана. Она может развиваться как постепенно, медленно, так и довольно быстро. Острое возникновения или нарастания сердечной недостаточности (вплоть до отека легких, трудно устраняется) и в ряде случаев - кардиогенного шока характерно для значительного разрушения створок аортального и митрального клапанов с их перфорацией и разрыва сухожильных хорд митрального клапана. Застойная сердечная недостаточность значительно отягощает прогноз, и если не проводят хирургическую коррекцию порока, большинство таких больных умирает даже в случае значительного эффекта антибактериальной терапии.
Эмболии фрагментами вегетаций возникают в среднем в 35-40% больных инфекционным эндокардитом. Среди эмболии сосудов большого круга кровообращения преобладают эмболии сосудов головного мозга (50% всех эмболий), почек, селезенки и брыжейки, сопровождающиеся инфарктом этих органов. Инфаркт селезенки проявляется острой болью и болезненностью органа при пальпации, инфаркт почки - также преходящей гематурией. Все проявления вскоре проходят. Эмболия брыжеечных артерий дает картину острого живота. Эмболия артерий сетчатки может стать причиной слепоты. Эмболии периферических артерий с развитием гангрены случаются относительно редко, преимущественно у больных инфекционный эндокардит грибковой этиологии. Эмболии могут быть первым признаком инфекционного эндокардита. После назначения антибиотикотерапии риск возникновения эмболии прогрессивно уменьшается.
Не таким частым, как инфаркт, но достаточно серьезным следствием эмболии при инфекционном эндокардите является развитие абсцессов, чаще селезенки, почек, мягких тканей.
Аутоиммунная патология. Поражения различных органов и тканей аутоиммунного происхождения включает гломерулонефрит, миокардит, асептический перикардит, артрит, неврит. Среди них наиболее распространенным является гломерулонефрит. Его диагностируют у 15-25% больных инфекционный эндокардит. Гломерулонефрит у таких больных основном протекает с изолированным мочевым синдромом, но иногда может проявляться и нефротическим синдромом.
У больных инфекционный эндокардит миокардит может иметь иммунный или токсический генез. Его признаки значительной степени маскируют проявления клапанной недостатки, поэтому выделить миокардиальный компонент нарушений кардиогемодинамики довольно сложно. При этом важное значение имеют развитие дилатации левых и правых полостей сердца, а также данные электро-и эхокардиографии.
Перикардит при инфекционном эндокардите может быть как асептическим, так и гнойным. Асептический перикардит обычно сопровождается другими аутоиммунными осложнениями и имеет относительно благоприятное течение, тогда как гнойный перикардит имеет плохой прогноз и требует иной лечебной тактики.
Артрит с синовитом выявляют у больных инфекционный эндокардит довольно редко. Подобно перикардита, он может быть как асептическим, аутоиммунным, так и гнойным.
Абсцессы кольца аортального клапана и прилегающего миокарда часто сопровождающиеся стойкой лихорадкой и могут приводить к возникновению фистул и сообщений аорты с предсердиями и левым желудочком, что сопровождается увеличением сердечной недостаточности. Это осложнение диагностируют лишь с помощью инструментальных методов исследования - эхокардиографии допплер или ангиокардиографии.
Микотичпи аневризмы периферических артерий относят к редким осложнений инфекционного эндокардита. их отмечают менее чем у 10% больных, однако их истинная частота, пожалуй, выше, поскольку в основном эти аневризмы остаются нераспознанными, потому что могут не вызывать каких-либо симптомов или проявляться только устойчивым невыясненным повышением температуры тела. Микотического аневризмы чаще всего локализуются в мозговых и периферических артериях, реже - в нисходящей части аорты, брыжеечных и селезеночных артериях. В процессе лечения инфекционного эндокардита они могут исчезать. Аневризмы могут также осложняться разрывом, что проявляется кровотечением. Разрыв аневризмы иногда возникает много недель и даже месяцев после клинического выздоровления больного от эндокардита.
Диагностика
Лабораторные методы исследования, используемые для диагностики инфекционного эндокардита, включают общие анализы крови и мочи, определение в крови острофазовых и некоторых иммунологических показателей, посев крови и по показаниям - серологические пробы.
Изменения в общем анализе крови неспецифичны и иногда мало выражены. Самые характерные из них:
1. Лейкоцитоз с нейтрофилезом различной степени выраженности. Выраженный лейкоцитоз - до 30 • 10 9 /л - обычно развивается при наличии вне-сердечных "видсивань" инфекции. Почти в 30% минорих в начале заболевания количество лейкоцитов в крови находится в пределах нормы, а иногда даже снижена. При этом, однако, наблюдают сдвиг лейкоцитарной формулы влево, значительно более постоянного, чем лейкоцитоз, признаком инфекционного эндокардита. Часто определяют также токсическое зернистость нейтрофилов.
2. Анемия чаще всего обусловлено угнетением костномозгового кроветворения вследствие интоксикации и имеет характер нормо-или гипохромной. Однако порой анемия приобретает характер гемолитической.
3. Увеличение СОЭ разной степени выраженности - от минимального до значительного (более 50 мм /ч) в течение нескольких месяцев отмечают примерно у 90% больных на инфекционный эндокардит. Этот показатель сохраняется длительно, до нескольких месяцев.
Неспецифическими проявлениями общевоспалительных синдрома является увеличение содержания С-реактивного протеина и диспротеинемия за счет гипер-в 2 - или гипер-у-глобулинемия.
У значительной части больных инфекционный эндокардит обнаруживают неспецифические изменения в общем анализе мочи в виде незначительной протеинурии и микрогематурии. При этом в пользу их связи с гломерулонефритом свидетельствует наличие цилиндрурии, устойчивость протеинурии. Преходящая макрогематурия характерна для инфаркта почек.
Диагностическое значение изменений иммунологических показателей крови относительно небольшое из-за их неспецифичность. Они включают:
1) увеличение уровня иммуноглобулинов М и G и циркулирующих иммунных комплексов
2) снижение уровня комплемента вследствие образования иммунных комплексов
3) появление ревматоидного фактора (у 60-70% больных).
Среди лабораторных методов наибольшее значение для диагностики инфекционного эндокардита имеет посев крови. Бактериемии или фунгемию в тот или иной период времени отмечают у всех больных инфекционный эндокардит. Установлено, что выделение бактерий из вегетаций в кровь обычно происходит не в течение короткого периода времени, а длительно, но нередко с разной интенсивностью. Поэтому считают, что для диагностики инфекционного эндокардита достаточно сделать не менее 3 посевы крови с промежутком не менее 1 ч, каждый отдельной венепункции, отложив на это время назначения антибиотиков (на 3-7 суток в зависимости от длительности предыдущей антибактериальной терапии).
Посев производят на двух средах: для определения аэробной и анаэробной флоры.
Частота ложноотрицательных результатов посева крови при инфекционном эндокардите сейчас составляет от 5 до 30% (в среднем около 10%). К их возможным причинам относят:
1) предварительное лечение антибиотиками
2) высокое содержание в крови противомикробных антител и других природных бактерицидных факторов
3) поражение правых отделов сердца при отсутствии септических видсивань в легких
4) наличие возбудителей, рост которых требует длительной, в течение 7-21 суток, инкубации (некоторые штаммы стрептококков, Corynebacterium, Haemophilus, Actino-bacillus, Cardiobacterium, Eikinella, Kingella и др. .) или специальных сред и методов культивирования (грибы, Brucella, Mycoplasma, Chlamidia, Histoplasma, Legionella, Coxiella burnetti, некоторые штаммы стрептококков и др.).
5) интермитивний характер бактериемии.
Серологические исследования крови проводят, если появляется подозрение на инфекционный эндокардит при устойчивых отрицательных результатов посева крови для выявления антител к антигенам редких возбудителей - Coxiella burnetti, пситтакоза и некоторых грибов.
Инструментальные методы диагностики. Диагностическое значение ЭКГ невелико. Признаки перегрузки левого желудочка в грудных отведениях свидетельствуют о развитии выраженной аортальной или митральной недостаточности.
рентгенография грудной клетки широко используют для определения наличия и выраженности венозного застоя в легких, а также изменений формы и размеров сердца. Изредка при этом удается увидеть отложение кальция в проекции митрального или аортального клапанов, которые могут образовываться как при ревматических пороках, так и вследствие дегенеративных поражений этих клапанов у лиц пожилого возраста. Важное диагностическое значение имеет выявление легочных инфильтратов, иногда с распадом, что позволяет заподозрить инфекционный эндокардит правых отделов сердца, осложненный септическими эмболии сосудов малого круга кровообращения.
Эхокардиография. Диагностическое значение этого метода при инфекционном эндокардите практически не уступает положительным результатам посева крови. Визуализацию вегетаций на клапанах относят к основным признаков этого заболевания. Эхокардиография с допплеровское исследование позволяет также выявить другую патологию структуры и функции клапанов, абсцессы их кольца и прилегающего миокарда, наличие жидкости в полости перикарда и оценить функцию желудочков.
При эхокардиографии в М-режиме вегетации в виде дополнительных "пушистых" эхо на створках аортального и митрального клапанов выявляют лишь в 50% больных инфекционный эндокардит. Чувствительной (до 75% случаев) является трансторакальная двумерная эхокардиография. При этом вегетации имеют вид внутрисердечных образований на ножке, прикрепляемые к створок клапанов, а в случае закрытия клАпана пролабирует в камеру с низким давлением. Характерной особенностью вегетаций является их вращательные движения независимо от движений створок клапанов. Минимальные размеры вегетаций, что визуализируются при эхокардиографии, составляют около 2 мм.
Основные критерии диагностики инфекционного эндокардита при эхокардиографии (Рекомендации ЕТК, 2004)
1) наличие плотной массы, прикрепленной к клапанного или пристеночного эндокарда или имплантированные протеза клапана
2) визуализация протеза или фистулы
3) недостаточность протезированными клапана, особенно в поздние сроки после имплантации.
Во всех сомнительных случаях при отрицательных результатов трансторакаль-ной эхокардиографии следует выполнять чреспищеводной эхокардиографии (см. вклейку, рис. 24). При отрицательных результатах и вероятности инфекционного эндокардита на основании клинических данных чреспищеводной эхокардиографии повторяют через 2-7 суток. Повторный отрицательный результат чреспищеводной эхокардиографии исключает инфекционный эндокардит (Рекомендации ЕТК, 2004).
Магнитно-резонансную томографию можно использовать для уточнения наличия приклапанного абсцесса. Она позволяет также получить информацию о причине очаговой неврологической симптоматики у больных инфекционный эндокардит (инфаркт, кровотечение из микотического аневризмы, абсцесс мозга).
Благодаря широкому распространению эхокардиографии с цветным допплеровское исследование использования инвазивного обследования сердца - его катетеризации и рентгеноконтрастного ангиографии - у больных инфекционный эндокардит значительно сократилось. На сегодня эти методы применяют только в некоторых случаях при решении спорных вопросов о показаниях к операции и ее объема, если антибактериальное лечение не дает желаемого эффекта.
Диагноз инфекционного эндокардита ("определенный" инфекционный эндокардит) устанавливают, если при наличии общего инфекционного процесса есть данные о привлечении эндокарда. "Определенный" инфекционный эндокардит может буги как с установленным возбудителем (положительный бакпосев крови или выявления бактериальной ДНК), так и с отрицательными результатами микробиологического исследования. Для установления диагноза в невыясненных случаях используют модифицированные критерии Университета Дьюка (Duke-критерии, 1994, 2004). Они включают:
"Большие" признаки (ургентные показания к проведению эхокардиографии и госпитализации):
• новое поражение клапана (шум регургитации)
• эпизоды эмболии неизвестного происхождения (особенно инфаркты мозга и почек)
• сепсис неизвестного происхождения
• гематурия, гломерулонефрит или подозрение на инфаркт почки
• лихорадка в сочетании с
- наличием протезированными клапана или другого имплантированного внутрисердечной материала
- другими факторами, способствующими возникновению инфекционного эндокардита
- желудочковой аритмией, возникшей впервые, или нарушениями проводимости
- сердечная недостаточность, возникшая впервые
- положительными посевами крови (если идентифицированы микроорганизмы типичные для инфекционного эндокардита)
- кожными (узелки Ослера, пятна Джейнуэя) или глазными (пятна Рота) проявлениями инфекционного эндокардита
- множественными и швидкозминюванимы легочными инфильтратами (при инфекционном эндокардите правых отделов сердца)
- периферийными абсцессами (почки, селезенки) невыясненного происхождения
- недавними диагностическими или лечебными манипуляциями, что сопровождаются существенным бактериемии при наличии склонности к инфекционного эндокардита.
"Малые" признаки:
• повышение температуры тела без вышеперечисленных признаков.
Точность критериев Университета Дьюка приближается к 100%. Они особенно информативны для диагностики инфекционного эндокардита правых отделов сердца, а также в случае отрицательных результатов посева крови ("вероятно" инфекционный эндокардит).
Дифференциальная диагностика. Из-за отсутствия специфических признаков инфекционного эндокардита дифференциальную диагностику его проводят с широким кругом заболеваний, иногда может представлять значительные трудности.
Если "необъяснимое" повышение температуры тела сочетается с грубым шумом в сердце вследствие его органической недостатки, подтвержденной данными анамнеза и эхокардиографии, следует иметь в виду возможность ревмокардита. Для него характерно возникновение заболевания почти исключительно в детском возрасте и очень редко - в юношеском, быстрое исчезновение артралгии и артрита при применении НПВП, другие кожные проявления (кольцевидная эритема), в части случаев острой ревматической лихорадки - хорея.
У больных с "невыясненной" лихорадкой и неспецифическим шумом в сердце без четких признаков его органического недостатка или без шума дифференциальную диагностику проводят в рамках синдрома лихорадки неясного генеза, причинами которого могут быть:
1) заболевания инфекционного происхождения, прежде сепсыс, туберкулез, остеомиелит, очаги гнойной инфекции в брюшной полости
2) острая ревматическая лихорадка
3) аутоиммунные заболевания, преимущественно системная красная волчанка, узелковый полиартерит и другие системные васкулиты с поражением мелких и средних артерий, дермато (поле) миозит
4) злокачественные опухоли из Паранеопластические реакциями, прежде лимфомы.
Инфекционный эндокардит с аутоиммунными осложнениями требует проведения дифференциальной диагностики с эндокардитом Либмана-Сакса при системной красной волчанке. О наличии системной красной волчанки свидетельствуют характерные кожные проявления (симптом бабочки, энантема, капи-ляриты и др.)., Фотосенсибилизация, полисерозит, лейкопения, а также наличие LE-клеток и высоких титров антител к ДНК и других компонентов ядерного материала. При эндокардите Либмана-Сакса, в отличие от инфекционного эндокардита, существенная дисфункция клапанов сердца развивается редко, редко наблюдают тромбоэмболии, часто результаты многочисленных посевов крови бывают отрицательными.
При наличии лихорадки с бактериемии и отсутствия четких клинических и инструментальных признаков органического порока сердца сложна дифференциальная диагностика инфекционного эндокардита и сепсиса. Диагноз инфекционного эндокардита в этих случаях базируется на выявлении признаков поражения сердца в процессе динамического наблюдения.
Особые сложности представляет распознавания инфекционного эндокардита в тех случаях, когда на первый план выступает одно из его осложнений, например тромбоэмболия, а признаки инфекционного заболевания слабо выражены и могут быть зачислены сопутствующих заболеваний ( хронического пиелонефрита, хронического бронхита или пневмонии). Это особенно характерно для лиц пожилого возраста, у которых часто обнаруживают полиорганной патологии, низкую реактивность иммунной системы и субклинические дегенеративные поражения митрального и аортального клапанов, сопровождающихся систолическим шумом.
Лечение
Основой медикаментозного лечения инфекционного эндокардита является антибактериальная терапия. Ее нужно начинать эмпирически сразу после трех заборов крови на стерильность. Выбор стартовых препаратов является важнейшей задачей, потому что во многом определяет прогноз заболевания.
Терапия инфекционного эндокардита представляет определенные трудности, так как возбудители, содержащиеся в вегетацию, защищенные слоем фибрина и из-за низкой активности метаболических процессов нередко характеризуются повышенной резистентностью к действию антибиотиков. В связи с этим эмпирическую терапию инфекционного эндокардита следует начинать с максимально активных антибиотиков широкого спектра действия.
Для максимальной эффективности антибиотикотерапии инфекционного эндокардита необходимо обеспечить устойчивое поддержание бактерицидной концентрации этих препаратов внутри вегетаций. С этой целью рекомендуют:
- применение антибиотиков с бактерицидным, а не бактериостатическим действием
- парентеральное, желательно внутривенное, введение антибиотиков, что позволяет поддерживать максимально высокую концентрацию препаратов в крови в течение большей части суток. Переход на пероральный употребление возможно лишь в отдельных случаях после получения хорошего и стойкого эффекта от парентерального введения препарата и, желательно, подтверждение высокой чувствительности к нему возбудителя при тестировании in vitro
- использование комбинаций антибиотиков, которые дают аддитивный эффект, прежде всего при низкой чувствительности возбудителя. Самой распространенной из таких комбинаций является сочетание р-лактаму (бензилпенициллина, ампициллина, цефалоспоринов) с аминогликозидом гентамицина сульфатом
- достаточную длительность лечения. Она в значительной степени зависит от вида возбудителя, но в основном составляет не менее 4 нед. В некоторых случаях, например при стафилококковом или грибковом эндокардите, инфекционном эндокардите протезированных клапанов или позднем начале лечения - через 6 нед и более после возникновения заболевания - продолжительность лечения достигает 1,5 мес и более. Ранняя отмена антибиотика к полной эрадикации инфекции грозит появлением рецидива.
В каждом конкретном случае антибактериальный препарат подбирают индивидуально, с учетом спектра его антимикробной активности, резистентности к нему распространенных возбудителей. Современная антибактериальная терапия инфекционного эндокардита определена Рекомендациями по лечению инфекционного эндокардита ЕТК (2004), основанные на результатах большого количества исследований.
Эмпирическую терапию после трех заборов крови начинают при осложнении сепсисом, тяжелой клапанной дисфункцией, нарушениями проводимости или эмболиями. Лечение в режиме эмпирической антибактериальной терапии рекомендуется также в случае отрицательного результата микробиологического исследования (табл. 15).
Таблица 15
Режимы антибиотикотерапии при инфекционном эндокардите естественных и протезированных клапанов

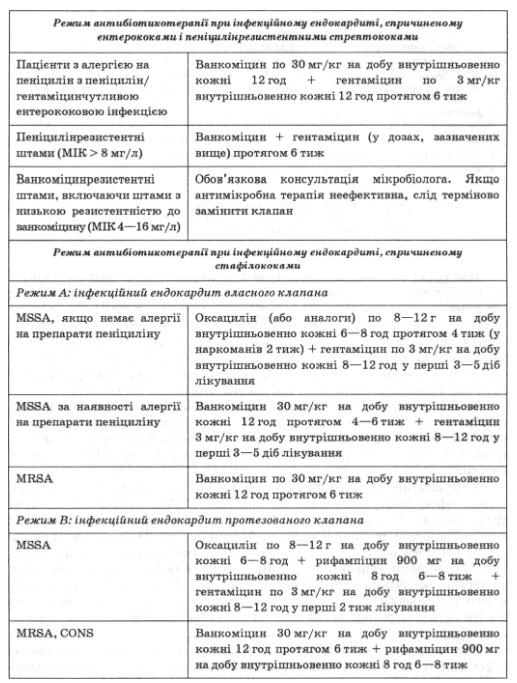

Об эффекте антибиотикотерапии судят прежде всего по динамике температуры тела. В случае устойчивого сохранения ее в течение недели или более от начала введения антибиотиков или возобновления после периода нормализации можно думать о неэффективности антибактериального лечения. Если лихорадка сохраняется при положительных результатах посева крови, следует думать о резистентности возбудителей, содержащихся в вегетацию, с применимым антибиотика или наличие защищенного от него очага инфекции, например абсцесса клапанного кольца и миокарда, септического эмбола или микотического аневризмы.
Терапия в отдельных клинических случаях. При инфицировании имплантированного электрокардиостимулятора или кардиовертера-дефибриллятора антибиотикоте-рапия основывается на результатах посевов крови. Продолжительность лечения основном 4-6 нед. Чаще всего рекомендуют удаление всей имплантированной системы.
В наркоманов, вводящих наркотики внутривенно, в 60-70% случаев инфекционный эндокардит вызванный MSSA. В более 70% больных поражается трехстворчатый клапан. Комплекс лечения включает любой пеницилиназорезистентний пенициллин или ванкомицин. По наркотической пента-зоциновои зависимости дополнительно назначают антипсевдомонадни препараты. При использовании коричневого героина растворяется в лимонном соке, к терапии включают противогрибковые препараты. Наркоманам с поражением клапанов или вовлечением в процесс левых отделов сердца к терапии необходимо добавить антибактериальные препараты, действующие на стрептококковой и энтерококковых флору.
Лечение осложнений. Быстрое и эффективное антибактериальное лечение инфекционного эндокардита может предотвратить эмболических осложнений, если пациент длительное время употреблял антикоагулянты непрямого действия. После установления диагноза инфекционного эндокардита их необходимо отменить и назначить гепарин.
После эмболических осложнений риск повторных эмболий высок. При эмболии сосудов головного мозга повторным эпизодам можно предотвратить путем хирургического вмешательства в ранние сроки (лучше в течение 72 ч). Перед операцией необходимо исключить геморрагический инсульт с помощью компьютерной томографии. Если оперативное вмешательство не выполнено в ранние сроки, то его целесообразно отложить на 3-4 недель.
Хирургическое лечение инфекционного эндокардита обычно проводят у больных со стойкой лихорадкой и бактериемии после курса антибактериальной терапии. Это эффективный метод восстановления внутрисердечной гемодинамики и санации полости сердца.
Показаниями к ургентного хирургического лечения при наличии активного инфекционного эндокардита собственных клапанов является (ЕТК, 2004, с дополнениями):
1) сердечная недостаточность вследствие острой недостаточности аортального или митрального клапана
2) персистивна лихорадка и сохранения бактериемии более 8 суток, несмотря на адекватную антимикробную терапию
3) признаки абсцесса, псевдоаневризмы, фистулы, разрыва одной или нескольких створок клапана, нарушение проводимости миокарда или другие симптомы некон-трольованого местного распространения инфекции
4) наличие микроорганизмов, не поддающихся элиминации антимикробными препаратами (грибы, Brucella, Coxiela), или быстрое разрушение сердечных структур (S. lugdunensis).
Если размеры вегетаций на митральном клапане более 10 мм или они увеличиваются, несмотря на антибиотикотерапию, или имеют вид таких, что "целуются", необходимо как можно раньше провести хирургическое вмешательство.
Прогноз при инфекционном эндокардите правых отделов сердца благоприятный. Хирургическое вмешательство необходимо при повторных эмболии легочных сосудов, если размеры вегетаций на трехстворчатом клапане более 20 мм.
Показаниями к хирургическому вмешательству при активном инфекционном эндокардите протезированными клапана есть (ЕТК, 2004)
1) ранний инфекционный эндокардит (менее 12 мес после оперативного вмешательства)
2) поздний инфекционный эндокардит, который осложнился дисфункцией искусственного клапана, в том числе существенной приклапанною регургитацией или обструкцией при сохранении позитивных посевов крови, формировании абсцесса, нарушениях проводимости, наличия вегетаций больших размеров, особенно стафилококковой этиологии.
Независимо от продолжительности предшествующего лечения антибиотиками перед оперативным вмешательством необходимо проводить полный курс антибиотикотерапии (не менее 7-15 суток).
У большинства больных хирургическое лечение заключается в замене клапанов. Для уменьшения вероятности рецидива показана имплантация клапанных протезов, в кольцо которых введены антисептические субстанции, медленно высвобождаются, - ионы серебра, антибиотики. Только в отдельных случаях, преимущественно при поражении митрального клапана без язв эндокарда и сохраненных пидклапан-ных структурах, возможно выполнение клапанозберигальних оперативных вмешательств путем вырезания краев створок с вегетациями, обработка мест перфорации створок и разрыва хорды. Поражение клапана легочной артерии не требует замены его на протез.
Хирургична летальность зависит от тяжести состояния больных и колеблется от 5 до 30-40%, что существенно ниже, чем среди больных, леченных консервативным способом.
Прогноз
Частота выздоровления при подостром инфекционном эндокардите колеблется в пределах 35-85%. Прогностически неблагоприятными факторами являются позднее начало лечения вследствие запоздалой диагностики, резистентность возбудителя к антибиотикам, невозможность его идентификации, наличие сердечной недостаточности, перенесенный инсульт и возраст более 60 лет. Инфекционный эндокардит протезированных клапанов, особенно ранней, имеет значительно худший прогноз, чем эндокардит собственных клапанов. Существенное влияние на результаты лечения имеет этиология инфекционного эндокардита. Прогноз хуже у больных эндокардит, вызванный грибами, стафилококками и pseudomonas.
Несмотря на эрадикацию инфекции, около 40% больных остаются инвалидами из-за выраженной застойной сердечной недостаточностью и остаточные явления перенесенного инсульта. Поздними осложнениями после клинического и микробиологического выздоровления является рецидив первичной инфекции, повторный инфекционный эндокардит и неинфекционной патологии.
В основных неинфекционных осложнений вылеченного инфекционного эндокардита относится развитие или усиление сердечной недостаточности вследствие остаточной дисфункции клапанов, инсульт и развитие микотического аневризмы.
Частота повторного инфекционного эндокардита, возникает через 6 мес и более после первичного, составляет около 5-8%. Он может развиваться как на пораженных, так и на интактных клапанах и обусловлено той же или другой инфекцией. На повторный инфекционный эндокардит всего подвергаются наркоманы и больные с врожденными, ревматическими и дегенеративными пороками сердца. Прогноз его хуже, чем в случае первичного инфекционного эндокардита.
Профилактика
Связь с медицинскими манипуляциями, способными вызвать преходящую бактериемии, прослеживают менее чем в 20% случаев инфекционного эндокардита. Однако даже в этих случаях нельзя исключить возможность другого источника инфицирования клапанов, в частности такого распространенного, как энергичное чистки зубов или активное жевание твердой пищи при наличии периодонтита. Несмотря на такую, в общем небольшую, количество случаев инфекционного эндокардита, через тяжесть этого заболевания, что составляет непосредственную угрозу для жизни больного, его профилактика является важным медицинским задачей.
соответствии с Рекомендациями ЕТК (2004), проведения профилактики инфекционного эндокардита показана при наличии таких факторов риска:
1. Факторы риска, связанные с патологией сердечно-сосудистой системы (* группа высокого риска):
- искусственные клапаны сердца *
- созданные во время кардиохирургической операции Кондуит *
- инфекционный эндокардит в анамнезе *
- сложные врожденные пороки сердца с цианозом *
- приобретенные пороки сердца
- пролапс митрального клапана с митральной регургитацией или значительным утолщением створок клапана
- врожденные пороки сердца без цианоза (кроме вторичного дефекта межпредсердной перегородки), в том числе двустворчатый клапан
- гипертрофическая кардиомиопатия.
2. Некардиального факторы риска:
- те, что способствуют образованию Абактериальный тромботических вегетаций
- те, что способствуют снижению антибактериальной защиты организма
- те, которые увеличивают риск возникновения и интенсивности бактериемии
- пожилой возраст.
3. Диагностические и лечебные мероприятия, сопровождающиеся бактериемии:
- бронхоскопия (жестким инструментом)
- цистоскопия при наличии инфекции мочевой системы
- биопсия мочевых путей или предстательной железы
- стоматологические процедуры, сопровождающиеся риском травмы десен или слизистой оболочки
- тонзилекгомия или аденоицектомия
- эзофагальная дилатация и склеротерапия
- манипуляции на желчных путях при их обструкции
- трансуретральная резекция предстательной железы
- инструментальные диагностические и лечебные вмешательства на мочеиспускательном канале
- литотрипсия
- вскрытие и дренирование любых инфицированных тканей
- гинекологические процедуры при наличии инфекции
- роды при наличии инфекции.
Профилактика инфекционного эндокардита при стоматологических манипуляциях, вмешательствах в полости рта, пищеводе и на верхних дыхательных путях предусматривает назначение при отсутствии аллергии на препараты пенициллина амоксициллина внутрь в дозе 2 г за 1 ч до манипуляции или ампициллина внутримышечно или внутривенно в дозе 2 г за 30 мин до вмешательства и впоследствии 1 г через 6 ч после введения первой дозы. В случае аллергии на препараты группы пенициллина рекомендуют использовать один из такивариантов пероральной профилактики: клиндамицина 600 мг или азитромицина 500 мг за 1 ч до манипуляции.
При процедурах и оперативных вмешательствах на органах мочеполовой системы и нижнего отдела пищеварительной системы рекомендуют одну из схем:
1) для больных с высоким риском - ампициллин 2 г (или амоксициллин 2 г) + гентамицин 1,5 мг /кг за 0,5-1 ч до процедуры и ампициллин 2 г (или амоксициллин 2 г) внутрь через 6 часов после процедуры
2) для больных со средним риском ампициллин или амоксициллин по 2 г за 0,5-1 ч до процедуры
3) в случае аллергии на препараты пенициллина: больным с высоким риском - ванкомицин по 1 г за 1-2 ч до процедуры + гентамицин по 1,5 г /кг внутривенно или внутримышечно 'внутримышечно; больным со средним риском рекомендуют ванкомицин без гентамицина.
Дальнейшая информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам. Информация предназначена только для медицинских специалистов.