- Склад
- Лікарська форма
- Фармакотерапевтична група
- Фармакологічні властивості
- Клінічні характеристики
- Показання
- Протипоказання
- Взаємодія з іншими засобами
- Особливості застосування
- У період вагітності
- При керуванні автомобілем
- Спосіб застосування та дози
- Діти
- Передозування
- Побічні реакції
- Термін придатності
- Умови зберігання
- Упаковка
- Категорія відпуску
- Виробник
- Місцезнаходження виробника
Кафнеа інструкція із застосування
Офіційна інструкція лікарського засобу Кафнеа розчин 40 мг/2 мл. Опис та застосування Kafnea, аналоги та відгуки. Інструкція Кафнеа розчин затверджена виробником.
Склад
діюча речовина: caffeine citrate;
1 флакон (2 мл) містить кофеїну цитрату 40 мг, що еквівалентно кофеїну основи 20 мг;
допоміжні речовини: кислота лимонна, моногідрат; натрію цитрат; вода для ін’єкцій.
Лікарська форма
Розчин для ін’єкцій.
Основні фізико-хімічні властивості: безбарвний розчин, вільний від будь-яких видимих часток.
Фармакотерапевтична група
Психоаналептики. Психостимулятори, засоби, що застосовуються при синдромі порушення уваги та гіперактивності (ADHD), та ноотропні засоби. Похідні ксантину.
Код АТХ N06B C01.
Фармакологічні властивості
Фармакодинаміка.
Кофеїн є стимулятором дихальної системи центральної дії. Він значно збільшує частоту дихальних рухів (вдихів/хвилину) у недоношених немовлят, а також значуще знижує кількість короткочасних і тривалих нападів апное. Є дані про те, що кофеїн чинить прямий вплив на міокард. Було відзначено, що у недоношених немовлят, які знаходяться на штучній вентиляції легень (ШВЛ), кофеїн знижує опір дихальних шляхів і збільшує податливість легень із супутнім зменшенням потреби у вдиханні кисню.
У недоношених немовлят з апное було виявлено наведені нижче фармакодинамічні ефекти кофеїну.
- Кофеїн підвищує частоту серцевих скорочень;
- кофеїн збільшував частоту дихальних рухів у деяких дослідженнях, але не у всіх;
- середній артеріальний тиск, TcPO2 (транскутанний парціальний тиск кисню), TcPCO2 (транскутанний парціальний тиск вуглекислого газу) не змінюються;
- об’єм кровотоку у черевній артерії та верхній брижовій артерії, LVO (лівошлуночковий викид), PCO2 (парціальний тиск вуглекислого газу) значним чином не змінюються;
- кофеїн підвищує мозковий кровотік у деяких дослідженнях, але не у всіх.
Фармакокінетика.
Абсорбція
Після внутрішньовенного введення навантажувальної дози 20 мг/кг кофеїну цитрату середній піковий рівень кофеїну у плазмі крові становить 12 мг/л. Після внутрішньовенної інфузії разової дози 10 мг/кг кофеїну цитрату середня ± СВ (стандартне відхилення) концентрація кофеїну у сироватці крові становила 14,5 ± 1,4 мкг/мл через 10 хвилин, 11,3 ± 0,1 мкг/мл через 24 години та 6,1 мкг/мл через 72 години. Після застосування навантажувальної дози 10 мг/кг кофеїну цитрату і перорального застосування підтримувальної дози 5 мг/кг/добу або 10 мг/кг/добу сироваткова концентрація досягала рівноважного стану приблизно через 5 діб, при цьому вища концентрація спостерігалася при застосуванні підтримувальної дози 5 мг/кг (див. рисунок нижче). Після застосування підтримувальних доз кофеїну цитрату 5 мг/кг рівні кофеїну у плазмі крові коливаються від 5 до 15 мг/л.
Розподіл
Кофеїн швидко розподіляється в організмі немовлят з об’ємом розподілу (V) 0,8−0,9 л/кг.
Метаболізм
У недоношених немовлят кофеїн погано метаболізується. Основними метаболітами кофеїну є параксантин (головний метаболіт), теобромін і теофілін. У недоношених немовлят спостерігалося взаємоперетворення між кофеїном і теофіліном та очікується, що приблизно 3−8 % введеного кофеїну перетворюватиметься на теофілін.
Кофеїн метаболізується у печінці за допомогою ферментів цитохрому Р450, головним чином CYP1A2. Цей фермент каталізує N1-, N3- та N7-деметилювання кофеїну. Крім того, CYP2E1 також каталізує N1- та N7-деметилювання, тоді як CYP3A каталізує 8-гідроксилювання. Метаболічні шляхи N3- та N7- є незрілими приблизно до 4 місяця після народження, що пояснює тривалий період напіввиведення і низький кліренс у немовлят віком до 4 місяців.
мкг/мл 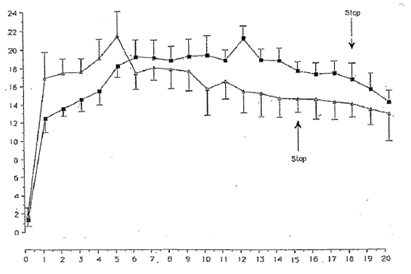
Дні життя.
Рисунок. Середні ± СВ сироваткові концентрації кофеїну після застосування кофеїну цитрату 10/5 (навантажувальна/підтримувальна доза) мг/мл [■] 13 недоношеним новонародженим і кофеїну цитрату 10/2,5 (навантажувальна/підтримувальна доза) мг/мл [Δ] 10 недоношеним новонародженим.
Виведення
Більше ніж 85 % кофеїну виводиться із сечею у незміненому вигляді. У недоношених немовлят (гестаційний вік від 28 до 32 тижнів) 85−97 % кофеїну виводиться у незміненому вигляді. Кінцевий період напіввиведення у немовлят зменшується від народження і досягає значення, характерного для дорослих, приблизно через 60 тижнів. Період напіввиведення кофеїну у недоношених новонароджених значно довший, ніж у новонароджених, які народилися вчасно. Середній кінцевий період напіввиведення у новонароджених коливається від 65 до 102 годин. Виведення кофеїну у недоношених немовлят повільне, а період напіввиведення становить від 80 до 120 годин. Після припинення лікування сироваткові концентрації кофеїну, ймовірно, залишаються підвищеними внаслідок тривалого періоду напіввиведення препарату (див. рисунок вище).
Особливі групи пацієнтів
Новонароджені азійського походження добре переносили внутрішньовенну навантажувальну дозу 20 мг/кг кофеїну цитрату із внутрішньовенним застосуванням підтримувальної дози 5 мг/кг/добу кофеїну цитрату. Застосування вищої підтримувальної дози призводило до підвищення частоти виникнення гіперглікемії та тахікардії.
В інших дослідженнях не було встановлено впливу статі або расової приналежності на об’єм розподілу кофеїну. Порушення функції печінки, визначене за рівнями креатиніну або сечовини у сироватці крові, не впливає на об’єм розподілу.
Клінічні дослідження.
Дослідження ефективності
У рандомізованому, подвійному сліпому, плацебо-контрольованому дослідженні, проведеному Erenberg та ін., оцінювали ефективність і безпеку застосування кофеїну цитрату для лікування апное у недоношених новонароджених. У дослідженні загалом брали участь 87 недоношених немовлят віком від 28 до 32 тижнів від моменту запліднення. Немовлята, яких рандомізували до групи кофеїну, отримували внутрішньовенно навантажувальну дозу 20 мг/кг кофеїну цитрату. Добову підтримувальну дозу кофеїну цитрату 5 мг/кг вводили в лікарській формі розчину для ін’єкцій внутрішньовенно або у вигляді розчину для перорального застосування протягом 10 днів.
Первинною кінцевою точкою було зниження щонайменше на 50 % частоти епізодів апное у порівнянні з вихідним рівнем і усунення апное. Кофеїну цитрат був значно більш ефективним, ніж плацебо, за показником зниження частоти епізодів апное щонайменше на 50 % за 6 днів (р < 0,05). Відсоток пацієнтів, у яких частота епізодів апное знизилася на 50 %, становив 68,9 % у групі активного лікування у порівнянні із 43,2 % у групі плацебо (р = 0,02). Кофеїну цитрат також був значно ефективнішим для усунення апное за 5 днів (р < 0,05). Відсоток пацієнтів, у яких епізоди апное були усунені, становив 24,4 % у групі активного лікування у порівнянні з 0 % у групі плацебо (р = 0,005).
Дослідження безпеки
Довгострокове дослідження безпеки, проведене Schmidt та ін., являло собою великомасштабне міжнародне дослідження за участю 2006 рандомізованих недоношених немовлят з масою тіла при народженні від 500 до 1250 г, у якому порівнювали кофеїн із плацебо з метою встановлення короткострокової та довгострокової безпеки кофеїну при лікуванні апное у недоношених немовлят, профілактиці апное у недоношених немовлят або сприянні екстубації. Немовлята у групі лікування препаратом отримували внутрішньовенну навантажувальну дозу 20 мг/кг кофеїну цитрату з подальшим застосуванням добової підтримувальної дози 5 мг/кг в лікарській формі розчину для ін’єкцій внутрішньовенно або у вигляді перорального розчину. Якщо апное зберігалося, добова підтримувальна доза могла бути збільшена максимум до 10 мг/кг. Підтримувальну дозу коригували щотижня у зв’язку зі зміною маси тіла.
Таблиця 1
Первинні та вторинні результати із клінічного дослідження Schmidt та ін.
Первинний результат (у коригованому віці 10−21 місяць) | Р-значе-ння | Інші результати (у коригованому віці 10−21 місяць) | Р-значе-ння | Вторинні короткострокові результати (до першої виписки додому) | Р-значе-ння |
Комбінований | Ретинопатія недоношених | Смерть | 0,75 | ||
Смерть або інвалідність | 0,008 | Усі стадії | 0,06 | Бронхолегенева дисплазія | < 0,001 |
Складові | Тяжка ретинопатія | 0,01 | Ретинопатія недоношених | 0,09 | |
Смерть до 18 місяців | 0,87 | Церебральний параліч | 0,2 | Ушкодження мозку | 0,44 |
Церебральний параліч | 0,009 | Судомні напади | 0,85 | Некротизуючий ентероколіт | 0,63 |
Затримка розвитку когнітивних функцій | 0,04 | Процентиль росту | 0,88 | Медикаментозна терапія тільки з приводу відкритої артеріальної протоки | < 0,001 |
Тяжка втрата слуху | 0,41 | Процентиль маси тіла | 0,66 | Хірургічне лікування відкритої артеріальної протоки | < 0,001 |
Двостороння сліпота | 0,58 | Окружність голови | 0,12 |
Доклінічні дані з безпеки.
Генотоксичність
Дослідження мутагенності у бактерій і ссавців in vitro, а також дослідження кластогенності in vitro та in vivo загалом не продемонстрували мутагенності та кластогенності кофеїну. У деяких дослідженнях спостерігалися позитивні результати, але у цих дослідженнях застосовували надзвичайно високі концентрації, летальні дози або невалідизовані методи. Вважається, що препарат Кафнеа не становить генотоксичної небезпеки для пацієнтів.
Канцерогенність
У невеликій кількості досліджень на тваринах кофеїн не продемонстрував канцерогенності або онкогенності. У дворічних дослідженнях канцерогенності, проведених на щурах, кофеїн (введений у чистому вигляді) не збільшував частоту утворення пухлин при застосуванні доз перорального розчину до 102 мг/кг/добу самцям і 170 мг/кг/добу самкам. Системна експозиція у тварин при застосуванні таких доз за розрахунками у 2−6 разів вища за таку у новонароджених при застосуванні рекомендованої підтримувальної дози 5 мг/кг/добу кофеїну цитрату.
Клінічні характеристики
Кафнеа Показання
Короткострокове лікування апное у недоношених немовлят гестаційного віку від 28 до 33 тижнів.
Протипоказання
Підвищена чутливість до діючої речовини або до будь-якої з допоміжних речовин.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Існує мало даних про взаємодії лікарських засобів з кофеїном у недоношених новонароджених. Однак CYP1A2 є основним ферментом, відповідальним за метаболізм кофеїну, тому кофеїн має потенціал до взаємодії з препаратами, які є субстратами для цього ферменту або інгібують його, або знижують його кількість. Дослідження за участю дорослих пацієнтів продемонстрували, що одночасне застосування мексилетину, циметидину, флувоксаміну, ідроциламіду для перорального застосування, метоксалену для перорального застосування і 5-метоксипсоралену, еноксацину, тіабендазолу, артемізиніну, флуконазолу і тербінафіну, верапамілу може знижувати виведення кофеїну. Одночасне застосування фенітоїну може збільшувати виведення кофеїну. Кофеїн пригнічує ефекти бензодіазепінів. Кофеїн підвищує рівні як ендогенного, так і введеного перорально мелатоніну, а також клозапіну. Кофеїн може спричиняти зниження біодоступності флувоксаміну.
При одночасному застосуванні антибактеріальних засобів, таких як ципрофлоксацин, еноксацин і піпемідова кислота, ломефлоксацин, норфлоксацин і офлоксацин, повідомляли про збільшення періоду напіввиведення і зниження кліренсу кофеїну.
Не слід одночасно застосовувати інші метилксантини (теофілін, амінофілін).
Особливості застосування
Перед початком лікування необхідно виключити інші причини виникнення апное (наприклад порушення з боку ЦНС, первинне захворювання легень, анемія, сепсис, метаболічні порушення, серцево-судинні порушення або обструктивне апное) або провести їх лікування до початку терапії кофеїну цитратом.
Кофеїн є стимулятором ЦНС, і у разі передозування кофеїну повідомляли про судомні напади. Препарат Кафнеа, розчин для ін’єкцій, слід застосовувати з обережністю немовлятам з епілепсією.
У клінічних дослідженнях було відзначено, що під час лікування у новонароджених може розвиватися некротизуючий ентероколіт. Пацієнтам слід проводити ретельний моніторинг щодо розвитку некротизуючого ентероколіту.
Вплив на серцево-судинну систему
Немовлятам із серцево-судинними захворюваннями препарат Кафнеа слід застосовувати з обережністю, оскільки було відзначено, що кофеїн збільшує частоту серцевих скорочень, лівошлуночковий викид і ударний об’єм.
Порушення функції нирок і печінки
Немовлятам з порушенням функції нирок або печінки препарат Кафнеа слід застосовувати з обережністю. У таких випадках слід контролювати концентрацію кофеїну у сироватці крові та коригувати дозу з метою уникнення потенційної токсичності.
Гастроезофагеальна рефлюксна хвороба
Препарат Кафнеа може розслабляти нижній стравохідний сфінктер і збільшувати виділення шлункової кислоти, що призводить до збільшення частоти епізодів гастроезофагеального рефлюксу у новонароджених.
Застосування у період вагітності або годування груддю
Вплив на репродуктивну функцію
Дані з досліджень на тваринах обмежені, але свідчать про відсутність небезпеки для репродуктивної функції у подальшому при застосуванні кофеїну новонародженим.
Застосування у період вагітності
Не застосовується.
Застосування у період годування груддю
Жінкам, які годують новонароджених дітей, що одержують терапію кофеїну цитратом, слід уникати вживання їжі, напоїв та лікарських засобів, що містять кофеїн. Якщо жінки вживають напої, що містять кофеїн, це слід враховувати при визначенні дози препарату для новонародженого.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами
Застосовується в умовах стаціонару.
Спосіб застосування Кафнеа та дози
Лікарський засіб Кафнеа, розчин для ін’єкцій, призначений для застосування у спеціалізованих неонатологічних відділеннях. Препарат призначений тільки для одноразового застосування одному пацієнту. Слід утилізувати будь-які залишки.
Перед застосуванням препарату слід переконатися, що жодний інший метилксантин (наприклад теофілін та амінофілін) не застосовується.
Необхідно визначити вихідні сироваткові рівні кофеїну, якщо мати дитини під час вагітності вживала рідини, що містять кофеїн, оскільки кофеїн легко проникає через плаценту.
Доза, виражена у перерахунку на кофеїн у чистому вигляді, становить половину від дози кофеїну цитрату (наприклад 20 мг кофеїну цитрату еквівалентно 10 мг кофеїну).
Навантажувальна доза: 20 мг/кг маси тіла кофеїну цитрату внутрішньовенно за допомогою шприцевого інфузомата протягом 30 хвилин.
Підтримувальна доза: 5 мг/кг кофеїну цитрату один раз на добу до зникнення апное або доти, доки лікування вважатиметься більше не потрібним. Якщо апное зберігається, підтримувальну дозу можна збільшити максимально до 10 мг/кг кофеїну цитрату один раз на добу. Слід коригувати підтримувальну дозу щотижня відповідно до зміни маси тіла. Якщо спостерігаються симптоми, що свідчать про токсичність кофеїну, а саме тахікардія, тахіпное (часте дихання), синдром підвищеної нервово-рефлекторної збуджуваності, тремор, судоми невідомої етіології та блювання, слід зменшити дозу кофеїну цитрату або припинити лікування. Слід зменшити дозу кофеїну цитрату або припинити лікування з інших клінічних причин.
Підтримувальну дозу слід вводити внутрішньовенно (протягом 10 хвилин). Підтримувальну дозу починають застосовувати через 24 години після навантажувальної дози.
Синдром відміни кофеїну: про симптоми абстинентного синдрому після короткострокової терапії (менше трьох тижнів) не повідомлялося.
Діти
Препарат застосовують недоношеним новонародженим гестаційного віку від 28 до 33 тижнів.
Передозування
Симптоми
При застосуванні дози, що перевищувала звичайну дозу у три рази, не відзначалося помітних побічних ефектів, окрім підвищення частоти виникнення синдрому підвищеної нервово-рефлекторної збуджуваності та зменшення маси тіла, яка нормалізувалася після припинення лікування. Застосування вищих доз може спричиняти гарячку, дратівливість, погане харчування, сонливість, тахіпное, синдром підвищеної нервово-рефлекторної збуджуваності, дрібний тремор кінцівок, артеріальну гіпертензію, опістотонус, тоніко-клонічні рухи, нецілеспрямовані (неконтрольовані) рухи щелепи і губ, блювання, гіперглікемію, підвищений рівень азоту сечовини у крові, підвищення загальної кількості лейкоцитів, судоми, неврологічні ускладнення, тахікардію, респіраторний дистрес-синдром, серцеву недостатність, здуття живота і ацидоз.
Лікування
У разі передозування кофеїну проводиться переважно симптоматичне і підтримувальне лікування. Було відзначено, що рівні кофеїну у плазмі крові знижуються після замінного переливання крові. Лікування судом може проводитися за допомогою внутрішньовенного застосування діазепаму або барбітуратів, таких як пентобарбітал натрію.
Побічні реакції
Некротизуючий ентероколіт є поширеним явищем у недоношених немовлят, а тому, незалежно від того, чи отримує новонароджений кофеїн, необхідно проводити обстеження щодо розвитку некротизуючого ентероколіту.
Таблиця 2
Відсоткова частка побічних явищ, про які найчастіше повідомляли у ході дослідження Erenberg та ін.
Побічне явище | Група лікування | |
Кофеїну цитрат | Плацебо | |
Реакція у місці ін’єкції | 8,7 | 12,8 |
Перинатальне порушення (залишкові аспірати, харчова непереносимість) | 8,7 | 5,1 |
Запор | 17,4 | 20,5 |
Порушення з боку травної системи (гастроезофагеальний рефлюкс, розширення петель кишечнику) | 4,3 | 7,7 |
Анемія | 6,5 | 17,9 |
Гіпонатріємія | 0 | 5,1 |
Висипання | 8,7 | 7,7 |
У ході неконтрольованих досліджень повідомляли про наведені нижче ефекти.
Стимуляція ЦНС: дратівливість, збудженість, синдром підвищеної нервово-рефлекторної збуджуваності.
Порушення з боку серцево-судинної системи: тахікардія, збільшений лівошлуночковий викид і збільшений ударний об’єм.
Порушення з боку травної системи: збільшена аспірація вмісту шлунка, шлунково-кишкова непереносимість.
Зміни рівня глюкози у сироватці крові: гіпоглікемія і гіперглікемія.
Порушення з боку нирок: підвищення сечовиділення, збільшення кліренсу креатиніну і підвищення виведення натрію і кальцію.
Побічні ефекти, що спостерігалися у контрольованих клінічних дослідженнях Schmidt та ін., включали тахікардію, тахіпное (часте дихання), синдром підвищеної нервово-рефлекторної збуджуваності, тремор, судоми невідомої етіології і блювання. Кофеїн тимчасово зменшував приріст маси тіла.
Термін придатності Кафнеа
3 роки.
Умови зберігання Кафнеа
Зберігати у недоступному для дітей місці при температурі не вище 30 °С.
Несумісність.
Дослідження сумісності не проводилися, оскільки препарат не відновлюється та не розводиться перед застосуванням.
Упаковка
По 2 мл у флаконі; по 10 флаконів у картонній коробці.
Категорія відпуску
За рецептом.
Виробник
Фебра Пті Лтд.
Місцезнаходження виробника
19 Оріон Роуд ЛЕЙН КЕВ Новий Південний Уельс 2066, Австралія.
Подальша інформація
Пам'ятайте, зберігайте ці та всі інші ліки в недоступному для дітей місці, ніколи не передавайте свої ліки іншим і використовуйте Кафнеа тільки за призначенням.
Завжди консультуйтеся зі своїм лікарем, щоб переконатися, що інформація, яка відображається на цій сторінці, може бути застосована до ваших особистих обставин.
Увага! Ця інструкція для медичного застосування лікарського засобу є офіційною інструкцією виробника Фебра Пті Лтд.
Авторське право:
- Фебра Пті Лтд
- http://www.drlz.com.ua - Державний реєстр ЛЗ України
| Тип даних | Відомості з реєстру |
| Торгівельне найменування: | Кафнеа |
| Виробник: | Фебра Пті Лтд |
| Форма випуску: | розчин для ін'єкцій, 40 мг/2 мл, по 2 мл у флаконі; по 10 флаконів у картонній коробці |
| Реєстраційне посвідчення: | UA/17874/01/01 |
| Дата початку: | 17.01.2020 |
| Дата закінчення: | 17.01.2025 |
| Міжнародне непатентоване найменування: | Caffeine |
| Умови відпуску: | за рецептом |
| Склад: | 1 флакон (2 мл) містить кофеїну цитрату 40 мг, що еквівалентно кофеїну основи 20 мг |
| Фармакотерапевтична група: | Психоаналептики. Психостимулятори, засоби, що застосовуються при синдромі порушення уваги та гіперактивності (ADHD), та ноотропні засоби. Похідні ксантину. |
| Код АТС: | N06BC01 |
| Заявник: | Фебра Пті Лтд |
| Країна заявника: | Австралія |
| Адреса заявника: | 19 Оріон Роуд ЛЕЙН КЕВ Новий Південний Уельс 2066, Австралiя |
| Тип ЛЗ: | Звичайний |
| ЛЗ біологічного походження: | Нi |
| ЛЗ рослинного походження: | Нi |
| Гомеопатичний ЛЗ: | Нi |
| Тип МНН: | Моно |
| Дострокове припинення | Нi |
| Код ATC | Назва групи |
| N | Засоби, що діють на нервову систему |
| N06 | Психоаналептики |
| N06B | Психостимулятори, засоби, що застосовуються при синдромі порушення уваги і гіперактивності (adhd) |
| N06BC | Похідні ксантину |
| N06BC01 | Кофеїн |
